Презентація на тему:
Крохмаль і целюлоза. Полімерна будова, властивості, застосування
Завантажити презентацію
Крохмаль і целюлоза. Полімерна будова, властивості, застосування
Завантажити презентаціюПрезентація по слайдам:
Завдання для обговорення У двох пронумерованих пробірках без написів містяться розчини глюкози й сахарози. З’ясуйте дослідним шляхом уміст кожної пробірки. Чому варення солодше за цукор, хоча вариться воно з цукром? Підтвердьте свою відповідь рівнянням реакції. Для чого в молоко додають соду? Напишіть рівняння реакцій, з допомогою яких можна здійснити перетворення: Сахароза → ? → етанол. На які три класи поділяються вуглеводи? Доведіть важливість реакції фотосинтезу для рослин. У чому полягає біологічна роль вуглеводів?
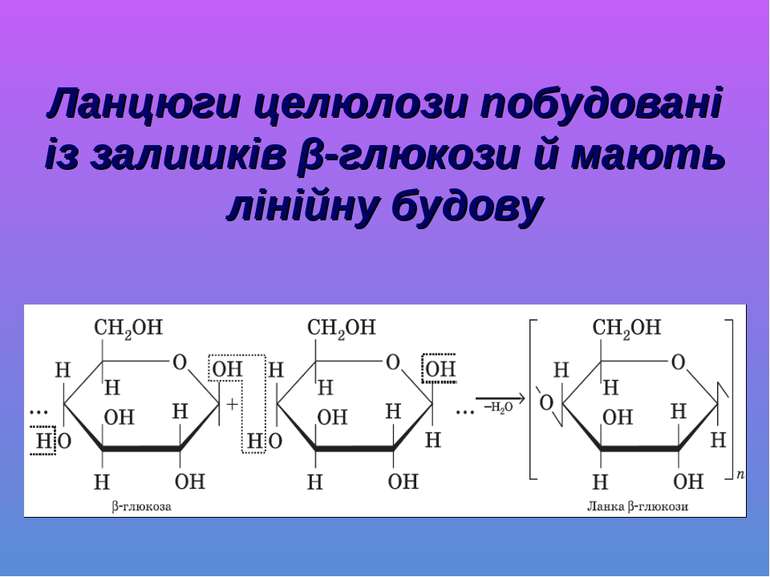
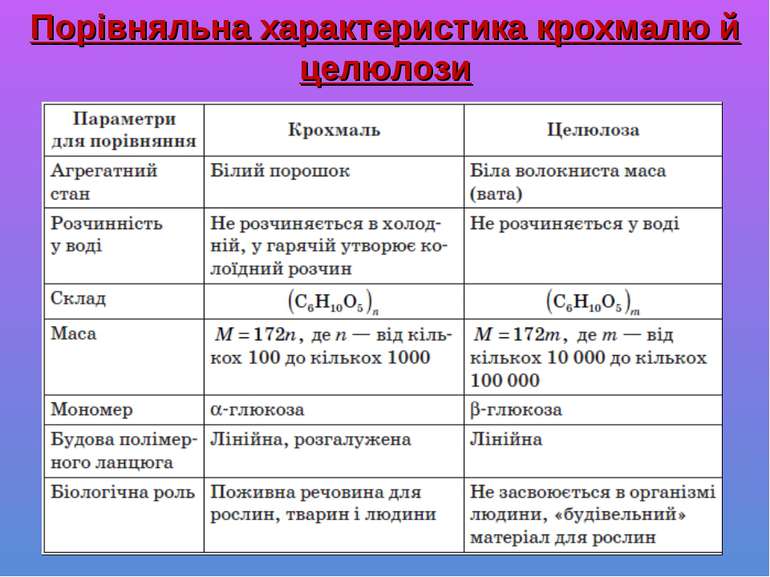
Крохмаль і целюлоза — природні полімери, загальна формула — (C6H10О5)n. Рівняння утворення крохмалю або целюлози можна подати так: nC6 H12 O6 → (C 6 H10 O5)n · nH2O
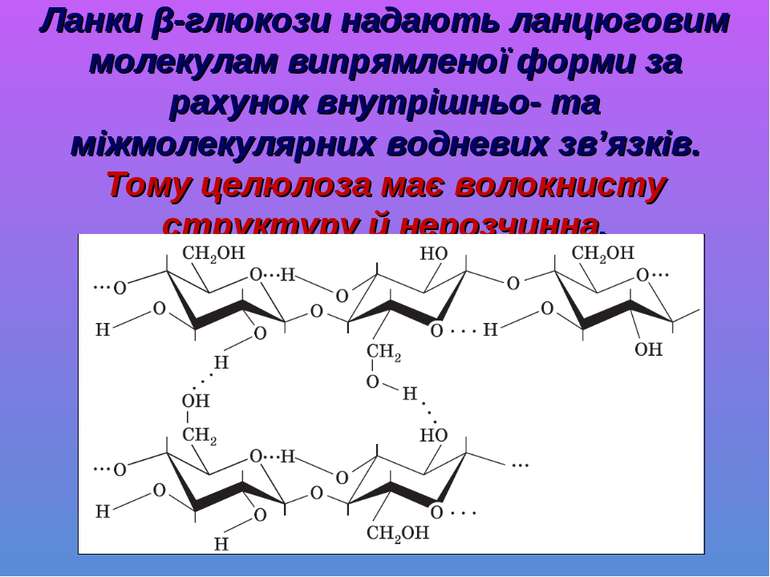
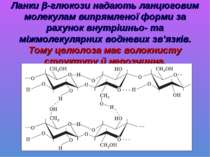
Ланки β-глюкози надають ланцюговим молекулам випрямленої форми за рахунок внутрішньо- та міжмолекулярних водневих зв’язків. Тому целюлоза має волокнисту структуру й нерозчинна.
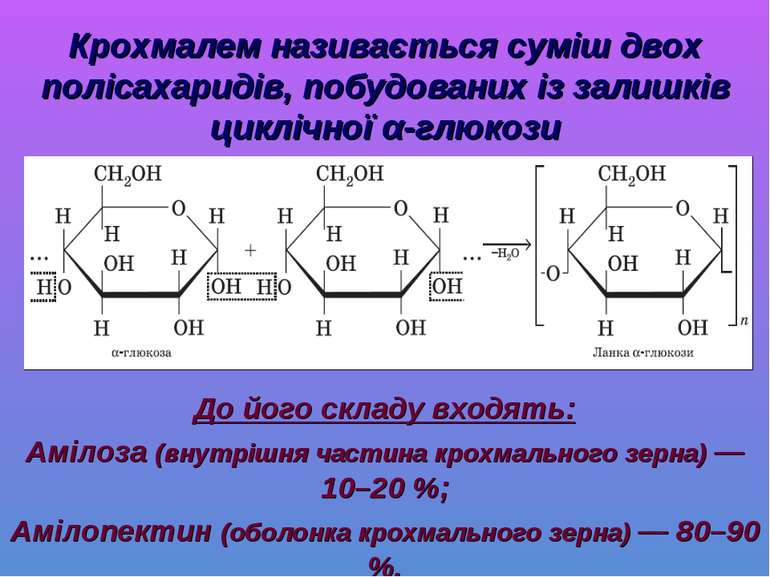
Крохмалем називається суміш двох полісахаридів, побудованих із залишків циклічної α-глюкози До його складу входять: Амілоза (внутрішня частина крохмального зерна) — 10–20 %; Амілопектин (оболонка крохмального зерна) — 80–90 %.
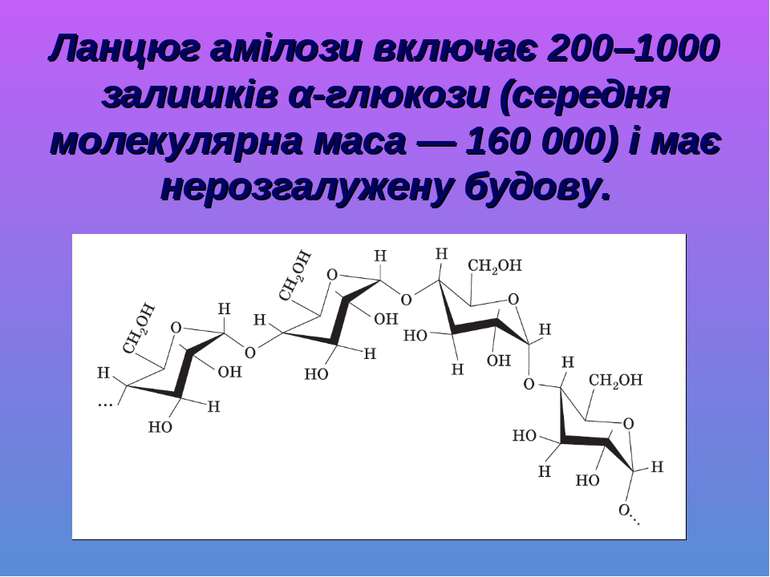
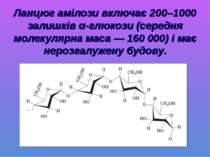
Ланцюг амілози включає 200–1000 залишків α-глюкози (середня молекулярна маса — 160 000) і має нерозгалужену будову.
Під час взаємодії амілози з іодом у водному розчині молекули іоду входять у внутрішній канал спіралі, утворюючи так звану сполуку включення. Ця сполука має характерний синій колір. Ця реакція використовується для виявлення як крохмалю, так і йоду (іодкрохмальна проба).
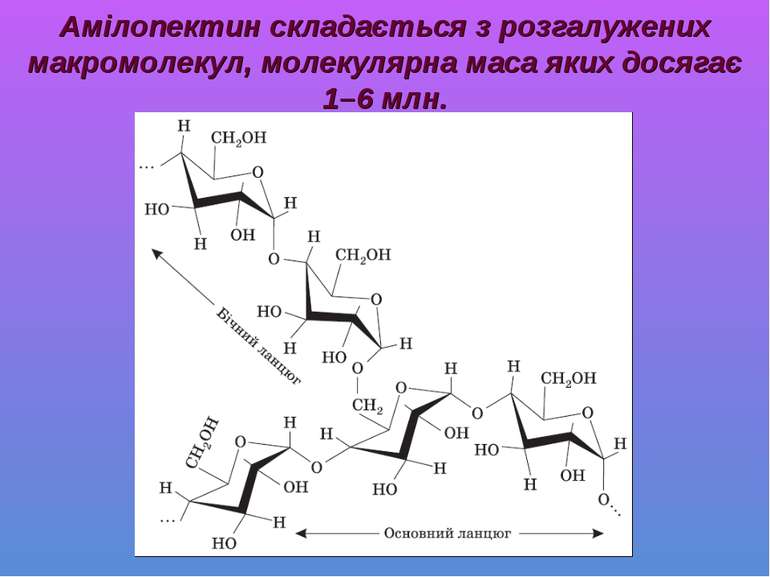
Амілопектин складається з розгалужених макромолекул, молекулярна маса яких досягає 1–6 млн.
Реакція взаємодії крохмалю й целюлози з водою — гідроліз, протікає за нагрівання в кислому середовищі або під дією ферментів: (C6H10O5)n · n H2O → nC6H12O6
Лабораторний дослід 12. Взаємодія крохмалю з водою Дрібку крохмалю розчиніть у холодній воді. Що спостерігаємо? Повільно, дотримуючись правил техніки безпеки й правил нагрівання, нагріваємо вміст пробірки. Що спостерігаємо? Чи можна вважати цей розчин істинним? Як називаються такі розчини?
Лабораторний дослід 13 В отриманий клейстер додайте дві-три краплі розведеного розчину іоду. Що спостерігаємо? (Поява фіолетово-синього забарвлення вказує на наявність крохмалю в розчині) Висновок: дія іоду є якісною реакцією на наявність крохмалю в речовині.
Практика Завдання 1. Обчисліть, скільки крохмалю утвориться в результаті фотосинтезу, якщо рослини виділяють при цьому 10 т кисню. Завдання 2. У двох пробірках містяться крохмаль і глюкоза. Як з допомогою досліду розпізнати ці речовини?
Завдання 3. Нітроцелюлози — продукти взаємодії целюлози й нітратної кислоти, надзвичайно горючі. Тринітроцелюлоза (піроксилін) — вибухова речовина, що застосовується у виробництві бездимного пороху. Під час вибуху відбувається розклад. Запишіть рівняння реакції: Завдання 4. Подумайте, чому із целюлози можна одержати во-локна, а із крохмалю їх одержати не можна.
Домашнє завдання Опрацювати матеріал параграфа, відповісти на запитання до нього, виконати вправи. Творче завдання. Дослідіть різні продукти харчування на наявність крохмалю і складіть звіт.
Презентацію створено за допомогою комп’ютерної програми ВГ «Основа» «Електронний конструктор уроку» © ТОВ «Видавнича група ˝Основа˝», 2012 Джерела: Усі уроки хімії. 9 клас / І. Ю. Старовойтова, О. В. Люсай. — Х.: Вид. група «Основа», 2009. — 239, [1] с.: іл., табл. — (Серія «12-річна школа»). Сайти: bibliomaniya.blogspot.com; school-collection.edu.ru; youtube.com; little-science.ru; lagis.com.ua; cooking.ua; vkusnosti.org
Схожі презентації
Категорії