Презентація на тему:
Провокуюча дія ліків при генетичних порушеннях (спадкові метгемоглобінемії; печінкові порфірії; спадкові жовтяниці; первинна подагра; системний червоний вовчак та ін.). Застосування сучасних лікарських засобів при спадкових захворюваннях
Завантажити презентацію
Провокуюча дія ліків при генетичних порушеннях (спадкові метгемоглобінемії; печінкові порфірії; спадкові жовтяниці; первинна подагра; системний червоний вовчак та ін.). Застосування сучасних лікарських засобів при спадкових захворюваннях
Завантажити презентаціюПрезентація по слайдам:
Провокуюча дія ліків при генетичних порушеннях (спадкові метгемоглобінемії; печінкові порфірії; спадкові жовтяниці; первинна подагра; системний червоний вовчак та ін.). Застосування лікарських засобів при спадкових захворюваннях Лектор проф. Посохова К.А.
Спадкові захворювання, при яких проявляється провокуюча дія ЛЗ Захворювання Печінкові порфірії Первинна подагра Спадкові метгемоглобінемії Токсикогенетичний ефект ЛЗ Загострення захворювання, викликане засобами для наркозу, етанолом, естрогенами та ін. Загострення етанолом, хлортіазидом, фуросемідом Гіперметгемоглобінемія (натрію нітрит, амілнітрит, нітрогліцерин, парацетамол та ін.)
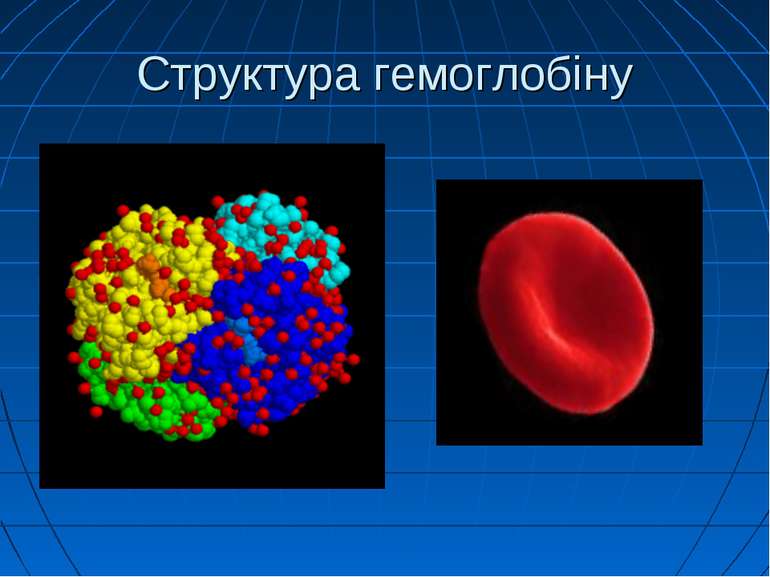
Спадкові метгемоглобінемії Гемоглобін виконує виключно важливу роль як переносник кисню від легень у тканини і вуглекислоти з тканин до легень. У легенях гемоглобін легко окислюється до оксигемоглобіну нестійкої сполуки гемоглобіну з киснем. У тканинах кисень відщеплюється і використовується для різноманітних окисно-відновних реакцій обміну речовин. Оксигемоглобін
Метгемоглобін На відміну від оксигемоглобіну, він містить тривалентне залізо, тому має міцний зв’язок з киснем, непридатний для транспорту кисню в тканини В еритроцитах здорових людей метгемоглобін знаходиться постійно, але в дуже малих кількостях 1-2,5 % від вмісту загального гемоглобіну Утворюється в еритроцитах під впливом оксидантів: пероксидів, продуктів розпаду білків у кишечнику під впливом бактерійної флори Рівень його може зростати до 3-4 % при деяких захворюваннях легень (пневмонії, пневмосклерозі), серця тощо.
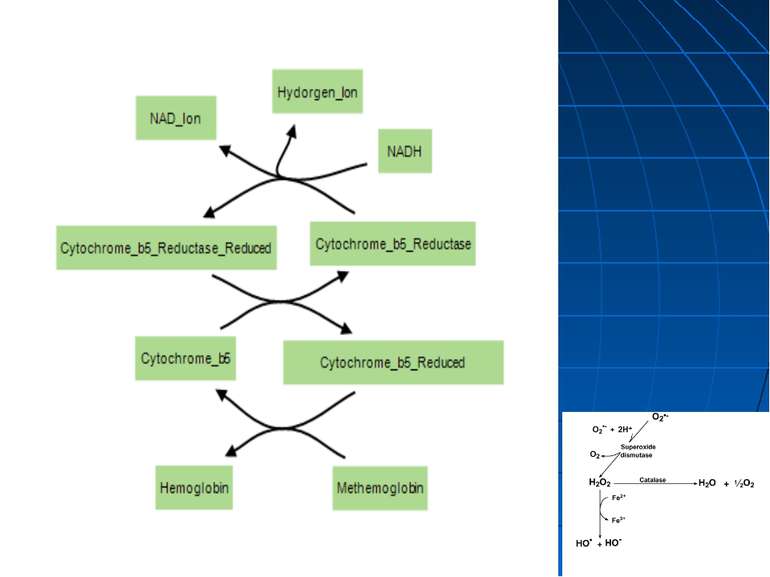
Низький рівень метгемоглобінемії у здорових людей пояснюється постійним відновленням метгемоглобіну в оксигемоглобін, що здійснюється метгемоглобінвідновлювальною системою її компоненти: нікотинамідаденіндинуклеотид (НАД), метгемоглобінредуктаза, глутатіон і аскорбінова кислота, Її допоміжні компоненти: каталаза і глутатіонпероксидаза
Дві форми ферменту, який бере участь у редукції метгемоглобіну в оксигемоглобін: НАД Н2-метгемоглобінредуктаза (метгемоглобінредуктаза-1, або діафораза-1) НАДФ Н2-метгемоглобінредуктаза-2 (метгемоглобінредуктаза-2, або діафораза-2). Провідною з них є діафораза-1. Якщо загальну метгемоглобінвідновлювальну здатність еритроцитів вважати за 100 %, то на активність діафорази-1 припадає близько 70 %, тоді як на діафоразу-2 лише 5-6 % і то тільки при наявності додаткового сильного відновника, наприклад, метиленового синього. Тому діафоразу-2 вважають резервним ферментом. Решта метгемоглобіну відновлюється в оксигемоглобін за допомогою глутатіону (9-12 %) і аскорбінової кислоти (12-16 %).
Рівень метгемоглобіну в крові залежить як від швидкості його редукції, так і від інтенсивності утворення інтенсивність метгемоглобінутворення стримується високим вмістом глутатіону і каталази в еритроцитах
Метгемоглобінутворювальні речовини Існує багато хімічних сполук, які, потрапляючи в організм ззовні, можуть проникати через мембрану еритроцитів і окислювати гемоглобін у метгемоглобін (метгемоглобінутворювальні речовини) До них належать бертолетова сіль, хлорноватистокислі солі, миш’яковистий водень, пірогалол, гідрохінон, гідразин і його похідні, анілін, ряд бактерійних токсинів тощо
Спадкові метгемоглобінемії група гетерогенних захворювань: ензимопенічна НАД Н2-залежна метгемоглобінемія, зумовлена дефіцитом глутатіону метгемоглобінемія у зв’язку з наявністю деяких аномальних гемоглобінів Метгемоглобінемія, яка супроводжує медикаментозний гемоліз в осіб з недостатністю активності Г6ФД еритроцитів Метгемоглобінемія, яка виникає у хворих з спадковою недостатністю печінкових мікросомальних гідроксилаз
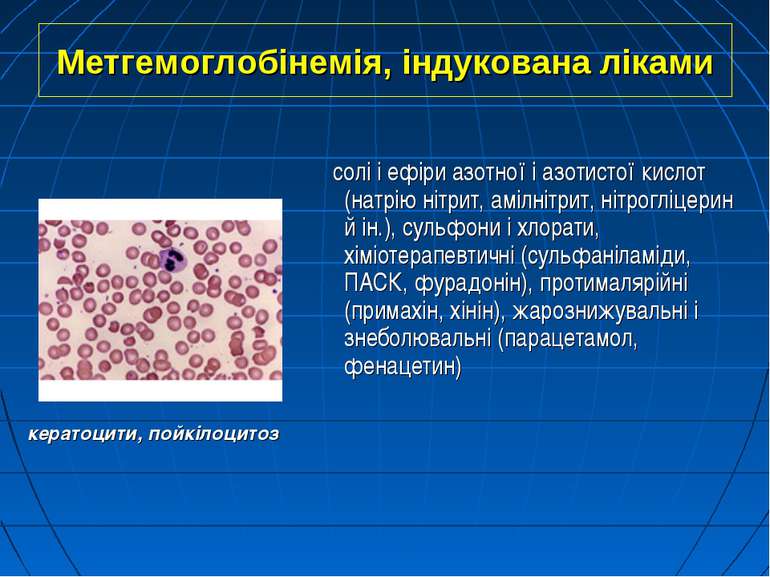
Метгемоглобінемія, індукована ліками солі і ефіри азотної і азотистої кислот (натрію нітрит, амілнітрит, нітрогліцерин й ін.), сульфони і хлорати, хіміотерапевтичні (сульфаніламіди, ПАСК, фурадонін), протималярійні (примахін, хінін), жарознижувальні і знеболювальні (парацетамол, фенацетин) кератоцити, пойкілоцитоз
Ці лікарські засоби у терапевтичних дозах у здорових людей суттєво не впливають на продукцію метгемоглобіну, хоча деякі з них при тривалому прийомі, особливо при передозуванні, можуть викликати недовготривалу метгемоглобінемію
Одним з наслідків спадкових метгемоглобінемій є значна стійкість до дії синільної кислоти і її солей (ціанідів). Такі особи можуть без небезпеки для життя переносити ціанід калію в дозах, що перевищують летальні в 40 разів. Профілактика метгемоглобінемії, зумовленої спадковою недостатністю метгемоглобінредуктази, полягає у своєчасному виявленні осіб з цією ензимопатією і недопущенні приймання вказаних лікарських і токсичних речовин Важливе діагностичне значення має визначення вмісту метгемоглобіну в крові, особливо активності метгемоглобінредуктази.
Лікування у фазі загострення спадкової метгемоглобінемії, яке виникло внаслідок приймання метгемоглобінутворювальних речовин метиленовий синій у вену - по 1-2 мг на 1 кг маси у вигляді 1 % розчину на 5-10 % розчині глюкози Не вводити повторно! - метиленовий синій у великих дозах стимулює метгемоглобінутворення аскорбінова кислота - всередину по 0,3 г 3 рази на день. Порівняно з метиленовим синім, дія аскорбінової кислоти проявляється повільніше і не призводить до повної ліквідації метгемоглобінемії. Аскорбінову кислоту призначають хворим після ліквідації гіперметгемоглобінемії метиленовим синім. введення у вену розчинів натрію гідрокарбонату, преднізолону, сибазону, цистаміну, плазми і тромбоцитарної маси.
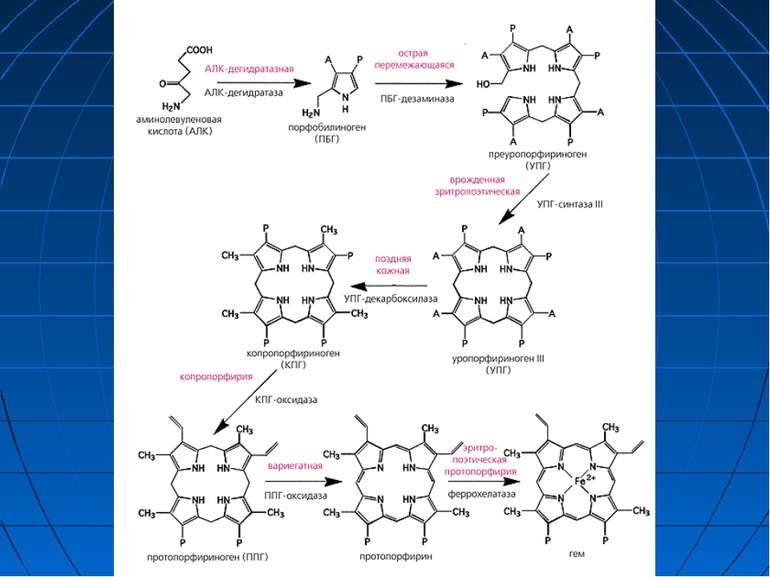
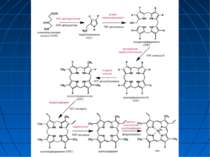
Порфірії Група клінічно близьких захворювань, які проявляються порушенням біосинтезу гему і підвищеною екскрецією протопорфіринів і їх попередників -амінолевулінової кислоти і порфобіліногену Характеризуються автосомно-домінантним типом успадкування з неповною пенетрантністю Активності ферменту, зниженої до ~ 50%, достатньо для нормальної швидкості синтезу гему майже 85% носіїв аномального гену проживають життя, не підозрюючи про цю хворобу
Класифікація порфірій відповідно до місця синтезу гему, в яких проявляються «помилки» метаболізму Печінкова порфірія (первинне порушення – у печінці) Еритропоетична порфірія (первинне порушення – у кістковому мозку) Відповідно до клінічного перебігу гострі форми Форми з переважаючим ураженням шкіри
Гостра порфірія – множинні симптоми I. Абдомінальні — біль у животі, нудота, блювання запор, пронос. II. Серцево-судинні — стійка синусова тахікардія (до 160), гипертонія. II. Неврологічні — м’язова атонія, біль у кінцівках, голові, шиї, грудній клітці; втрата чутливості, ураження черепно-мозкових нервів (дисфагія, диплопія, афонія, парез лицевого і окорухового нервів); порушення тазових функцій; парези і паралічі; параліч дихання. IV. Розлади психіки: безсоння; сильний неспокій; депресія, істерія; сплутаність свідомості і дезорієнтація; галюцінації; тоніко-клонічні судоми; манії; коматозний стан; епілептичні напади. Може призводити до діагностичних помилок!
Фактори, які провокують загострення порфірії перенесений вірусний гепатит С (причина порфірії - у 20-80% випадків у різних країнах світу) Деякі ліки Вживання алкоголю: «Не пий – порфіріком станеш!» гемодіаліз (штучна нирка) продукти органичної хімії, вдихання парів етильованого бензину, ртуті, свинцю
Порфірія Частіше - гостра переміжна порфірія, яка проявляється після закінчення статевого дозрівання, інколи в більш ранньому віці Загострення її при прийомі лікарських засобів: барбітуратів, сульфонів, сульфаніламідів, амідопірину, грізеофульвіну, стероїдних гормонів – ГКС, естрогенів, протизаплідних препаратів, до складу яких вони входять, ряду протиепілептичних засобів і транквілізаторів, наркозних препаратів, етилового спирту, хінгаміну, алілізопропілацетату
Профілактика ускладнень фармакотерапії при печінкових порфіріях передбачає повне виключення вказаних препаратів, які здатні провокувати загострення хвороби Велике значення має виявлення осіб з латентним перебігом захворювання. Для цього використовується навантаження гліколом. Після спеціальної дієти у здорових осіб він не змінює вміст попередників порфіринів у сечі, тоді як при прихованій формі інтермітуючої порфірії їх кількість зростає до 200 %.
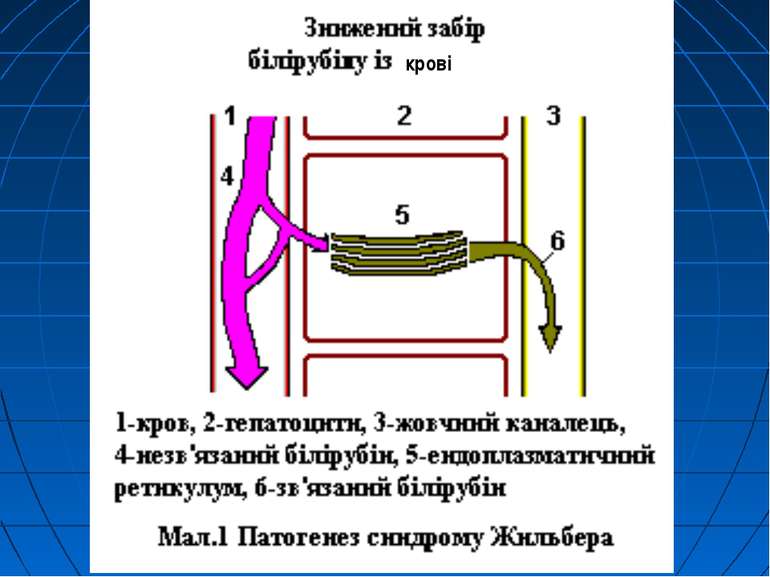
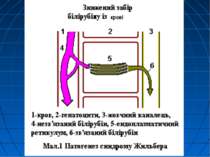
Спадкові жовтяниці Печінка відіграє важливу роль в обміні білірубіну і в метаболізмі багатьох ендогенних речовин і ксенобіотиків. Із різних ланок обміну цього пігменту, на особливу увагу заслуговує процес утворення глюкуронідів білірубіну, що здійснюється в ендоплазматичній сітці гепатоцитів. У цьому процесі бере участь багато ферментів, особливо уридиндифосфатглюкуронілтранс-фераза (УДФГТ), яка здійснює перенесення глюкуронової кислоти від уридинди-фосфатглюкуронової кислоти (УДФГК) до білірубіну, тироксину, деяких стероїдних гормонів, чи чужорідних речовин. Проте при захворюваннях, які супроводжуються різким гемолізом (наприклад, при гемолітичній хворобі новонароджених), білірубінкон’югуюча активність печінки може виявитися недостатньою. Внаслідок цього в крові накопичується все більше і більше некон’югованого (дуже токсичного) білірубіну. Виникає некон’югована гіпербілірубінемія, навіть ядерна жовтяниця.
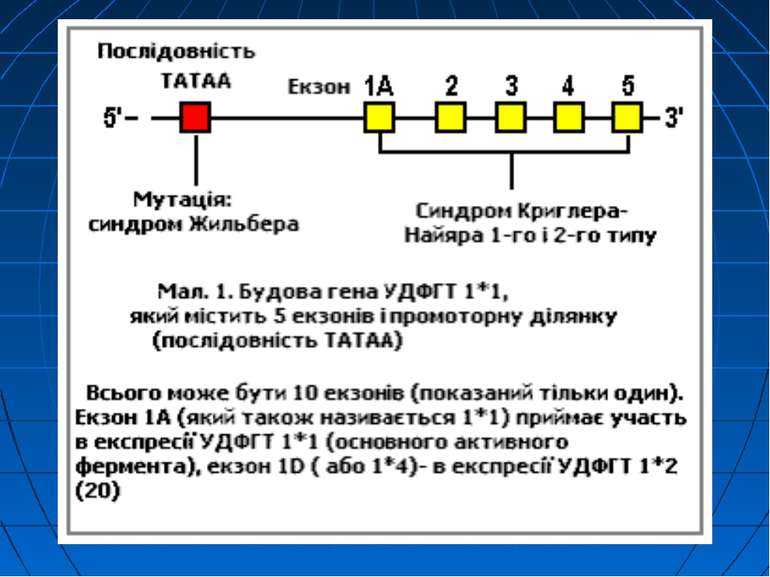
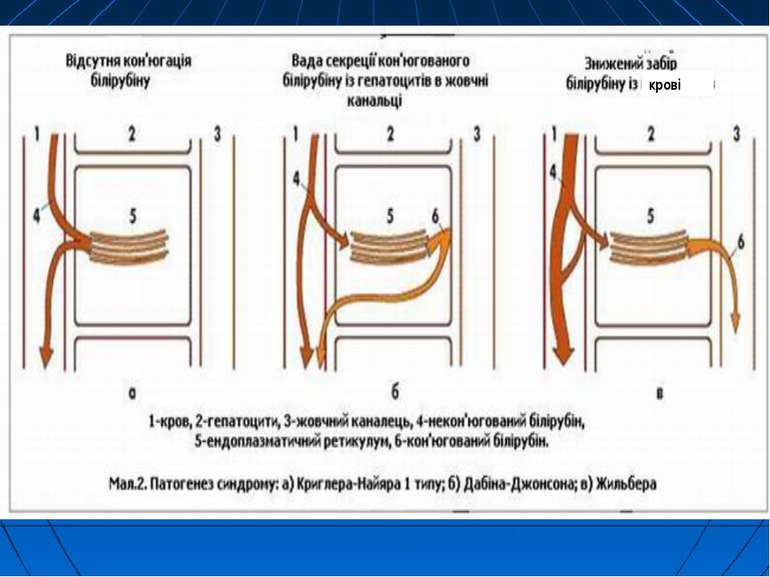
Генетична патологія УДФГТ у людей (родинна негемолітична жовтяниця) Недостатність активності УДФГТ може бути наслідком, по-перше, генетичної патології цього ферменту, по-друге, тимчасової незрілості його, по-третє, результатом інгібуючої дії агентів внутрішнього і зовнішнього середовища. Генетична патологія УДФГТ у людей проявляється в двох формах родинної негемолітичної жовтяниці: а) гіпербілірубінемії негемолітичної спадкової з ядерною жовтяницею (синдром Кріглера-Наджара); б) гіпербілірубінемії юнацької ідіопатичної родинної (синдром Жільбера).
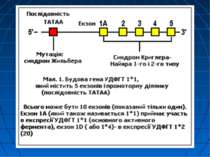
Синдром Кріглера-Наджара важка форма спадкових жовтяниць. Клініка: різко виражена жовтяниця і тяжкі неврологічні прояви, особливо при ядерній жовтяниці жовтяничне забарвлення шкіри з’являється вже на першу добу життя дитини, інтенсивність якого поступово зростає. Жовтяниця продовжується все життя. Рівень білірубіну в більшості випадків перевищує 20 мг %, в окремих хворих досягає навіть 50 мг %. Вміст уробіліногену в сечі і калі дуже низький, стілець ахолічний. На фоні зростаючої гіпербілірубінемії, звичайно через декілька тижнів-місяців після народження з’являються симптоми ураження ЦНС: судоми, підвищення тонусу скелетних м’язів, ністагм, анорексія, опістотонус, психічні розлади. У більшості хворих прояви ядерної жовтяниці наростають, аж до летального наслідку. Діти рідко доживають до 2-3, тим більше 5 років. У легких випадках, що трапляються рідко, прогноз сприятливий, тому що гіпербілірубінемія не досягає високого рівня. При цьому помірна жовтяниця єдиний прояв захворювання.
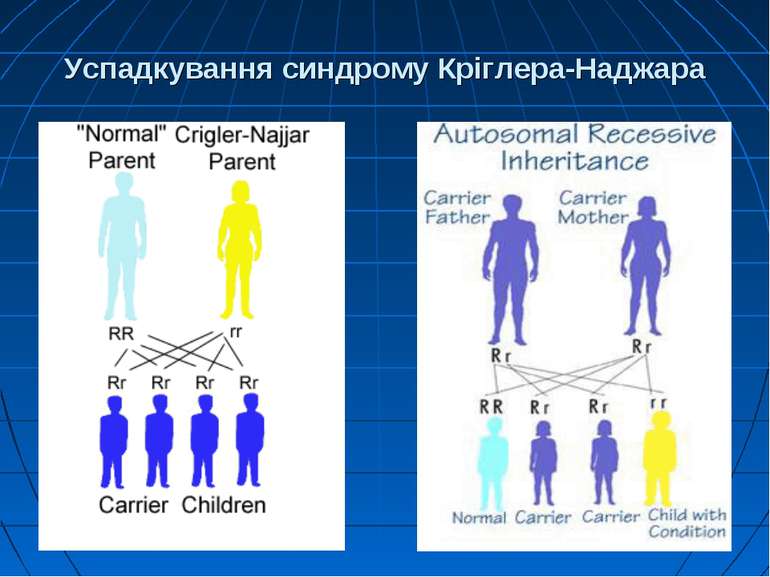
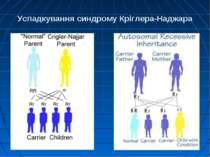
Синдром Кріглера-Наджара Захворювання успадкується за автосомно-рецесивним типом. Виникає у нащадків гомозиготних батьків. У родичів пробанда виявляються гетерозиготні носії дефектного гена. У них патологія печінки може залишатися латентною: утворення глюкуронідів білірубіну і екскреція їх проходять нормально. Але у таких випадках кон’югація лікарських засобів, наприклад, саліцилатів, які звичайно призначаються у великих дозах, здійснюється в недостатній мірі. Це може призвести до підвищення вмісту білірубіну в крові і медикаментозної інтоксикації.
Синдром Кріглера-Наджара За відсутності спадковості (відсутність подібних хворих у сімї) шанс виникнення цього синдрому внаслідок виникнення мутації у гені UGT1A1 складає 1:500 така людина стає переносником дефектного гену
Синдром Кріглера-Наджара призводив до смерті у дитячому віці до появи такого методу лікування як фототерапія сьогодні такі пацієнти досягають зрілості, можуть мати власних дітей (необхідність генетичного скринінгу на наявність дефектного гену!)
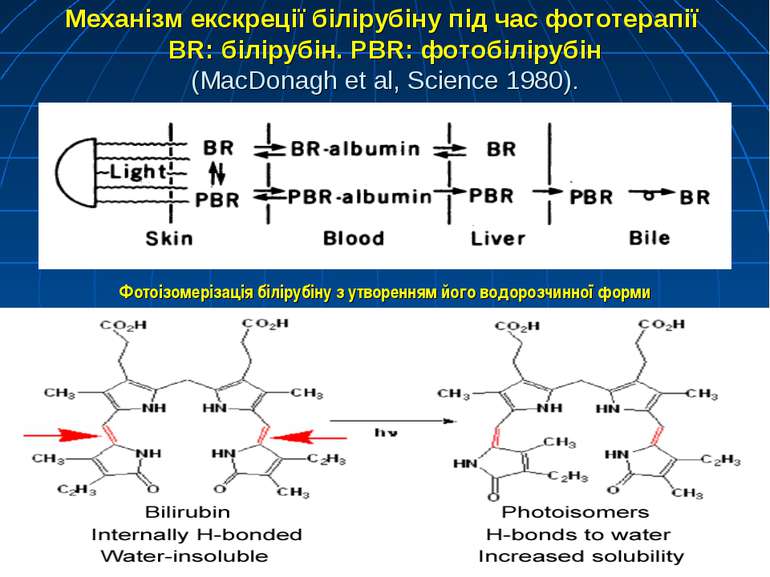
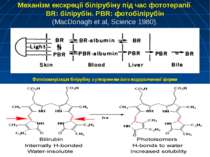
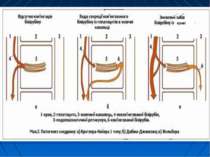
Механізм екскреції білірубіну під час фототерапії BR: білірубін. PBR: фотобілірубін (MacDonagh et al, Science 1980). Фотоізомерізація білірубіну з утворенням його водорозчинної форми
Синдром Жільбера (некон’югована гіпербілірубінемія) 3%-7% населення США, 10% - деякі народності Кавказу проявляється звичайно в юнацькому віці, у 20-30 років Успадковується за автосомно-домінантним типом синдром Жільбера може проявлятись після перенесеного вірусного гепатиту, інфекційного мононуклеозу, малярії, хімічного ураження печінки тощо - ці фактори провокують появу симптомів захворювання, яке до цього знаходилось у латентному стані
Синдром Жільбера Синдром Жільбера перебігає м’яко, не супроводжується нервовими і психічними розладами, ніколи не завершується ядерною жовтяницею. В період загострення хворі скаржаться на біль у животі, підвищену втомлювальність, нудоту, відригування, печію, гіркоту в роті тощо. Інтенсивність жовтяниці постійно змінюється. Жовтяниця може на деякий час зникати, виникати знову або наростати після фізичного навантаження, емоційного напруження, приймання алкоголю, деяких ліків, приєднання інших захворювань. Часто спостерігається лише легка іктеричність склер. У хворих на синдром Жільбера рівень непрямого білірубіну, звичайно, не перевищує 3-5 мг %, дуже рідко, особливо при загостренні хвороби, 10-15 мг %. Може порушуватися метаболізм лікарських засобів. Зокрема, встановлено зменшення біотрансформації бутаміду.
Синдром Дабіна-Джонсона проявляється в молодому віці Скарги: підвищена втомлюваність, біль у правому підребер’ї, нудоту, понижений апетит, відраза до жирної іжі і алкогольних напоїв, проноси і сверблячка шкіри хронічна або інтермітуюча нерізко виражена жовтяниця. Періодично - знебарвлення калу і темна сеча через білірубінурію. спадковий дефект локалізується в апараті Гольджі, периканалікулярній зоні чи біліарній мембрані гепатоцитів, що призводить до підвищення екскреторної функції печінки і регургітації білірубіну. У цитоплазмі гепатоцитів виявляється значна кількість перибіліарно розміщеного пігменту, що надає незвичайне забарвлення печінці (зелено-сіре, сіро-синє, чорно-зелене тощо). автосомно-домінантна природа успадкування
Синдром Ротора за своєю сутністю і клінічними проявами дуже нагадує попередній синдром. Патогенез: недостатня екскреція глюкуронідів білірубіну і його регургітація. Жовтяниця при синдромі Ротора виникає в дитячому віці. Вміст білірубіну в крові може перевищувати 10 мг %, у вигляді прямого і непрямого пігменту. Хворі скаржаться на підвищену втому, біль у правому підребер’ї, понижений апетит та ін. автосомно-домінантний характер успадкування дефектного гена.
Ефективність лікування фенобарбіталом, як індуктором глюкуронізації при спадкових жовтяницях, визначається рівнем дефіциту активності УДФГТ. При важкій формі синдрому Кріглера-Наджара індукція цього ферменту неможлива, тоді як фототерапія сприяє зменшенню неврологічних симптомів і гіпербілірубінемії. У хворих на легку форму синдрому Кріглера-Наджара, коли активність УДФГТ знижена лише частково, призначення фенобарбіталу призводить до тривалої ліквідації гіпербілірубінемії і зниження клінічних проявів. При гіпербілірубінемії вище 20 мг % терапія фенобарбіталом, як і поєднання його з фототерапією, часто неефективна. В таких випадках тільки замінна гемотрансфузія може поліпшити стан хворого.
У хворих на синдром Жільбера під впливом фенобарбіталу гіпербілірубінемія зникає, стан хворого поліпшується. Нерідко виникає тривала ремісія, особливо при поєднанні його з фототерапією, дієтотерапією, вітамінами, жовчогінними і седативними засобами. При синдромах Дабіна-Джонсона і Ротора інтенсивність жовтяниці зменшується під впливом жовчогінних препаратів: алохолу, холензиму, холосасу й ін. Ці засоби застосовують переважно в разі загострення захворювання, яке виникає при фізичному навантаженні, прийманні алкоголю, естрогенів, оральних протизаплідних засобів.
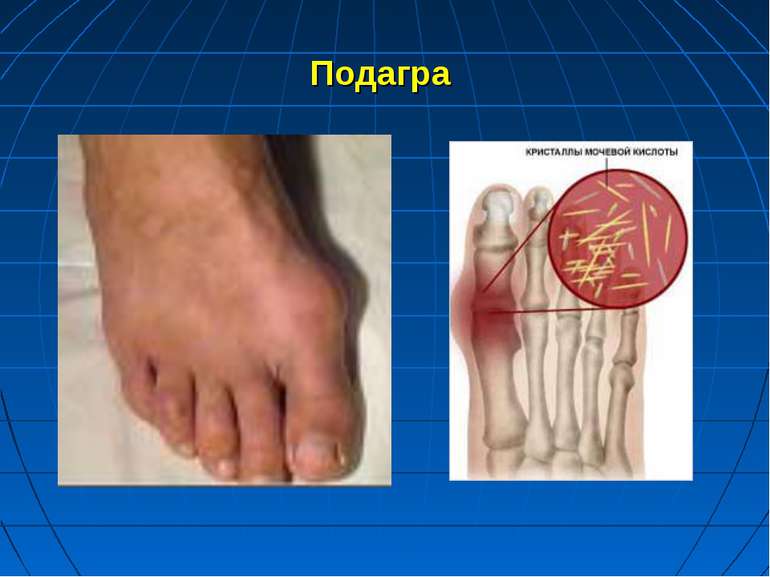
Первинна подагра розвивається в літніх людей через порушення обміну і екскреції пуринів і виражається прискоренням синтезу сечової кислоти та пониженням виведення її нирками Накопичення уратів у кістковій і хрящовій тканинах спричиняє появу запальних процесів, особливо в суглобах, і утворення сечокислих конкрементів у нирках Успадкується подагра за автосомно-домінантним типом з неповною пенетрантністю В осіб з генетично детермінованою схильністю до порушення обміну пуринів ознаки подагри легко виникають під впливом численних зовнішніх факторів, зокрема алкоголю і діуретичних засобів: дихлотіазиду і фуросеміду. Вживання алкогольних напоїв стимулює процес утворення лактату з пірувату, що негативно відбивається на екскреції сечової кислоти нирками. Це сприяє підвищенню вмісту її в організмі, провокує загострення хвороби. Дихлотіазид і фуросемід гальмують виведення сечової кислоти нирками, чим сприяють виникненню гіперурикемії.
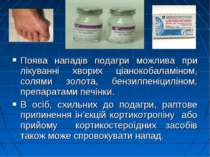
Поява нападів подагри можлива при лікуванні хворих ціанокобаламіном, солями золота, бензилпеніциліном, препаратами печінки. В осіб, схильних до подагри, раптове припинення ін’єкцій кортикотропіну або прийому кортикостероїдних засобів також може спровокувати напад.
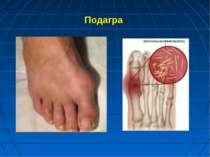
Подагра Напад подагри виникає раптово або після продромального періоду у вигляді психічного пригнічення, кишкових розладів, переважно вночі. Виникає різкий біль у ділянці одного чи декількох суглобів. Вони набрякають, шкіра над ними стає гіперемійованою, напруженою. З’являється сильний озноб. Температура нерідко перевищує 41 о С. Профілактика передбачає виключення приймання дихлотіазиду і фуросеміду, тим більше вживання алкогольних напоїв. Неприпустима також раптова відміна лікування кортикотропіном і кортикостероїдними засобами.
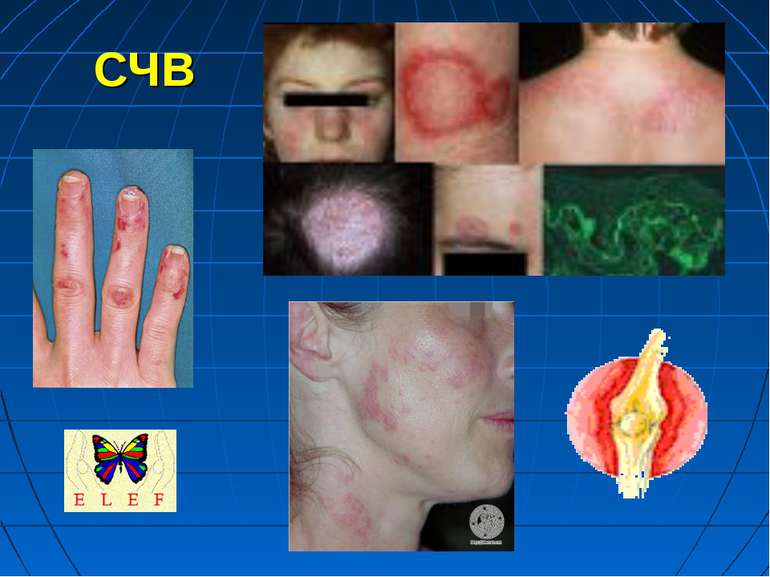
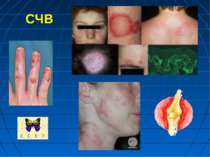
Системний червоний вовчак - СЧВ спадково детерміноване захворювання виникає або загострюється під впливом деяких несприятливих зовнішніх і внутрішніх факторів, зокрема при прийомі лікарських засобів: антигіпертензивні (апресин, резерпін, метилдофа), протиаритмічні (новокаїнамід, хінідин), протиепілептичні (дифенін, гексамідин, карбамазепін, етосуксимід, триметин, фенобарбітал), хіміотерапевтичні (бензилпеніцилін, стрептоміцин, тетрациклін, сульфаніламіди, похідні ГІНК) засоби, бутадіон, пеніциламін, алопуринол, клофібрат, метил- і пропілтіоурацил, кортикостероїди, оральні протизаплідні препарати
Під їх впливом зростають клінічні прояви системного червоного вовчака. З’являється тривала лихоманка, артрити і артралгії, висипка і феномен “метелика” на обличчі, інколи ознаки ендо- і перикардиту, хронічної пневмонії, гломерулонефриту, спленомегалія, збільшення лімфатичних вузлів, гіпохромна анемія тощо. При відміні цих препаратів далеко не завжди відмічається затихання патологічного процесу. Захворювання може прогресувати аж до смерті. Тому при загостренні системного червоного вовчака необхідно провести енергійне лікування кортикостероїдами й іншими засобами.
СЧВ лікарські препарати можуть не тільки загострювати ідіопатичний системний червоний вовчак, але й спричиняти розвиток лікарського системного червоного вовчака. На відміну від ідіопатичного вовчака, останній перебігає менш тяжко і після відміни підозрюваного лікарського засобу, як правило, зникає. При лікарському системному червоному вовчаку нирки вражаються дуже рідко.
СЧВ У світовій літературі описано декілька сот випадків синдрому червоного вовчака, який виникав через тривале лікування лікарськими засобами. Причому близько 2/3 з них були індуковані апресином і новокаїнамідом. Нерідко таке ускладнення викликає хінін, протиепілептичні засоби, аміназин, ізоніазид, пеніциламін. Переважно лікарський системний червоний вовчак виникає у процесі лікування хворих новокаїнамідом. Сумарна доза, яка необхідна для індукування цього захворювання новокаїнамідом, варіює від 14 до 3600 г. Від початку лікування до появи ознак цього захворювання проходить від 3 міс до 2 років безперервного приймання новокаїнаміду, в середньому 6 міс. В окремих випадках цей строк скорочується до 2 тижнів або продовжується до 4,5 років і більше.
СЧВ-синдром На другому місці за частотою спричинення лікарського системного червоного вовчака знаходиться апресин. Це захворювання звичайно виникає не менш ніж через 3 місяці, інколи декілька років, щоденного приймання цього препарату в дозі 0,4 г. При його відміні прояви хвороби поступово зникають аж до повного одужання. Пришвидшити одужання можливо шляхом приймання кортикостероїдних засобів.
Схожі презентації
Категорії