Презентація на тему:
Прості речовини кисень і залізо
Завантажити презентацію
Прості речовини кисень і залізо
Завантажити презентаціюПрезентація по слайдам:
Узагальнення й систематизація вивченого матеріалу 1) На які групи можна поділити всі речовини? 2) Які прості речовини вивчили в 7 класі? 3) А на які групи можна поділити прості речовини? 4) За якою ознакою?
Групова робота Група 1 Оксиген Хімічний символ — __________ Відносна атомна маса Ar (О)_________ Будова атома: +)) Число протонів _________ р Число електронів ________ e− Число нейтронів ________ n Валентність _________
Група 2 Кисень Тип речовини ____________ Має ____________________ будову. Хімічна формула _________________ Відносна молекулярна маса Mr (O)____________ Фізичні властивості Розчинність у воді ________ Агрегатний стан _________ Колір __________ Запах __________ Смак __________
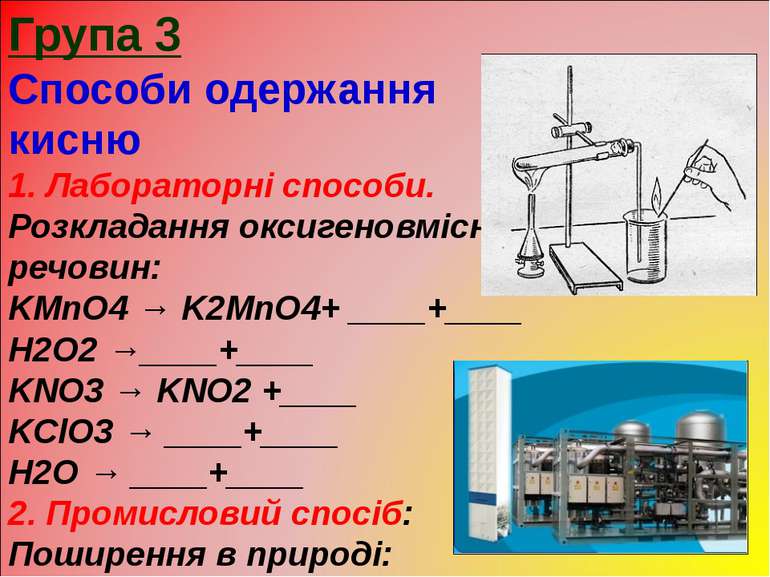
Група 3 Способи одержання кисню 1. Лабораторні способи. Розкладання оксигеновмісних речовин: KMnO4 → K2MnO4+ ____+____ H2O2 →____+____ KNO3 → KNO2 +____ KClO3 → ____+____ H2O → ____+____ 2. Промисловий спосіб: Поширення в природі:
Група 4 Хімічні властивості кисню Взаємодія з неМе C+O2→ S +O2→ P +O2→ N2+O2→ Взаємодія з Ме Mg +O2 → Li +O2 → Al +O2 → Cu +O2 → Окиснення — це реакція взаємодії ____________ Горіння — це реакція _______, що супроводжується виділенням______ і______. Оксиди — складні речовини, що складаються з ________ елементів, один з яких ______.
Група 5 Ферум Хімічний символ — _____________________ Відносна атомна маса Ar (Fe)____________ Будова атома: +)))) Число протонів (р) Число електронів (e−) Число нейтронів (n) Валентність
Група 6 Залізо Тип речовини ______________ Має ________________ будову. Хімічна формула _____________ Фізичні властивості Розчинність у воді ____________ Агрегатний стан _____________ Колір ___________ Запах __________ Смак __________ Специфічні властивості _______________
Група 7 Способи одержання заліза 1. Доменне виробництво чавуну 2. Відновлення заліза зі сполук Fe2O3+ H2 → Fe3O4+CO → Fe2O3+Al → Fe2O3+C → Поширення в природі: _________________
Група 8 Хімічні властивості заліза 1. Взаємодія з неметалами Fe+O2→ Fe+S→ Fe+Cl2→ 2. Взаємодія з кислотами Fe+HCl→ Корозія — це _____________. Способи захисту від корозії: _______________.
Домашнє завдання Повторити матеріал про прості речовини — кисень і залізо. Творче завдання. Навести свої приклади хімічних властивостей кисню й заліза (по два-три рівняння реакцій).
Схожі презентації
Категорії