Презентація на тему:
ВСМОКТУВАННЯ ЛІКАРСЬКИХ РЕЧОВИН В ОРГАНІЗМІ
Завантажити презентацію
ВСМОКТУВАННЯ ЛІКАРСЬКИХ РЕЧОВИН В ОРГАНІЗМІ
Завантажити презентаціюПрезентація по слайдам:
Всмоктування – процес поступлення лікарських речовин із місця їх введення в кров. Всмоктування залежить від шляху введення, лікарської форми, розчинності лікарської речовини у ліпідах та швидкості кровотоку в місці введення. Основними показниками, що характеризують всмоктування є: повнота всмоктування – кількість (у %) речовини, яка всмокталась; час досягнення максимальної концентрації (Тmax) – швидкість всмоктування ЛЗ і швидкість настання терапевтичного ефекту; константа швидкості абсорбції (Ка) – швидкість поступлення ЛЗ в кров із місця введення; період напівабсорбції (Т1/2а) – час, необхідний для поступлення в кровоносне русло половини дози препарату із місця введення.
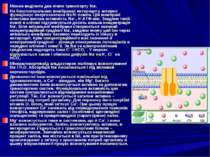
Після вивільнення із лікарської форми лікарська речовина у вигляді діючої молекулярної субстанції вступає у біофазу. При всіх шляхах введення ЛЗ обов’язково повинен проникнути через різноманітні біологічні мембрани епітеліальних чи ендотеліальних клітин, або ж клітин-мішеней шляхом пасивної дифузії, полегшеної дифузії, активного транспорту чи ендоцитозу. Незважаючи на загальні закономірності цих процесів є ряд особливостей, характерних для всмоктування ліків в кров при ентеральному (пероральному, сублінгвальному і ректальному) та парентеральному позасудинному (внутрім’язовому, підшкірному, інгаляційному, місцевому) шляхах введення ЛЗ.
Всмоктування у травному каналі Під всмоктуванням у травному каналі розуміють перехід речовин із порожнин цього каналу у внутрішнє середовище організму, тобто в кров або лімфу. Роль відділів травного каналу в процесі всмоктування різна. Слизова оболонка ротової порожнини має інтенсивне кровопостачання. Нею всмоктуються деякі лікарські препарати (органічні нітрати, валідол, ніфедипін тощо), котрі проникають через вени голови, які впадають у яремну вену, в системний кровоток, обминаючи печінку і вже через кілька хвилин викликають ефект. Важливим є те, що ЛЗ, які всмоктуються у слизовій оболонці рота не зазнають пресистемної елімінації і не підлягають агресивному впливу шлункового соку.
У шлунку всмоктуються невеликі нейтральні молекули (спирт, вода) і деякі інші ЛЗ, які мають кислотну природу. Це пов’язано з тим, що шлунковий сік людини має рН в межах 1-3. При такому рН лікарські засоби, які є слабкими органічними основами будуть іонізувати і їх всмоктування відбуватись не буде, оскільки іонізовані речовини майже не проникають через біологічні мембрани. І навпаки, слабкі органічні кислоти у порожнині шлунка будуть знаходитись в неіонізованому стані і добре всмоктуються слизовою оболонкою шлунка. Так, кислота ацетилсаліцилова практично повністю всмоктується в шлунку, оскільки перебуває в неіонізованому стані і добре розчиняється в ліпідах. Кисле середовище шлунка, крім впливу на іонізацію ЛЗ, може викликати і їх хімічне руйнування (наприклад бензилпеніцилін, еритроміцин тощо), тому ці засоби або вводяться іншими шляхами, або ж для їх введення застосовують спеціальні лікарські форми, які захищають їх від прямого впливу шлункового вмісту. Необхідно також відзначити, що ряд ЛЗ можуть приводити до руйнування слизового бар’єру, який захищає слизову оболонку шлунка від руйнівної дії соляної кислоти, чим викликати виразкування слизової. До таких засобів відносяться кислота ацетилсаліцилова, жовчні кислоти, глюкокортикостероїди, високі концентрації етилового спирту.
У товстій кишці всмоктується вода і завершується всмоктування невеликої кількості продуктів гідролізу вуглеводів, білків та жирів. Завдяки цьому можуть всмоктуватись компоненти, які входять до складу живильних клізм (глюкоза, вітаміни, вода та ін.). Транспортуючись із прямої кишки, значна частина лікарської речовини надходить в кров не через ворітну вену, а системою нижньої порожнистої вени, минаючи печінку, що дозволяє уникнути пресистемного метаболізму та безпосередньго впливу на слизову шлунка.
Всмоктування відбувається в основному в тонкій кишці, яка має довжину близько 3 м (дванадцятипала – приблизно 30 см, порожня – 120 см, клубова – 130 см). Переважно речовини всмоктуються в порожній кишці, а клубова кишка є резервною зоною. Завдяки складкам, ворсинкам і мікроворсинкам загальна поверхня, на якій відбувається всмоктування, значно більша (в 600 разів) від поверхні тонкої кишки і становить близько 200 м2.
Структурною основою всмоктування є ворсинка, вкрита ентероцитами, мембрана яких забезпечує заключний мембранний гідроліз поживних речовин та початкові етапи всмоктування. Кожна ворсинка має артеріолу, яка розгалужується на капіляри, вену, лімфатичну судину та тладком'язові клітини (завдяки ним ворсинки періодично скорочуються). Протягом доби всмоктується кілька сотень грамів вуглеводів, близько 100 г жиру, 50-100 г білків, 7-8 л води, до 100 г різних електролітів. Але потенційні можливості всмоктування значно більші: може всмоктуватись кілька кілограмів вуглеводів, до 1 кг жиру, 0,7 кг білків, близько 20 л води. Всмоктування відбувається завдяки пасивному транспорту речовин без затрат енергії (дифузія, осмос, фільтрація) і активному – з її витратами. Звичайно домінує один або кілька механізмів всмоктування.
Велика роль у процесах всмоктування належить інтенсивності кровотоку. Якщо до їди через слизову оболонку тонкої кишки протікає близько 200 мл крові за 1 хв, то в процесі травлення кровотік зростає до 500-600 мл за 1 хв. Завдяки цьому ентероцити забезпечуються енергією для активних процесів всмоктування, постійно підтримується градієнт кожної речовини між вмістом ворсинок і кров'ю. Одні речовини всмоктуються активно в ентероцит, а потім пасивно – в міжклітинну рідину і кров, інші проходять по проміжках між ентероцитами. Певне значення для переходу речовин через ентероцит має їх розчинність у ліпідах мембран.
У порожнині тонкої кишки рН близька до нейтрального (~8), тому всмоктування кислотних і лужних сполук залежить від їх рКа, розчинності у воді і ступеня подрібнення. Велика поверхня епітелію проксимальної частини тонкої кишки забезпечує всмоктування багатьох лікарських препаратів. Всмоктування ліків у здухвинній кишці і товстому кишечнику зазвичай менш ефективне, у першому випадку – із-за відносно невеликого, а в другому – із-за значного зменшення площі кишкового епітелію. Внаслідок відмінностей між рН всередині клітин і концентрацією іонів у порожнині травного тракту можлива навіть дифузія лікарських речовин із клітин в бік травного тракту. Так, слабкі основи, які вводились парентерально, можуть з’явитись у кишковому вмісті, в той час як слабколужні речовини, які вводились перорально, у лужному середовищі тонкої кишки існують у вигляді неіонізованих сполук і добре всмоктуються.
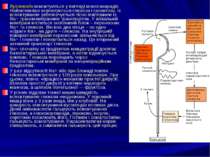
Існують наступні особливості всмоктування речовин різної хімічної природи у травному тракті. Вода і мінеральні солі. До органів травлення щодоби надходить близько 10 л води: 2- З л з їжею, від 6 до 7 л – з травними соками. З калом же виділяється лише 100-150 мл її. Основна маса води всмоктується у тонкій кишці. Незначна кількість води всмоктується у шлунку та товстій кишці. Вода всмоктується переважно у верхніх відділах тонкої кишки завдяки осмосу, якщо осмотичний тиск хімусу нижчий, ніж плазми крові. Вода легко проникає через бар'єр за осмотичним градієнтом. А якщо у дванадцятипалій кишці міститься гіперосмотичний хімус, то вода з крові надходить сюди. Всмоктування вуглеводів, амінокислот, а особливо мінеральних солей сприяє одночасному всмоктуванню води. Разом із водою всмоктуються й водорозчинні вітаміни. Тому всі чинники, які порушують процес всмоктування харчових речовин, утруднюють і водний обмін організму. Вирішальна роль у перенесенні води через мембрани і міжклітинні проміжки належить іонам Na+ і С1¯.
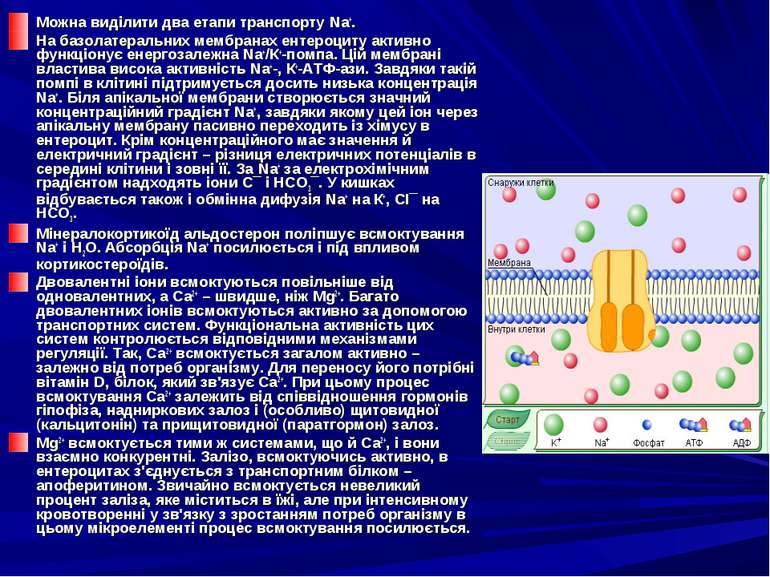
Можна виділити два етапи транспорту Na+. На базолатеральних мембранах ентероциту активно функціонує енергозалежна Na+/К+-помпа. Цій мембрані властива висока активність Na+-, К+-АТФ-ази. Завдяки такій помпі в клітині підтримується досить низька концентрація Na+. Біля апікальної мембрани створюється значний концентраційний градієнт Na+, завдяки якому цей іон через апікальну мембрану пасивно переходить із хімусу в ентероцит. Крім концентраційного має значення й електричний градієнт – різниця електричних потенціалів в середині клітини і зовні її. За Na+ за електрохімічним градієнтом надходять іони С¯ і НСО3¯. У кишках відбувається також і обмінна дифузія Na+ на К+, СІ¯ на НСО3. Мінералокортикоїд альдостерон поліпшує всмоктування Na+ і Н2О. Абсорбція Na+ посилюється і під впливом кортикостероїдів. Двовалентні іони всмоктуються повільніше від одновалентних, а Са2+ – швидше, ніж Мg2+. Багато двовалентних іонів всмоктуються активно за допомогою транспортних систем. Функціональна активність цих систем контролюється відповідними механізмами регуляції. Так, Са2+ всмоктується загалом активно – залежно від потреб організму. Для переносу його потрібні вітамін D, білок, який зв'язує Са2+. При цьому процес всмоктування Са2+ залежить від співвідношення гормонів гіпофіза, надниркових залоз і (особливо) щитовидної (кальцитонін) та прищитовидної (паратгормон) залоз. Мg2+ всмоктується тими ж системами, що й Са2+, і вони взаємно конкурентні. Залізо, всмоктуючись активно, в ентероцитах з'єднується з транспортним білком – апоферитином. Звичайно всмоктується невеликий процент заліза, яке міститься в їжі, але при інтенсивному кровотворенні у зв'язку з зростанням потреб організму в цьому мікроелементі процес всмоктування посилюється.
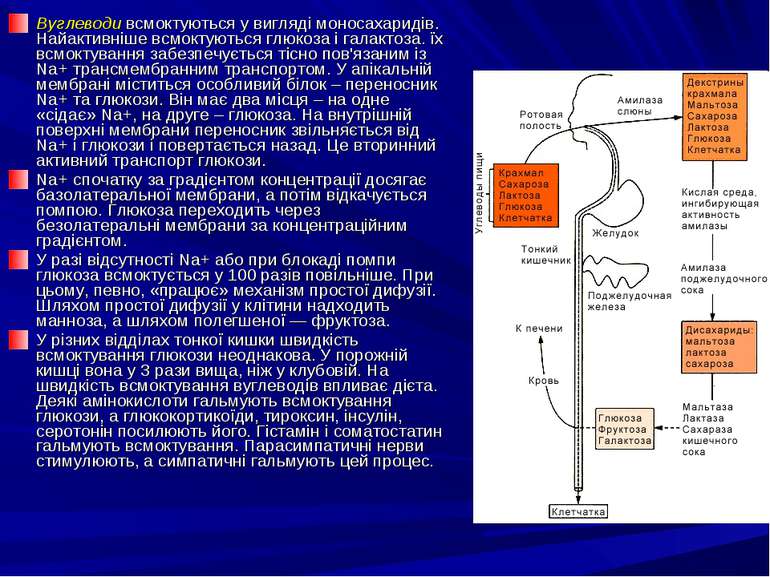
Вуглеводи всмоктуються у вигляді моносахаридів. Найактивніше всмоктуються глюкоза і галактоза. їх всмоктування забезпечується тісно пов'язаним із Na+ трансмембранним транспортом. У апікальній мембрані міститься особливий білок – переносник Na+ та глюкози. Він має два місця – на одне «сідає» Na+, на друге – глюкоза. На внутрішній поверхні мембрани переносник звільняється від Na+ і глюкози і повертається назад. Це вторинний активний транспорт глюкози. Na+ спочатку за градієнтом концентрації досягає базолатеральної мембрани, а потім відкачується помпою. Глюкоза переходить через безолатеральні мембрани за концентраційним градієнтом. У разі відсутності Na+ або при блокаді помпи глюкоза всмоктується у 100 разів повільніше. При цьому, певно, «працює» механізм простої дифузії. Шляхом простої дифузії у клітини надходить манноза, а шляхом полегшеної — фруктоза. У різних відділах тонкої кишки швидкість всмоктування глюкози неоднакова. У порожній кишці вона у 3 рази вища, ніж у клубовій. На швидкість всмоктування вуглеводів впливає дієта. Деякі амінокислоти гальмують всмоктування глюкози, а глюкокортикоїди, тироксин, інсулін, серотонін посилюють його. Гістамін і соматостатин гальмують всмоктування. Парасимпатичні нерви стимулюють, а симпатичні гальмують цей процес.
Білки. Продукти гідролізу білків всмоктуються у вигляді вільних амінокислот, дипептидів та трипептидів. Амінокислоти й олігопептиди всмоктуються головним чином шляхом зв'язаного з Na+ вторинного активного транспорту. Кількість амінокислот, що всмоктується шляхом простої дифузії, незначна. Швидкість всмоктування різних амінокислот різна. Так, найшвидше всмоктуються аргінін, метіонін, лейцин, а дещо повільніше – аланін, серин, глутамінова кислота. L-форми амінокислот всмоктуються активніше, ніж D-форми. Через базальну та латеральну мембрани амінокислоти за градієнтом концентрації переходять у міжклітинну рідину, а потім у кров. Через слизову оболонку тонкої кишки всмоктується незначна кількість деяких невеликих пептидів. Це особливо виражено у новонароджених, коли ще не досить активні протеолітичні ферменти шлунка та підшлункової залози. Всмоктування відбувається шляхом піноцитозу. Таким чином у організм дитини з молоком матері надходять антитіла, що забезпечують імунні реакції.
Жири всмоктуються в проксимальних відділах тонкої кишки. Продукти гідролізу жиру – жирні кислоти, моногліцерини, фосфоліпіди, холестерин – утворюють разом із солями жовчних кислот у порожнині кишки міцели діаметром близько 3 нм (мал.). Гідрофобне ядро міцели оточене зовні гідрофільною оболонкою із солей жовчних кислот. Коли міцела контактує з апікальною мембраною ентероцита, солі жовчних кислот залишають міцелу, виконавши транспортну роль. Без жовчних кислот всмоктується лише 50—60 % жирів. Інші складові частини міцели шляхом дифузії проникають у ентероцит, і в його ендоплазматичній сітці та пластинчастому комплексі (апараті Гольджі) відбувається синтез нових тригліцеринів, притаманних даному організму. Тут утворюються хіломікрони – дуже дрібні структури, до складу яких, крім тригліцеринів, входять фосфоліпіди, холестерин та інші ліпіди. Хіломікрони вкриті ззовні ліпопротеїновою оболонкою. З ентероцитів хіломікрони проникають у лімфатичні судини шляхом піноцитозу. Вони проходять між клітинами. Таким чином, у лімфу потрапляє 80-90 % жиру, що всмоктався. В хіломікронах виявляють довголанцюгові жирні кислоти. Через 3-4 год після вживання жирної їжі, коли лімфа починає надходити в кров, плазма крові завдяки присутності хіломікронів стає подібною до молока. Секретин, гормони кори надниркових, щитовидної залоз, гіпофіза посилюють всмоктування жиру. Парасимпатичні нерви стимулюють, а симпатичні гальмують цей процес.
Вітаміни. Всмоктування жиророзчинних вітамінів (А, D, Е, К) зв'язане із всмоктуванням жирів. Механізми всмоктування водорозчинних вітамінів різні. Вітамін С і рибофлавін переносяться шляхом дифузії. Фолієва кислола, ймовірно, всмоктується в голодній кишці у кон’югованому вигляді. Вітамін В12 (ціанокобаламін) всмоктується за участю специфічного переносника – гастромукопротеїна (внутрішній фактор Касла).
Фактори, що впливають на всмоктування у травному тракті На ступінь та швидкість всмоктування ЛЗ в травному тракті впливає ряд факторів, які можна розділити на фармацевтичні, фізико-хімічні та фізіологічні: Фармацевтичні особливості лікарських засобів і лікарських форм (швидкість розпаду, час розчинення, наявність допоміжних речовин, стабільність лікарських засобів в травному тракті тощо). Традиційні лікарські форми можна розмістити в порядку зниження швидкості абсорбції наступним чином: розчини > суспензії > капсули > прості таблетки > таблетки в оболонці > лікарські форми із сповільненим вивільненням лікарського засобу.
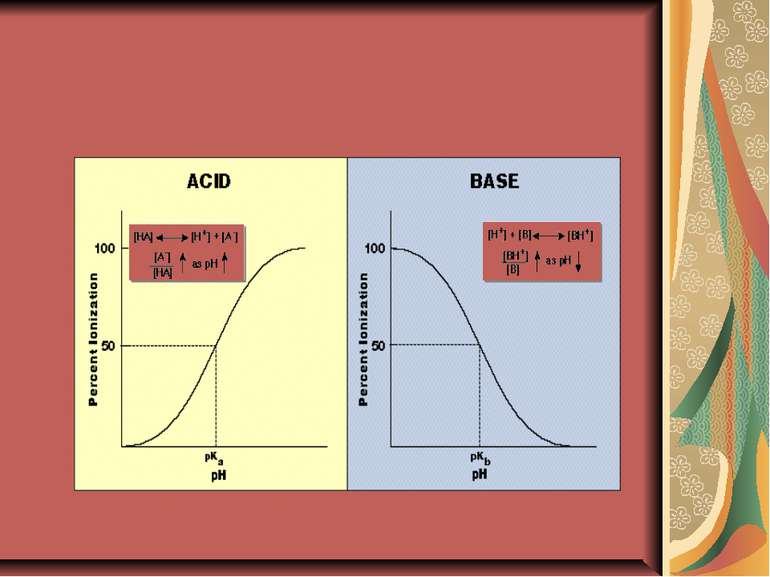
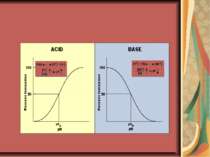
Фізико-хімічні властивості ЛЗ. Для здійснення абсорбції ЛЗ повинен бути в деякій мірі ліофільним (для того, щоб проникнути через мембрану, яка містить велику кількість ліпідів) і в той же час гідрофільним (для того щоб проникнути з мембрани у водну фазу). Більшість препаратів відносяться до слабких кислот чи основ. При цьому неіонізовані форми, будучи ліофільними, здатні легко проникати через мембрану. Дисоціація слабких кислот описується наступними співвідношеннями: НА ↔ Н+ + А¯, де Ка – константа дисоціації слабких кислот; [НА]- концентрація недисоційованої речовини; [Н+]- концентрація іонів водню, [А¯] концентрація аніонів лікарської речовини. Логарифмування данного виразу приводить до рівняння Гендерсона-Гессельбаха: де рКа= – lg(Ka), тобто логарифм константи дисоціації сполуки, який чисельно дорівнює значенню рН при якому дисоціація даної сполуки становить 50%. Аналогічне рівняння можна вивести і для слабких основ: де Kw – іонний добуток води (рКw=14), [ВОН] – концентрація недисоційованої речовини, [В+] – концентрація катіонів лікарської речовини, Kb – константа дисоціації основи. З наведених рівнянь видно, що із збільшенням значення рН середовища дисоціація кислот зростає, а основ – зменшується, що впливає на їх всмоктуваня. Так, аспірин (рКа=3) буде у більшій мірі всмоктуватись у шлунку (рН~2), ніж в кишечнику (рН~7), а для хініну (рКа=8,4) справедливим є зворотнє відношення. В той же час не варто забувати, що сумарна площа епітелію кишечника значно перевищує площу шлункового епітелію.
Важливим фізико-хімічним показником, який зумовлює всмоктування препарату, є його ліпофільність. Мірою ліпофільності (Р) сполуки є коефіцієнт розподілу між органічним розчинником (зазвичай октанолом) і водою. Величина lg(Р) коливається в діапазоні від –6 до +6 для високогідрофільних і високоліпофільних сполук відповідно. Лікарська форма у ШКТ зазнає дезінтеграції і розчинення. Препарат у місці всмоктування повинен перебувати у водному розчині, у зв’язку з чим швидкість розчинення ЛЗ є одним з лімітуючи факторів абсорбції, особливо для слабо розчинних сполук. Серед факторів, що впливають на розчинність, важливе значення має ступінь диспергування лікарської субстанції. Розмір мікрочасточок зворотно пропорційний загальній поверхні розчиненої речовини: наприклад, куб із гранню в 1 см має площу 6 см2, однак якщо цей куб розділити на маленькі кубики з гранню 0,1 см, то їх сумарна площа складе вже 60 см2, що значно покращує швидкість всмоктування. Солі слабких кислот і основ мають значно кращу розчинність у водній фазі, ніж їх вільні аналоги. Таким сином, прийом препарату у вигляді солі приводить до збільшення розчинності і відповідно ступеня абсорбції речовини.
Фізіологічні фактори: – моторика шлунково-кишкового тракту, від якої залежить тривалість перебування ЛЗ в його відділах. Наприклад, у хворих на мігрень моторика шлунка сповільнена, його спорожнення відбувається пізніше, ніж в нормі. В результаті при застосуванні НПЗЗ у цих хворих знижується абсорбція, а ефекти сповільнюються в часі. На моторику ШКТ впливають і цілий ряд лікарських засобів та деякі інші фактори)
Вплив різних факторів на швидкість спорожнювання шлунка № Фактор Підвищення Зниження 1. Лікарські засоби - антихолінергічні препарати + - наркотичні анальгетики + - трициклічні антидепресанти + - наркотики + - етанол + - метоклопрамід + + - препарати жовчних кислот + - бікарбонат натрію + 2. Захворювання - виразкова хвороба шлунка + - виразкова хвороба шлунка дванадцятипалої кишки + - стеноз воротаря + - інфаркт міокарда + - травма, больовий синдром + - мігрень + 3. Характер харчування - великий об’єм їжі спочатку + потім + - їжа з великою кількістю жирів +
Їжа може змінювати фармакокінетичні параметри медикаментів – розчинність, всмоктування, метаболізм, виведення. Зміни всмоктування ЛЗ під впливом їжі можуть бути пов’язані з варіаціями шлункової секреції і рН шлункового вмісту, а також з різним часом перебування їжі в шлунку. Приймання їжі викликає підвищення рН шлункового вмісту у 3 рази і більше в залежності від виду їжі. В процесі приймання їжі діюча субстанція деяких ЛЗ в кислому середовищі шлунка може руйнуватись не дивлячись навіть на наявність кислотостійкої оболонки. Тому прийом ліків, які випускають навіть у кислотостійкій оболонці необхідно здійснювати натще або перед їдою. Як відомо, тривалість перебування харчової грудки в шлунку може становити від 1 до 4 годин. ЛЗ, який входить в склад харчової грудки (якщо його приймати під час їди) буде поступати в кишечник значно пізніше, ніж при вживанні натще (в цьому випадку ЛЗ може потрапити до кишечника вже через 10-13 хв). В результаті зниження інтенсивності всмоктування деякі ліки можуть утворювати комплекси або хелати – тетрацикліни та препарати заліза з катіонами кальцію, що містяться у молочних продуктах, що є причиною сповільнення їх всмоктування. Можливі також взаємодії між бісфосфонатами (етифронат натрію) і кальцієм, β-блокатором атенололом і кальцієм, лінкоміцмном чи кліндаміцином і циклом атом натрію, магнієм і фосфатами, парацетамолом і пептинами, кальцієм, магнієм і фітатами. Окрім різноманітних хімічних взаємодій з ЛЗ їжа може адсорбувати їх, покривати слизом, погіршуючи таким чином всмоктування в кров. Можлива також конкуренція харчових інгредієнтів з ЛЗ за транспортні механізми, особливо, якщо вони всмоктуються за допомогою активного транспорту. Наприклад, конкуренція виникає між амінокислотами і ЛЗ з подібною хімічною структурою (леводопа, α-метилдофа, 5-фторурацил). Ці ліки доцільніше приймати між прийомами їжі.
Проте, прийом їжі одночасно з ЛЗ може сприяти і збільшенню швидкості його всмоктування, особливо в тих випадках, коли розчинність препарату підвищується під час тривалого перебування в шлунку. ЛЗ з великою молекулярною масою (гризеофульвін, нітрофурантоїн, спіронолактон) посилено всмоктуються при їх вживанні разом з їжею, оскільки покращується їх розчинність внаслідок перемішування в харчовій грудці і наявністю шлункового соку, який змочує рівномірно всі частини. Жиророзчинні речовини (сульфаніламіди, гризеофульвін, фенітоїн, карбамазепін, кетоконазол) швидко всмоктуються, особливо якщо їжа місить жир. Деякі ЛЗ, особливо при тривалому застосуванні, можуть порушувати всмоктування деяких інгредієнтів їжі і викликати різні патологічні стани. Так, гормональні оральні контрацептиви порушують всмоктування Фотієвої і аскорбінової кислот, рибофлавіну, антикоагулянти непрямої дії пригнічують всмоктування вітаміну К, проносні засоби – всмоктування жиророзчинних вітамінів тощо.
Вплив їжі на всмоктування лікарських речовин Всмоктування Лікарські препарати Зниження Ацетилсаліцилова кислота, бензилпеніцилін, ізоніазид, леводопа, рифампіцин, тетрацикліни, цефалоксин Підвищення Анаприлін, апресин, дихлотіазид, карбамазепін, нітрофурантоїн, спіронолактон, хлорохін Уповільнення Дигоксин, ізосорбіду мононітрат, парацетамол, сульфазин, фенобарбітал, фенацетин, фуросемід, еритроміцин Без змін Метронідазол, нітрозепам, оксазепам, преднізолон, теофілін, феноксиметилпеніцилін, хлорпропамід
Вік. Процес всмоктування у значній мірі залежить від віку. Всмоктування ліків із ШКТ дитини тісно зв’язаний зі ступенем морфологічних і функціональних змін травного тракту. Найбільш виражені зміни функцій ШКТ спостерігаються протягом перших тижнів життя дитини. Безпосередньо в немовляти рН середовища в шлунку складає 6-8, але зменшується до 1-3 через кілька годин після народження. Секреція кислот у шлунку поступово знижується протягом перших 10 днів життя. Величина рН тісно пов'язана з розвитком слизової шлунка і з процесом секреції кислот, яких у немовляти менше, ніж у дітей, що завершили постнатальний розвиток. У дітей старше 3 років дані показники відповідають дорослим людям. Час спорожнювання шлунка більш тривалий в немовлят, а перистальтика кишечника нерегулярна і залежить від виду їжі. Протягом неонатального періоду активність механізмів, що регулюють транспорт лікарських препаратів через стінку кишечнику знижена. В міру збільшення віку збільшується активність механізмів всмоктування і подальша морфологічна диференціація. Тому в дітей біодоступність ліків завжди нижча, ніж у дорослих, в основному за рахунок швидкості всмоктування в ШКТ. У зв'язку з цим ризиковано призначати новонародженим дітям препарати для приймання усередину, якщо немає можливості контролювати оптимальний рівень препаратів у крові чи відсутня можливість у клінічних умовах швидко оцінити фармакологічний ефект. У людей похилого віку знижується функція шлунка і кишечника, знижується тонус різних відділів ШКТ, спостерігаються атрофічні процеси в м'язах шлунка і черевній стінці, що призводить до уповільнення всмоктування лікарських речовин з кишечника. Швидкість всмоктування препаратів у ШКТ людей старших вікових груп знижена в зв'язку з атрофічними процесами в стінці шлунка, зменшенням системного кровообігу, судинними змінами, порушеннями кровопостачання стінки шлунка. У літньому віці виникають трофічні порушення секреторного апарату, м'язових волокон, знижується секреторна функція. У людей старечого віку наступає гіпохлоргідрія (знижений вміст соляної кислоти в шлунковому соку) і ахілія шлунка (відсутність у шлунковому соку вільної соляної кислоти і ферментів) спостерігаються майже в 50% випадків.
Фізіологічні особливості різних відділів ШКТ і регіональне всмоктування лікарських засобів Відділ рН вмісту Мембрана Кровообіг Площа поверхні Час проходження Обхід печінки Ротова порожнина Біля 7 Тонка Хороший, швидка абсорбція при малих дозах Мала Короткий Так Стравохід 5-6 Дуже товста, всмоктування відсутнє – Мала Короткий – Шлунок 1-3, декомпозиція лікарських форм, де іонізація слабких кислот Нормальна Хороший Мала 30-40 хв, незначна абсорбція Ні Дванадцятипала кишка 6-6,5, наявність жовчних кислот, сурфактантні явища Нормальна Хороший Дуже велика Дуже короткий, біля 6 хв Ні Тонкий кишечник 7-8 Нормальна Хороший Дуже велика, довжина 2,5-3,5 м, поверхня 80 см2/см Біля 3 год Ні Товстий кишечник 5,5-7 Нормальна Хороший Не дуже велика, довжина 1-1,3 м Тривалий, до 24 год Так, в прямій і частково здухвинній кишці
Всмоктування при парентеральному позасудинному введенні Нашкірне введення. Деякі речовини мають високу ліпофільність і можуть всмоктуватись та проявляти системну дію при нанесенні їх на шкіру (наприклад, нітрогліцерин). Трансдермальні лікарські форми отримують все більше поширення, оскільки з їх допомогою вдається тривалий час підтримувати стаціонарну концентрацію речовин у плазмі крові. При підшкірному введенні ЛЗ розчиняються у тканинній рідині, всмоктуються у капіляри і лімфатичні судини дерми/ Підшкірно вводять водні та олійні розчини ліків (вітаміни, камфора), суспензії (пролонговані форми інсуліну). У підшкірній клітковині утворюється депо препарату. Лікувальна дія при цьому розпочинається швидше, ніж при пероральному, але повільніше, через 10-30 хв., ніж при внутрішньом’язовому введенні. При шокових, колаптоїдних станах всмоктування ліків з підшкірної клітковини різко сповільнюється.
При внутрім’язовому введенні водних розчинів гідрофільних препаратів спостерігається їх швидке всмоктування в кров (через 10-15 хв.). ЛЗ проникає через перимізій, епімізій, плазмолему ендотеліальних клітин капілярів (рис. ) і розповсюджується по кровоносних судинах ендомізію сусідніх м’язевих волокон, м’язових пучків і цілих м’язів з допомогою загальновідомих механізмів клітинного транспорту – пасивної і полегшеної дифузії, активного транспорту і піноцитозу. Із олійних розчинів ліпофільні препарати всмоктуються повільно, утворюючи в м’язах депо. Відомі особливості кінетики ЛЗ при введенні їх у різні ділянки м’язової тканини. Швидше відбувається всмоктування при введенні препарату у м’язи стегна, ніж при введенні у сідничні м’язи. Так, наприклад, при введенні в стегно з сечею екскретується значно більше цефалоридину, ніж при введенні у сідничну ділянку.
При інгаляційному введенні більшість речовин абсорбуються і проявляють системну дію, хоча багато з них мають і місцевий ефект. Вдихання газоподібних і рідких лікарських речовин (аерозолів) забезпечує майже таке саме швидке надходження їх в кров, як і введення у вену, однак воно не є інвазивним, що важливо стосовно дітей, осіб похилого віку і виснажених хворих. Швидкість абсорбції залежить від об’єму дихання, площі активної поверхні альвеол, проникності їх стінки, розчинності речовин у ліпідах, йонізації молекул ЛЗ, інтенсивності кровотоку. Є дані про всмоктування лікарських засобів із сечового міхура. Наприклад, при введенні в сечовий міхур тіо-ТЕФу, адріаміцину, дауноміцину всмоктувалося через 1 годину 2-20 % від уведеної дози цих препаратів. Всмоктування препаратів зростало при захворюваннях чи під час проведення інструментальних досліджень. При запальних захворюваннях статевої сфери у жінок в ряді випадків використовують місцеве застосування ЛЗ, наприклад, введення їх у порожнину матки. Результати про всмоктування в кров після ін’єкції в порожнину матки отримані для стрептоміцину, причому всмоктування зростало при одночасному введенні гіалуронідази.
Схожі презентації
Категорії