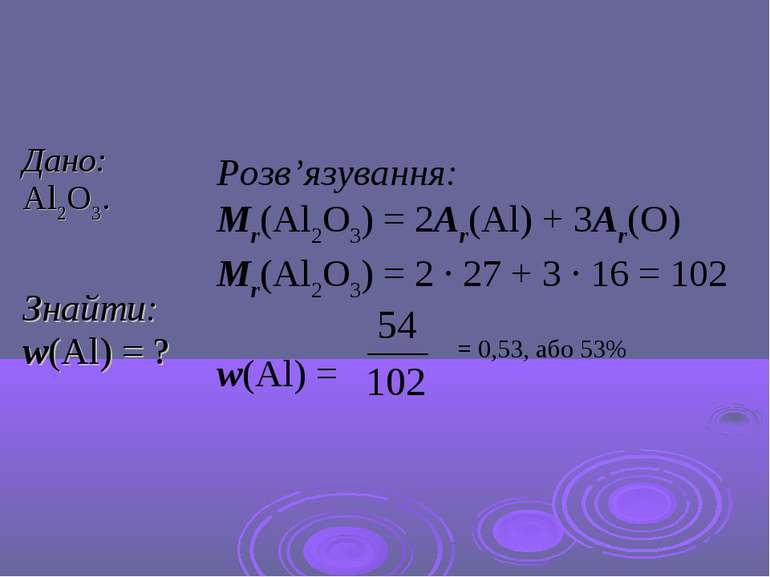Презентація на тему:
Масова частка елемента в речовині
Завантажити презентацію
Масова частка елемента в речовині
Завантажити презентаціюПрезентація по слайдам:
Мета Закріпити знання про хімічні формули, вміння обчислювати відносну молекулярну масу. Поширити знання з математики про частки на обчислення масової частки елемента в складі речовини. Навчити обчислювати масову частку елемента в складній речовині, використовувати поняття «масова частка» для розв'язання задач на визна чення хімічних формул
Хімічна формула дає змогу обчислити не тільки відносну молекулярну чи формульну маси, а ще й масову частку, яка припадає на кожний елемент у складі речовини.
Масова частка елемента в речовині – це величина, що визначається відношенням маси, яка припадає на елемент, до маси всієї речовини.
Масова частка позначається w (читається дубль-ве) і виражається у частках одиниці або у відсотках. Спосіб обчислення полягає у знаходженні частини від цілого за формулою: w = де w – масова частка елемента; Ar – відносна атомна маса елемента; n – кількість атомів елемента у формулі; Mr – відносна молекулярна або формульна маса речовини.
Висновки Масова частка елемента в речовині – це також безрозмірна фізична величина, що дорівнює відношенню маси елемента до загальної маси речовини. Знаючи масову частку елемента, можна визначити його масу в будь-якій масі речовини і за масовими частками елементів визначити формулу речовини.
Приклади розв’язування задач Задача 1 Обчислити масову частку Алюмінію у глиноземі Al2O3. Задача 2 Визначити, яку масу алюмінію можна дістати з глинозему масою 200 тис. т, якщо відомо, що масова частка Алюмінію в глиноземі становить 53%. Задача 3 Вивести формулу речовини, якщо відомо, що до її складу входить Сульфур (масова частка становить 40%) і Оксиген.
Розв’язування: Mr(Al2O3) = 2Ar(Al) + 3Ar(O) Mr(Al2O3) = 2 · 27 + 3 · 16 = 102 w(Al) = = 0,53, або 53%
Дано: m(Al2O3) = 200 тис.т. w(Al) = 53% = 0,53 m(Al) - ? Розв’язування: З умови задачі відомо, що глинозем масою 1т містить 1т · 0,53 = 0,53т Al, а 200 тис. т – 200тис. т · 0,53 = 106 тис. т Al.
Дано: w(S) = 40% w (O) = 60% SxOy - ? Розв’язування: Позначимо число атомів Сульфуру через х, атомів Оксигену – через у. Число атомів у речовині прямо пропорційне масовій частці елемента й обернено пропорційне його відносній атомній масі, тобто x : y = х : у = 1,25 : 3,75 Знайдені числа виражають кількісне відношення між атомами елементів. Але відношення між атомами може бути виражене тільки цілими числами. Тому обираємо найменше із знайдених чисел, приймаємо його за одиницю і ділимо на нього решту чисел: х : у =
Схожі презентації
Категорії