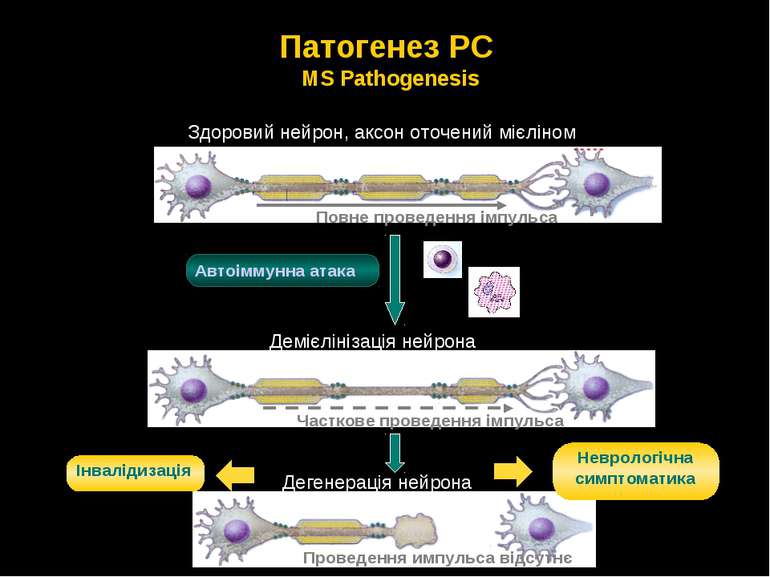
Презентація на тему:
Сучасні методи діагностики і лікування розсіяного склерозу у пацієнтів
Завантажити презентацію
Сучасні методи діагностики і лікування розсіяного склерозу у пацієнтів
Завантажити презентаціюПрезентація по слайдам:
Сучасні методи діагностики і лікування розсіяного склерозу. Керівник КМ Центру РС к.м.н. Кобись Т.О.
Актуальність проблеми Currency of problem Вcьoго у світі нараховується більше 2,5 млн. хворих на РС. В Україні зареєстровано 18,5 тис. хворих на РС. РС – імунопатологічне захворювання, що характеризується демієлінізацією білої речовини ЦНС Довгостроковий прогноз неблагоприємний Через 15 років після початку захворювання пацієнти: > 80% мають обмеження функцій > 50% не можуть пересуватися без сторонньої допомоги > 70% мають труднощі при самообслуговуванні
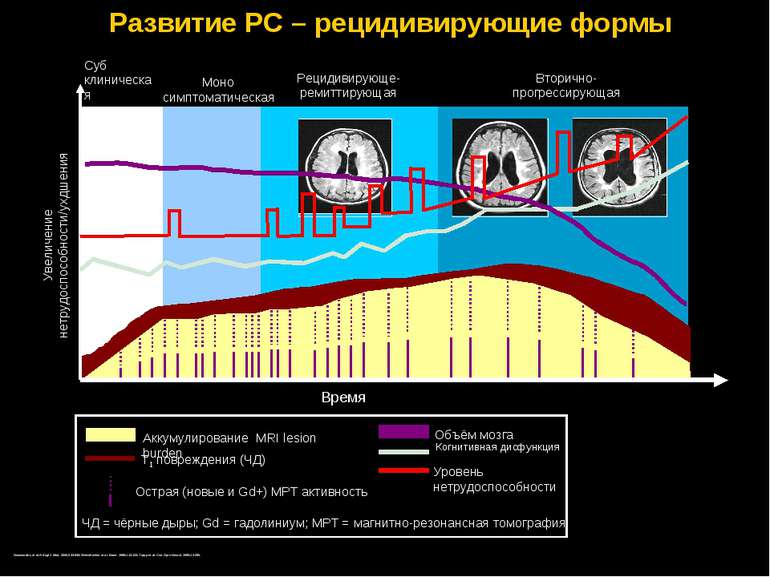
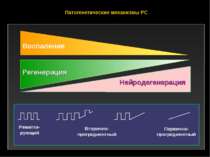
Развитие РС – рецидивирующие формы Увеличение нетрудоспособности/ухдшения ЧД = чёрные дыры; Gd = гадолиниум; МРТ = магнитно-резонансная томография. Время Уровень нетрудоспособности Объём мозга T1 повреждения (ЧД) Аккумулирование MRI lesion burden Острая (новые и Gd+) МРТ активность Когнитивная дисфункция Суб клиническая Моно симптоматическая Рецидивирующе-ремиттирующая Вторично-прогрессирующая Noseworthy et al. N Engl J Med. 2000;343:938; Weinshenker et al. Brain. 1989;112:133; Trapp et al. Curr Opin Neurol. 1999;12:295.
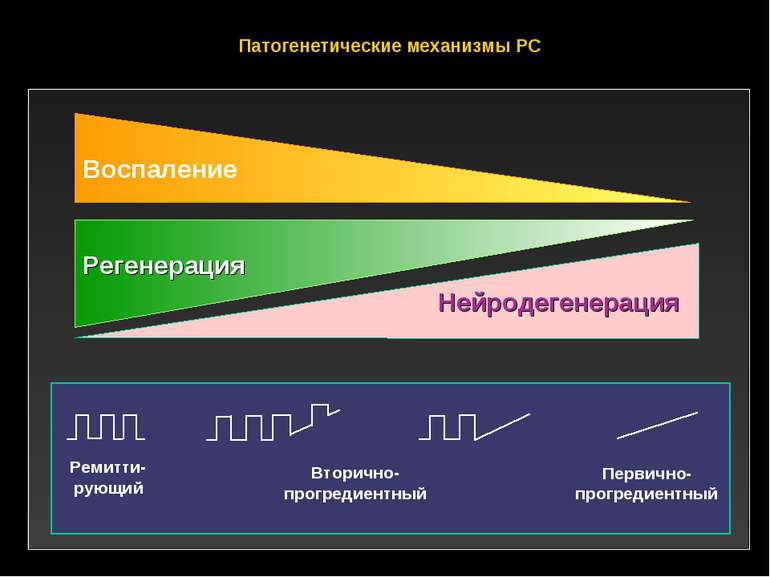
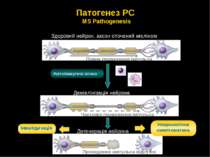
Большинство процессов повреждения, восстановления и нейродегенерации являются клинически невидимыми при РС Обострения Инвалидизация Когнитивные нарушения Воспаление, определяемое МРТ Демиелинизация Нейродегенерация Атрофия мозга . Клинически видимые процессы Не видимая активность заболевания
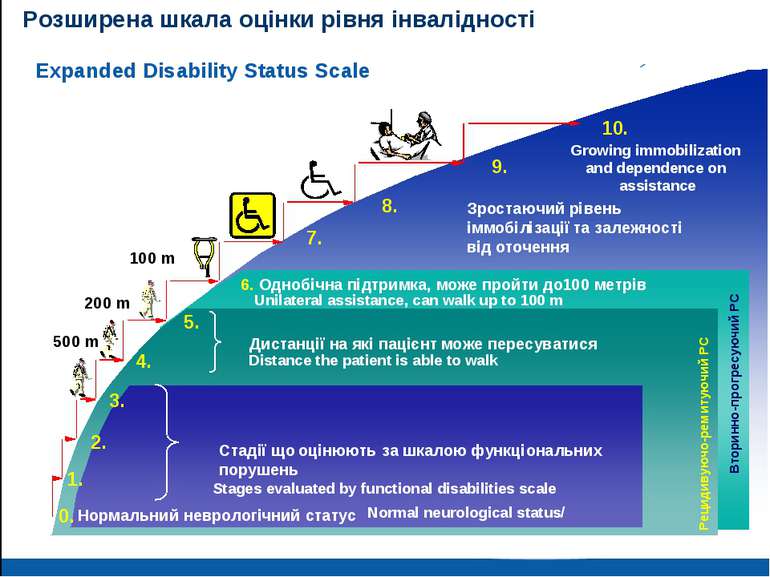
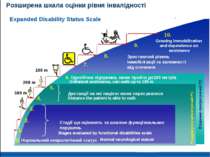
Розширена шкала оцінки рівня інвалідності Distance the patient is able to walk Unilateral assistance, can walk up to 100 m Stages evaluated by functional disabilities scale / Normal neurological status Growing immobilization and dependence on assistance
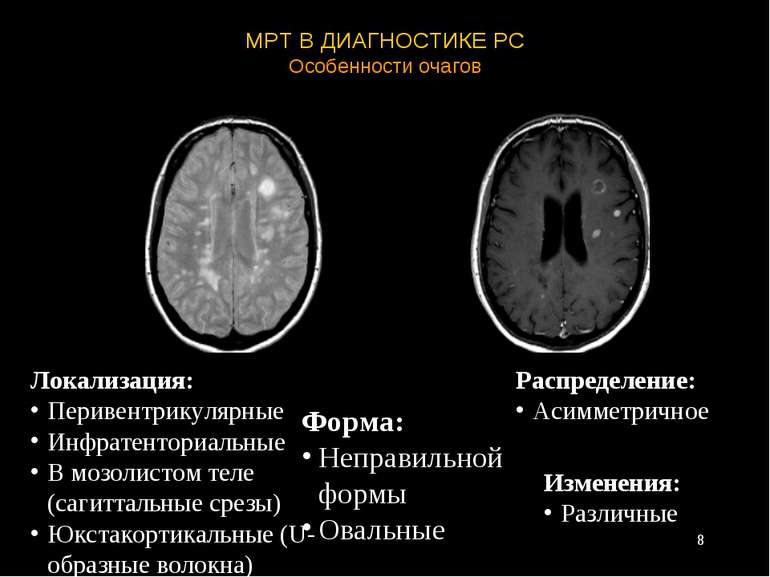
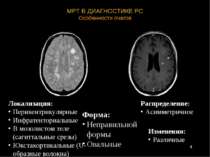
МРТ В ДИАГНОСТИКЕ РС Особенности очагов Локализация: Перивентрикулярные Инфратенториальные В мозолистом теле (сагиттальные срезы) Юкстакортикальные (U-образные волокна) Форма: Неправильной формы Овальные Распределение: Асимметричное Изменения: Различные *
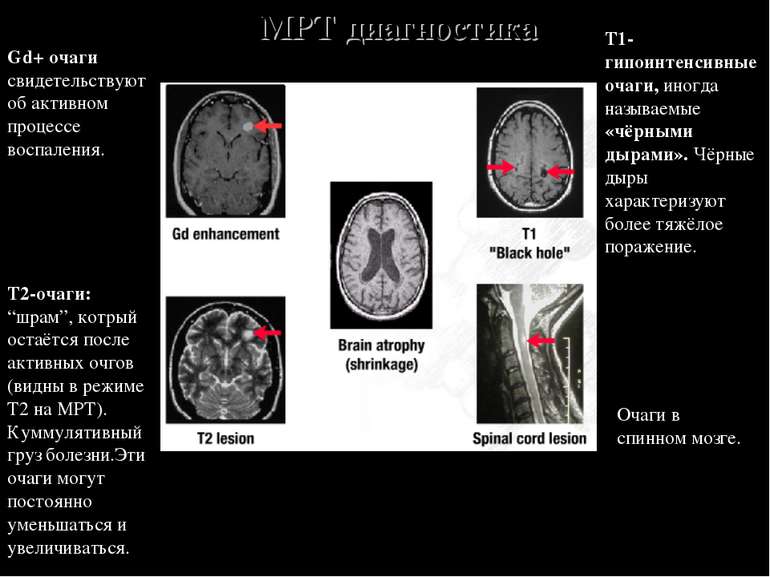
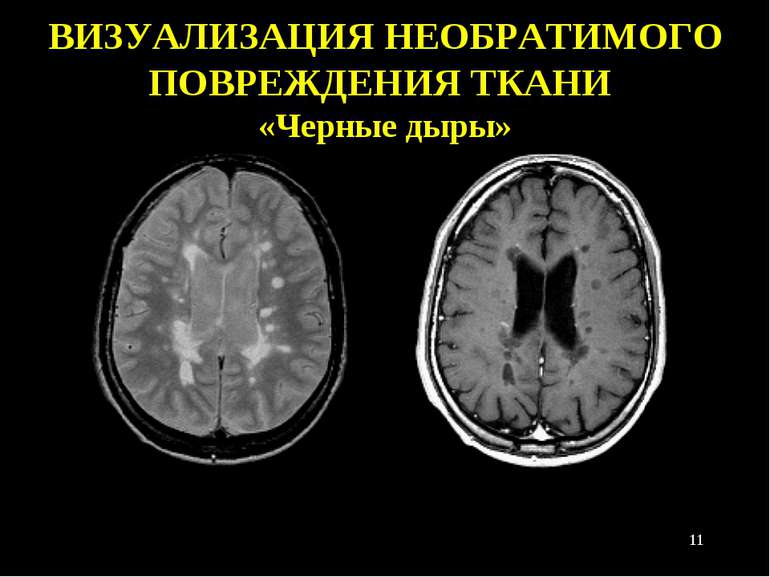
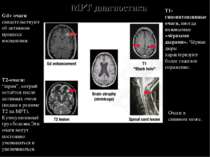
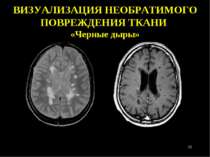
Т1-гипоинтенсивные очаги, иногда называемые «чёрными дырами». Чёрные дыры характеризуют более тяжёлое поражение. Очаги в спинном мозге. Gd+ очаги свидетельствуют об активном процессе воспаления. Т2-очаги: “шрам”, котрый остаётся после активных очгов (видны в режиме T2 на МРТ). Куммулятивный груз болезни.Эти очаги могут постоянно уменьшаться и увеличиваться. МРТ диагностика
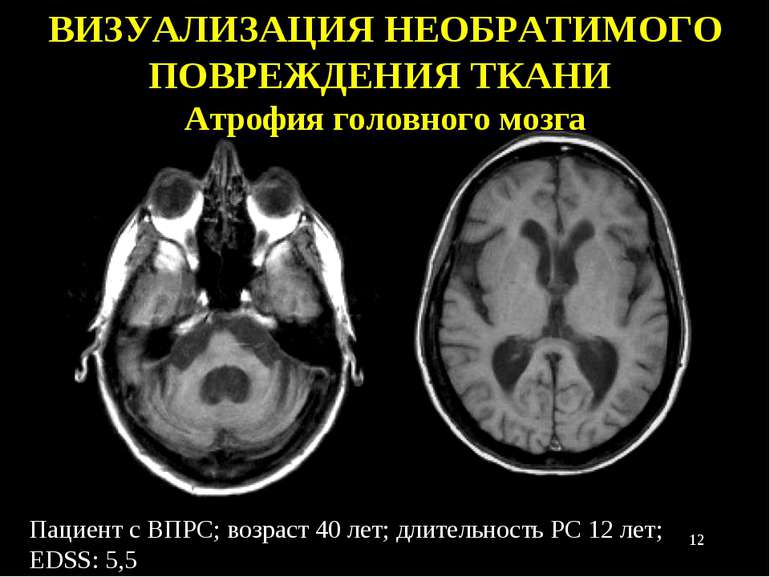
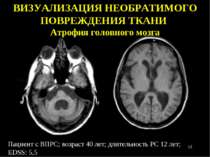
Пациент с ВПРС; возраст 40 лет; длительность РС 12 лет; EDSS: 5,5 ВИЗУАЛИЗАЦИЯ НЕОБРАТИМОГО ПОВРЕЖДЕНИЯ ТКАНИ Атрофия головного мозга *
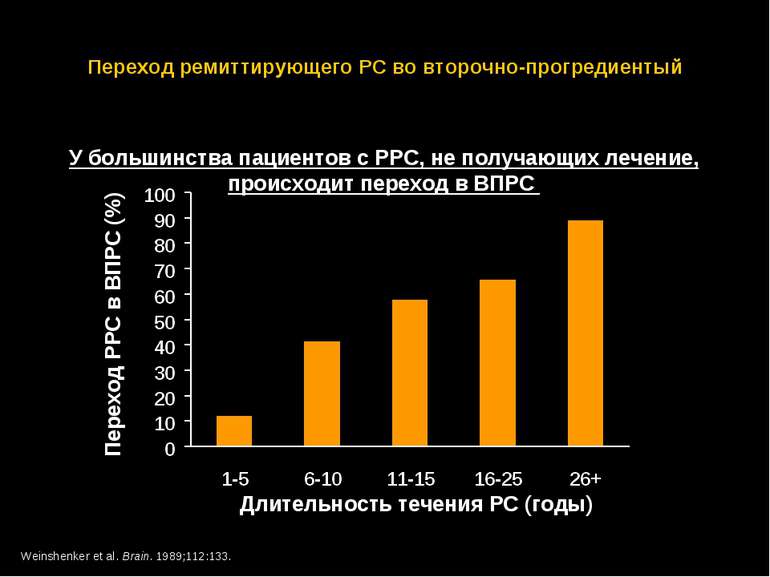
Переход ремиттирующего РС во второчно-прогредиентый Weinshenker et al. Brain. 1989;112:133. Переход РРС в ВПРС (%) Длительность течения РС (годы) У большинства пациентов с РРС, не получающих лечение, происходит переход в ВПРС
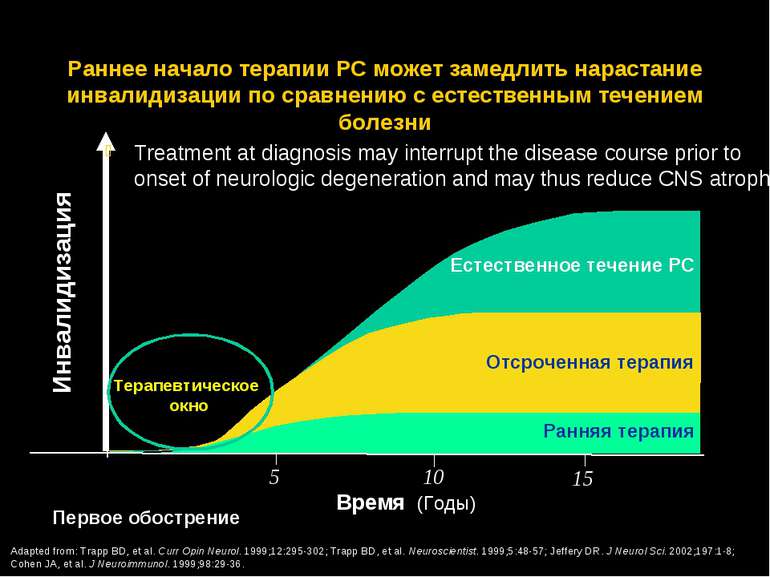
Раннее начало терапии РС может замедлить нарастание инвалидизации по сравнению с естественным течением болезни Естественное течение РС Отсроченная терапия Ранняя терапия Первое обострение Инвалидизация Время (Годы) Adapted from: Trapp BD, et al. Curr Opin Neurol. 1999;12:295-302; Trapp BD, et al. Neuroscientist. 1999;5:48-57; Jeffery DR. J Neurol Sci. 2002;197:1-8; Cohen JA, et al. J Neuroimmunol. 1999;98:29-36. 5 10 15 Терапевтическое окно Treatment at diagnosis may interrupt the disease course prior to onset of neurologic degeneration and may thus reduce CNS atrophy
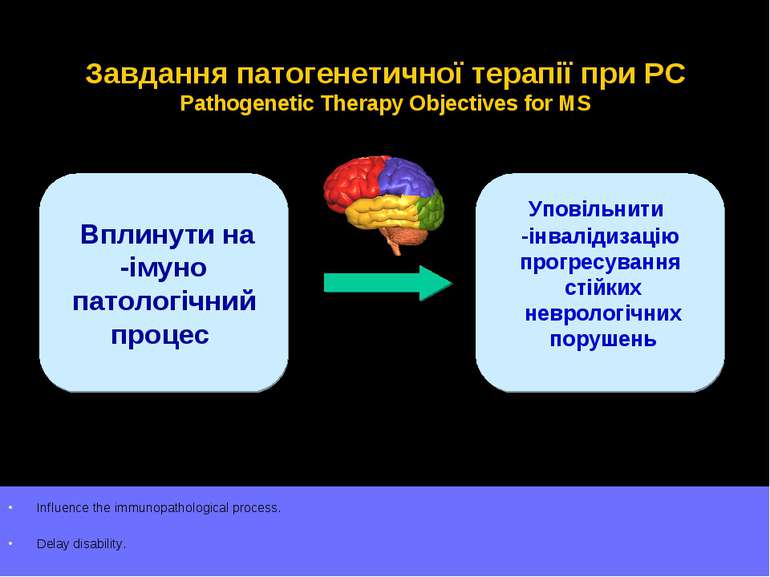
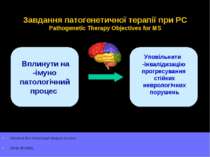
Завдання патогенетичної терапії при РС Pathogenetic Therapy Objectives for MS Вплинути на імуно- патологічний процес Уповільнити інвалідизацію- прогресування стійких неврологічних порушень Influence the immunopathological process. Delay disability.
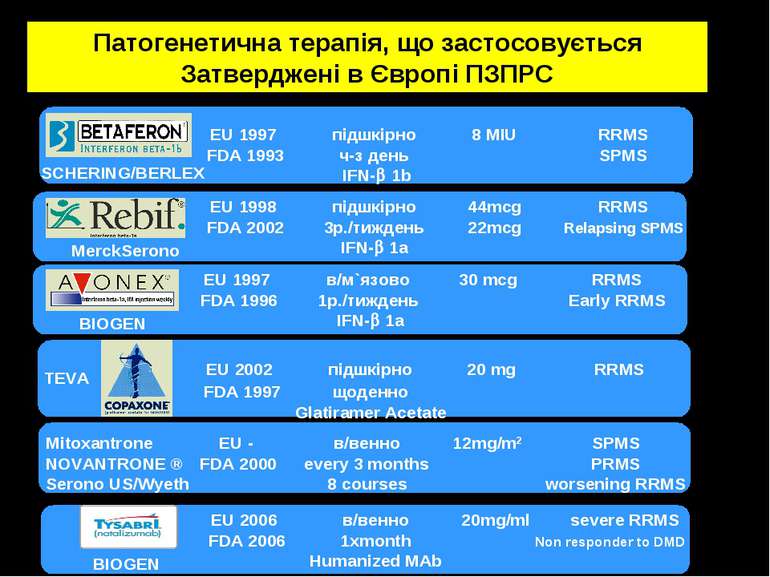
Сравнительная характеристика препаратов Интерферон β-1а Интерферон β-1а Интерферон β-1В Глатимера ацетат Натализумаб Частота введения 3 раза в неделю 1 раз в неделю Через день Каждый день 1 раз в месяц Способ введения Подкожно Глубоко внутримышечно Подкожно Подкожно Внутривенная инфузия Доступный аутоинжектор Нет Нет Да Нет Нет Форма выпуска Заполненный шприц Заполненный шприц Заполненный шприц Заполненный шприц Концентриро-ванный р-р для инфузии Размер иглы 29G 23G 30G 29G Условия хранения Нуждается в охлаждении Нуждается в охлаждении Комнатная температура Нуждается в охлаждении Нуждается в охлаждении Программа индивидуальной поддержки пациентов Нет Нет Да Нет Нет Возможность амбулаторного лечения или на дому Да Да Да Да Только в условиях специализи-рованного стационара
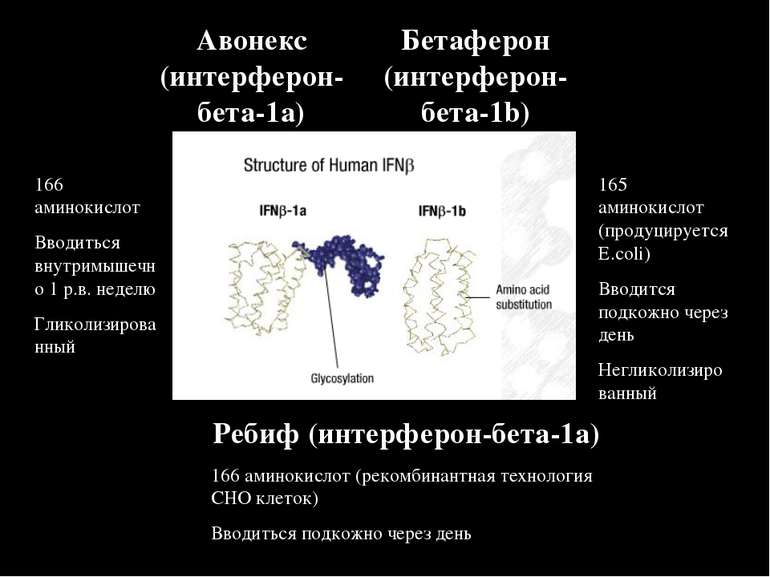
Авонекс (интерферон-бета-1а) Бетаферон (интерферон-бета-1b) 165 аминокислот (продуцируется E.coli) Вводится подкожно через день Негликолизированный 166 аминокислот Вводиться внутримышечно 1 р.в. неделю Гликолизированный Ребиф (интерферон-бета-1а) 166 аминокислот (рекомбинантная технология CHO клеток) Вводиться подкожно через день
Дія інтерферонів-бета на рівні імунної системи Бетаінтерферони знижують експресію прозапальних субстанцій та підвищує єкспресію протизапальних медіаторів.
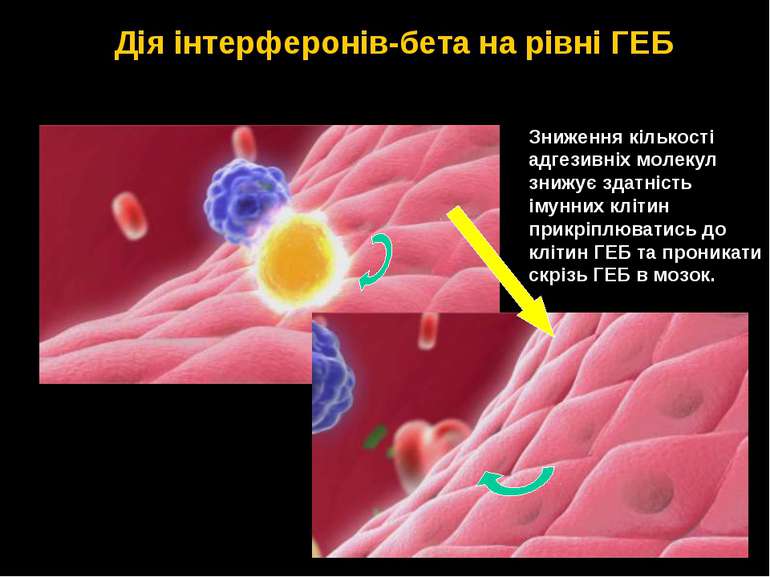
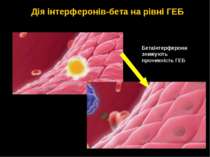
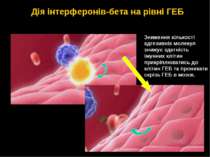
Зниження кількості адгезивніх молекул знижує здатність імунних клітин прикріплюватись до клітин ГЕБ та проникати скрізь ГЕБ в мозок. Дія інтерферонів-бета на рівні ГЕБ
Глатирамера Ацетат (ГА) Стандартизированная смесь синтетических полипептидов, содержащих четыре аминокислоты: L-глутаминовую кислоту, L-лизин, L-аланин и L-тирозин в определенном молярном соотношении, напоминающих основной белок миелина (ОБМ) - myelin basic protein (MBP)
Из истории создания Копаксон (Тева) был создан в ходе экспериментов на мышиной модели экспериментального аллергического энцефалита (ЭАЭ) в научном институте (Израиль). С целью активировать аутоиммунные реакции и вызвать развитие экспериментального аллергического энцефалита мышам вводились пептиды (кополимеры), сходные по аминокислотной последовательности с основным белком миелина (ОБМ). Всего было синтезировано и протестировано 11 различных кополимеров. Неожиданно оказалось, что кополимеры не могут вызвать ЭАЭ. Напротив, они уменьшают проявления ЭАЭ у животных с уже развившимся заболеванием (Teitelbaum, 1971). С этого момента началась серия экспериментов на животных: глатирамера ацетат уменьшал выраженность ЭАЭ на моделях мышей, крыс, морских свинок и приматов. Наиболее эффективным оказался кополимер-1 (глатирамера ацетат, Копаксон). Известно, что макаки-резус и бабуины при развитии ЭАЭ, индуцированного ОБМ, погибают через 2 недели после начала клинических проявлений. Введение же им ГА вызывало обратное развитие симптоматики.
Механизм действия Копаксона Действие Копаксона направлено не на общее подавление иммунного ответа, а на селективное торможение аутореактивных Т-лимфоцитов. Являясь по строению аналогом фрагмента основного белка миелина Копаксон конкурирует с ним за связывание с антиген-представляющими молекулами на клетках крови в процессе формирования тримолекулярного комплекса - начальном этапе любой иммунной реакции и в связи с этим, подавляет иммунный ответ на основной антиген-миелин, предупреждая, таким образом, развитие демиелинизирующего повреждения в ЦНС.
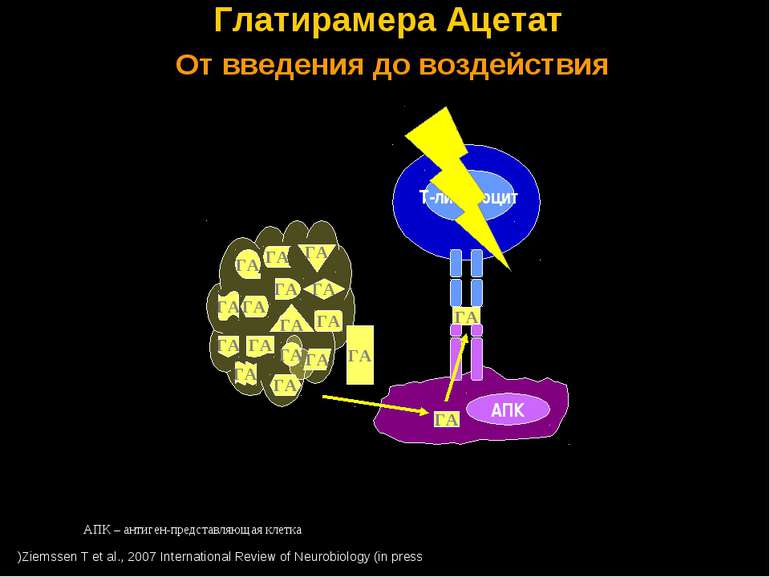
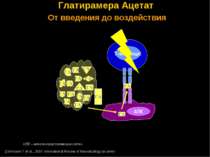
ГА ГА Глатирамера Ацетат От введения до воздействия Ziemssen T et al., 2007 International Review of Neurobiology (in press) АПК – антиген-представляющая клетка
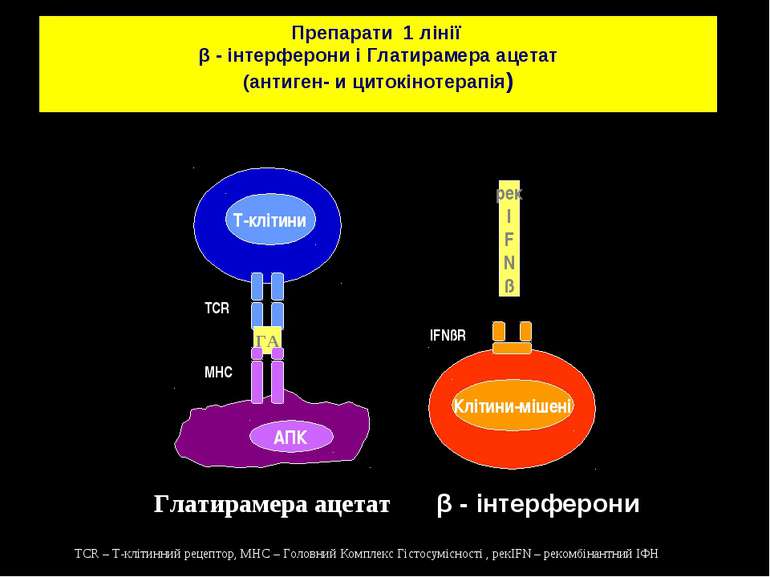
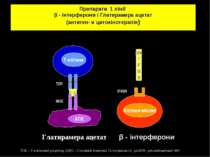
ГА TCR MHC Клітини-мішені рек I F N ß IFNßR Глатирамера ацетат Препарати 1 лінії β - інтерферони і Глатирамера ацетат (антиген- и цитокінотерапія) β - інтерферони TCR – Т-клітинний рецептор, МHC – Головний Комплекс Гістосумісності , рекIFN – рекомбінантний ІФН
Терапія другої лінії - Мітоксантрон і Тісабрі (наталізумаб) Мітоксантрон - діє на CD4-лімфоцити, заторможує синтез РНК та ДНК за рахунок вбудовування в їх структуру з наступною блокіровкою синтезу, викликає аберацію хромосом за рахунок дії на топоізомеразу ІІ. Потрібно проводити моніторинг рівня лей.,тромб., в крові у звязку з цитотоксичною дією та моніторинг ЕКГ Тісабрі-нове направлення в лікуванні РС (моноклональне антитіло) Призначаються в разі відсутності ефекту від препаратів 1 лінії, наявності протипоказань та виражених побічних явищ злоякісного перебігу РС
Моноклональні антитіла – новий напрямок в лікуванні РС Використовується унікальна властивість розрізняти і зв’язувати різні молекулярні групування, що беруть участь в патологічному процесі. Перші препарати антитіл були отримані при імунізації тварин, в подальшому розроблені технології отримання повністю гуманізованих антитіл. Моноклональні антитіла широко застосовуються в онкології, а також для терапії аутоімунних і хронічних запальних захворювань (ревматоїдний артрит, псоріаз, розсіяний склероз) Для лікування аутоімунних захворювань застосовується цілий ряд гуманізованих антитіл, блокующих різні механізми імунітету. Серед них антитіла до рецепторів - Т-лімфоцитів СD25, СD52 – гальмують активацію лімфоцитів, - СD4 – блокують функцію Т-лімфоцитів – хелперів - СD18 – перешкодають міграції лімфоцитів в осередок запалення та інші.
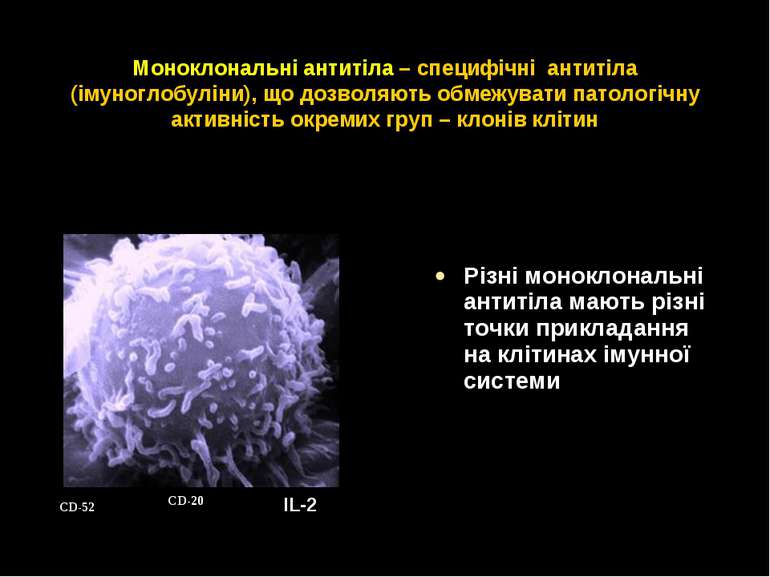
Моноклональні антитіла – специфічні антитіла (імуноглобуліни), що дозволяють обмежувати патологічну активність окремих груп – клонів клітин Різні моноклональні антитіла мають різні точки прикладання на клітинах імунної системи IL-2 СD-20 СD-52
Моноклональні антитіла Т-клітини Natalizumab Схвалений в 2006 році Daclizumab Аlemtuzumab Ustakinumab В-клітини Rituximab Ocralizumab Ofatumumab Ataccept
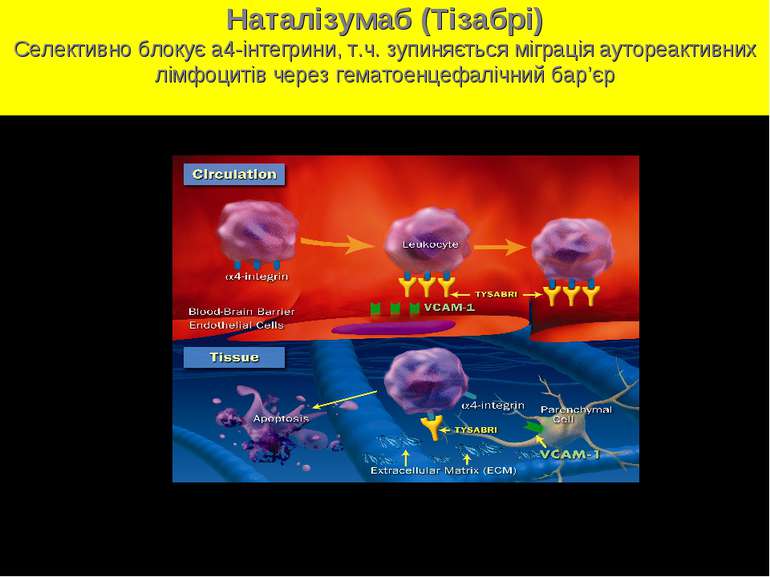
Наталізумаб (Тізабрі) Селективно блокує а4-інтегрини, т.ч. зупиняється міграція аутореактивних лімфоцитів через гематоенцефалічний бар’єр
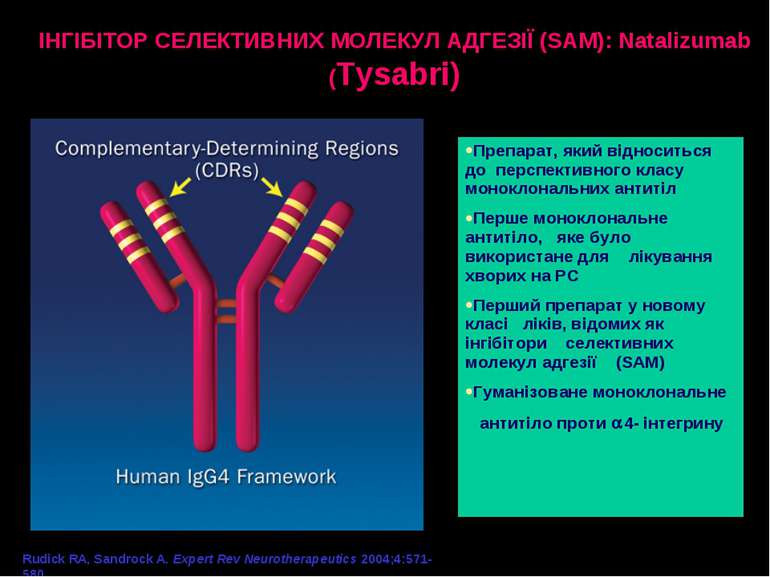
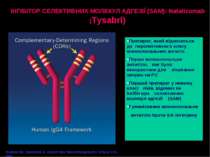
ІНГІБІТОР СЕЛЕКТИВНИХ МОЛЕКУЛ АДГЕЗІЇ (SAM): Natalizumab (Tysabri) Препарат, який відноситься до перспективного класу моноклональних антитіл Перше моноклональне антитіло, яке було використане для лікування хворих на РС Перший препарат у новому класі ліків, відомих як інгібітори селективних молекул адгезії (SAM) Гуманізоване моноклональне антитіло проти 4- інтегрину Rudick RA, Sandrock A. Expert Rev Neurotherapeutics 2004;4:571-580.
Наталізумаб (Тізабрі) На кінець березня 2009 року 52 тис.пацієнтів у всьому світі отримали наталізумаб (комерційний і в клінічних дослідженнях); Наталізумаб знижує ризик прогресування інвалідизації на 42%, частоту клінічних рецидивів на 68% за рік, при МРТвиявлено на 92% меньше бляшок порівняно з плацебо (АFFIRM) Рідкі інфузії (1 раз на міс.) Крім пов’язаних з інфузією побічних дій (озноб, висипка, астенія) спостерігались віддалені побічні дії, повязані з імуносупресією, (вагінальні інф., тонзіліти,герпетичні інфекції) У 2 пацієнтів, що отримували комбіновану терапію наталізумабом і ІFNβ-1a розвинулась прогресуюча мультифокальна лейкоенцефалопатія .
ПРОГРЕСУЮЧА ЛЕЙКОЕНЦЕФАЛОПАТІЯ ПМЛ розвивається при імунодефіцитних станах різної етіології Частота розвитку ПМЛ після лікування Тізабрі 1.2/10 000 пацієнтів - Переваги лікування наталізумабом не дозволяють відмовитись від нього навіть під загрозою розвитку ПМЛ - На сучасному етапі – це не є фатальне захворювання, лікування проводится в умовах ВРІТ, застосовується метилпреднізолон 1000 мг №3, в/в крап. В подальшому – противірусні засоби – mefloquine, mitazapin - Для подальшого попередження випадків розвитку ПМЛ пропонується оцінювати титр вірусу в лікворі перед лікуванням.
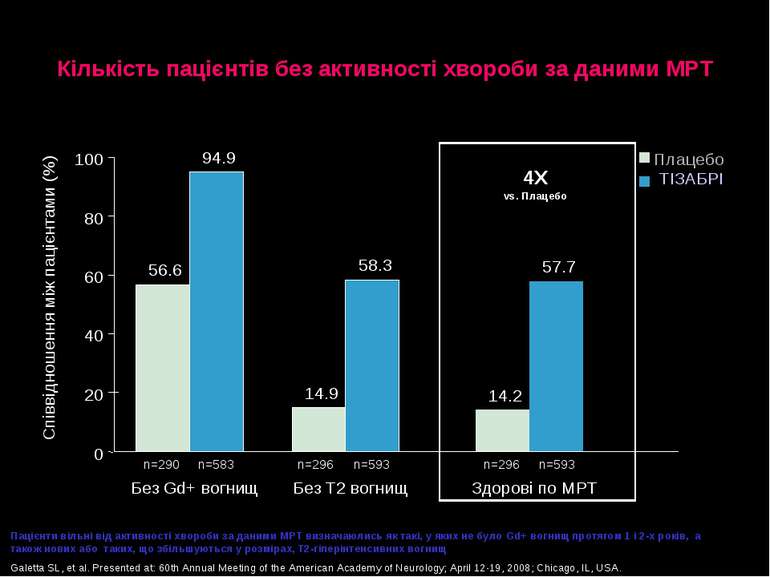
Кількість пацієнтів без активності хвороби за даними МРТ Пацієнти вільні від активності хвороби за даними МРТ визначаюлись як такі, у яких не було Gd+ вогнищ протягом 1 і 2-х років, а також нових або таких, що збільшуються у розмірах, T2-гіперінтенсивних вогнищ Galetta SL, et al. Presented at: 60th Annual Meeting of the American Academy of Neurology; April 12-19, 2008; Chicago, IL, USA. 56.6 14.9 14.2 94.9 58.3 57.7 0 20 40 60 80 100 Без Gd+ вогнищ Без T2 вогнищ Здорові по МРТ Співвідношення між пацієнтами (%) Плацебо ТІЗАБРІ n=290 n=583 n=296 n=593 n=296 n=593 4X vs. Плацебо
ТІЗАБРІ: Переваги перевищують Ризики Рідкий ризик ПМЛ ( 1.2/ 10 000 пацієнтів) Доведені переваги Зменшення рівня рецидивів Зниження прогре- сування інвалідності Покращення якості життя Свобода від хвороби Yousry TA, et al. N Engl J Med. 2006;354:924-933.
Моноклональні антитіла Переваги : -Висока специфічність; -Підвищення ефективності лікування; -Рідке введення; Попередження: -Тривале зменьшення кількості Т- і В-лімфоцитів; -Тривалий вплив на імунну відповідь -Рідкі, але серйозні побічні дії ( лейкоенцефалопатія, малегнізація) Моноклональні антитіла
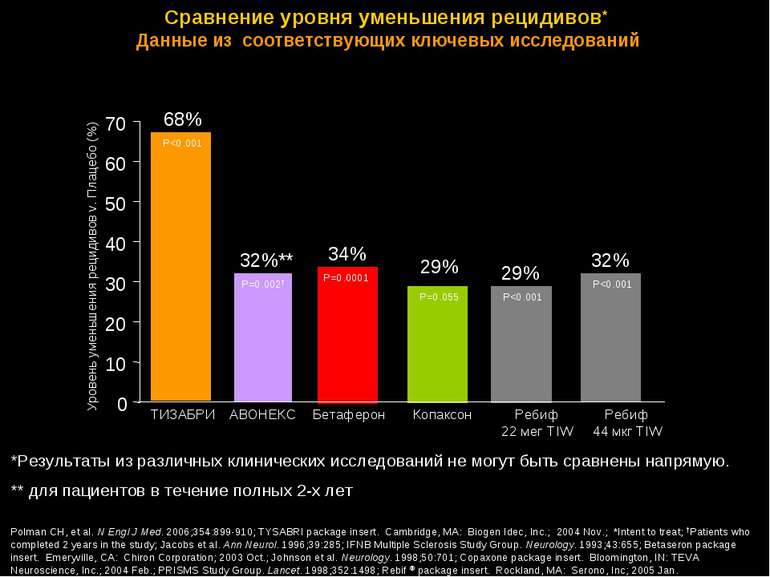
Сравнение уровня уменьшения рецидивов* Данные из соответствующих ключевых исследований *Результаты из различных клинических исследований не могут быть сравнены напрямую. ** для пациентов в течение полных 2-х лет Polman CH, et al. N Engl J Med. 2006;354:899-910; TYSABRI package insert. Cambridge, MA: Biogen Idec, Inc.; 2004 Nov.; *Intent to treat; †Patients who completed 2 years in the study; Jacobs et al. Ann Neurol. 1996;39:285; IFNB Multiple Sclerosis Study Group. Neurology. 1993;43:655; Betaseron package insert. Emeryville, CA: Chiron Corporation; 2003 Oct.; Johnson et al. Neurology. 1998;50:701; Copaxone package insert. Bloomington, IN: TEVA Neuroscience, Inc.; 2004 Feb.; PRISMS Study Group. Lancet. 1998;352:1498; Rebif ® package insert. Rockland, MA: Serono, Inc; 2005 Jan. Уровень уменьшения рецидивов v. Плацебо (%) 29% 34% 29% 68% 32% 32%** 0 10 20 30 40 50 60 70 Бетаферон Ребиф 22 мег TIW АВОНЕКС Копаксон ТИЗАБРИ Ребиф 44 мкг TIW P=0.0001 P=0.002† P
Влияние ПИТРС на степень атрофии головного мозга Galetta et al. Arch Intern Med. 2002;162:2161; Jacobs et al. N Engl J Med. 2000;343:898; Simon et al. Neurology. 2000;55:185; Li et al. Ann Neurol. 1999;46:197; PRISMS Study Group. Neurology. 2001;56:1628; Comi et al. Ann Neurol. 2001;49:290; Stone et al. Neurology. 1997;49:862; Rudick et al. Neurology. 1999;53:1698; Jones et al. Neurology. 2001;56(suppl 3):A379; Sormani et al. Neurology. 2004;62:1432-34. Препарат Атрофия мозга Авонекс® ↓ 55% (2-й год) Бетаферон® (8 MIU) Нет данных Ребиф® (44мкг) Не эффективен (p=СН) Копаксон® 2 противоречивых исследования (1 с положительным результатом и 1 с отрицательным) ↓ 25% (18 мес.) p=СН ↓ 40% (с 9 по 18 мес. используя метод SIENA) Натализумаб ↓ 44% (2-й год, p=0.004)
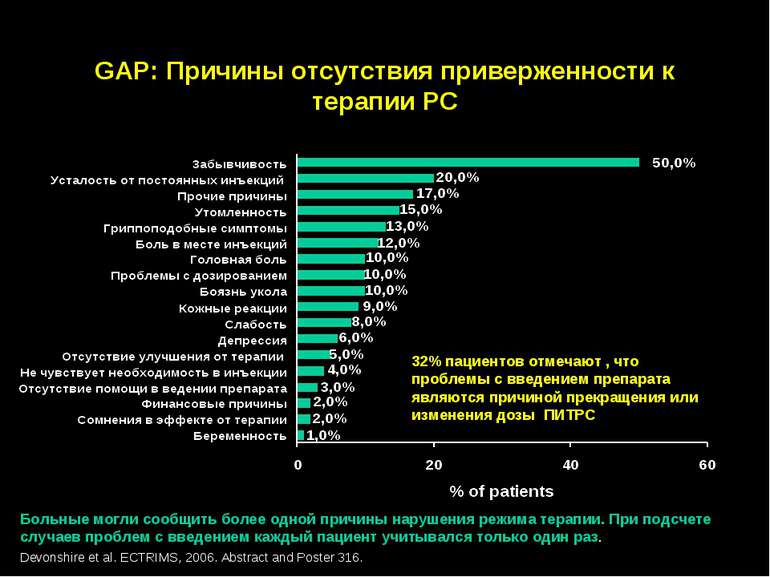
GAP: Причины отсутствия приверженности к терапии РС Больные могли сообщить более одной причины нарушения режима терапии. При подсчете случаев проблем с введением каждый пациент учитывался только один раз. Devonshire et al. ECTRIMS, 2006. Abstract and Poster 316. 32% пациентов отмечают , что проблемы с введением препарата являются причиной прекращения или изменения дозы ПИТРС
GAP: Причины отсутствия приверженности к терапии РС Забудькуватість – 50% Втома від постійних інєкцій -20% Грипоподібні симптоми -13% Біль в місті інєкцій – 12% Головний біль – 10% Боязнь інєкцій -10% Шкірні реакції -10%
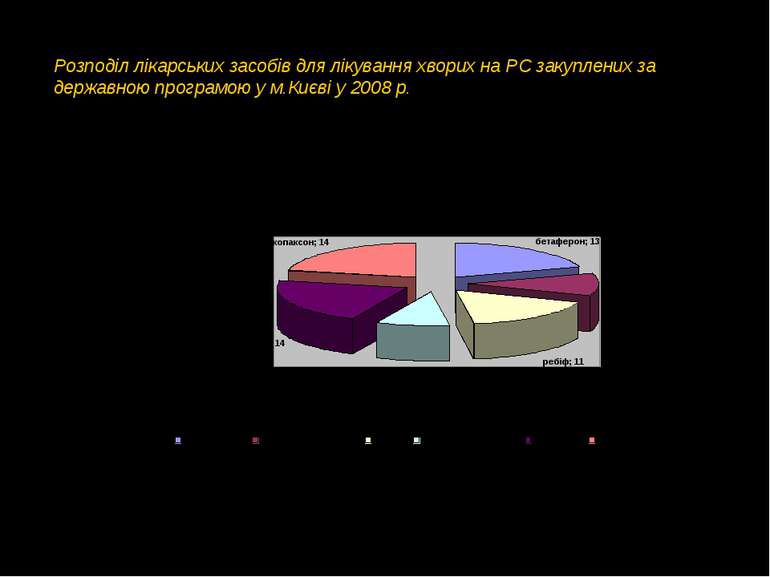
Розподіл лікарських засобів для лікування хворих на РС закуплених за державною програмою у м.Києві у 2008 р.
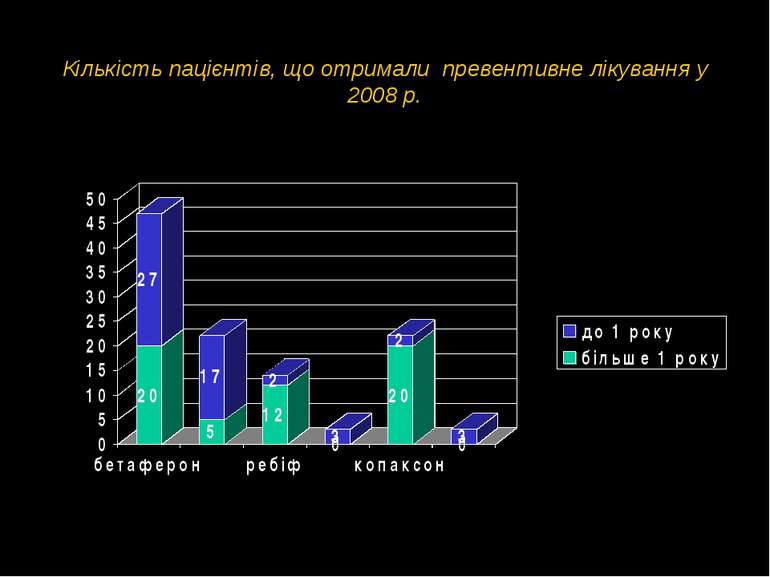
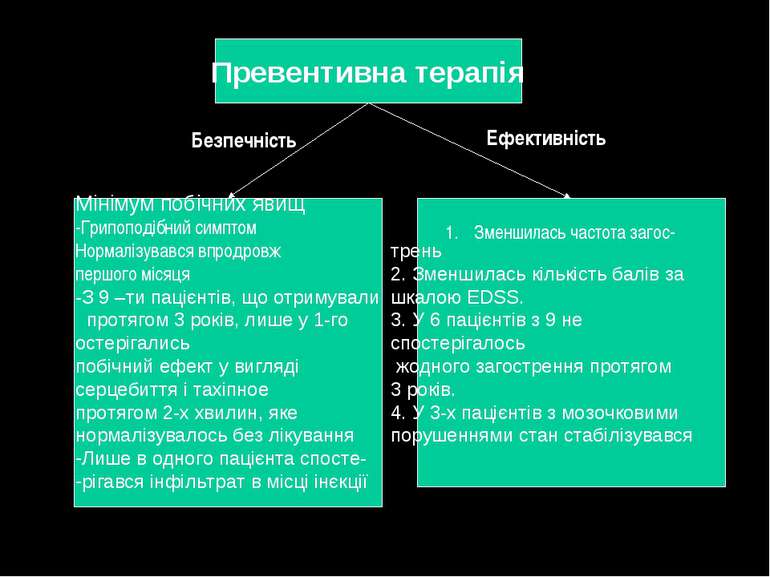
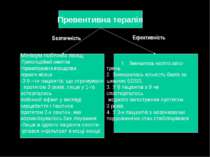
Превентивна терапія Мінімум побічних явищ -Грипоподібний симптом Нормалізувався впродровж першого місяця -З 9 –ти пацієнтів, що отримували протягом 3 років, лише у 1-го остерігались побічний ефект у вигляді серцебиття і тахіпное протягом 2-х хвилин, яке нормалізувалось без лікування Лише в одного пацієнта спосте- рігався інфільтрат в місці інєкції трень 2. Зменшилась кількість балів за шкалою EDSS. 3. У 6 пацієнтів з 9 не спостерігалось жодного загострення протягом 3 років. 4. У 3-х пацієнтів з мозочковими порушеннями стан стабілізувався Безпечність Ефективність Зменшилась частота загос-
Висновки: Conclusions На тлі прийому імунотропних препаратів у хворих з РС відмічається стабілізація неврологічного дефіциту за шкалою EDSS і зменьшення кількості загострень. Препарати патогенетичної терапії уповільнюютьпрогресування захворювання у хворих з РС
Схожі презентації
Категорії