Презентація на тему:
Хіміко-токсикологічний аналіз синтетичних „лікарських” отрут основного характеру
Завантажити презентацію
Хіміко-токсикологічний аналіз синтетичних „лікарських” отрут основного характеру
Завантажити презентаціюПрезентація по слайдам:
Хіміко-токсикологічний аналіз синтетичних „лікарських” отрут основного характеру Доц. Михалків М.М. Лекція № 14
ПЛАН. Застосування, токсикологічна характеристика, методи виділення з біологічного матеріалу і методи аналізу похідних п-амінобензойної кислоти. Застосування, токсикологічна характеристика, методи виділення з біологічного матеріалу і методи аналізу похідних фенотіазину. Застосування, токсикологічна характеристика, методи виділення з біологічного матеріалу і методи аналізу похідних 1,4-бензодіазепіну.
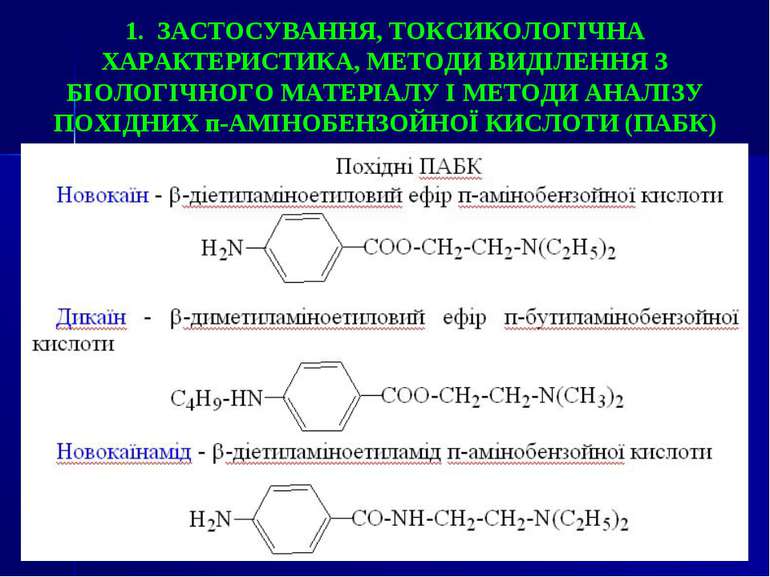
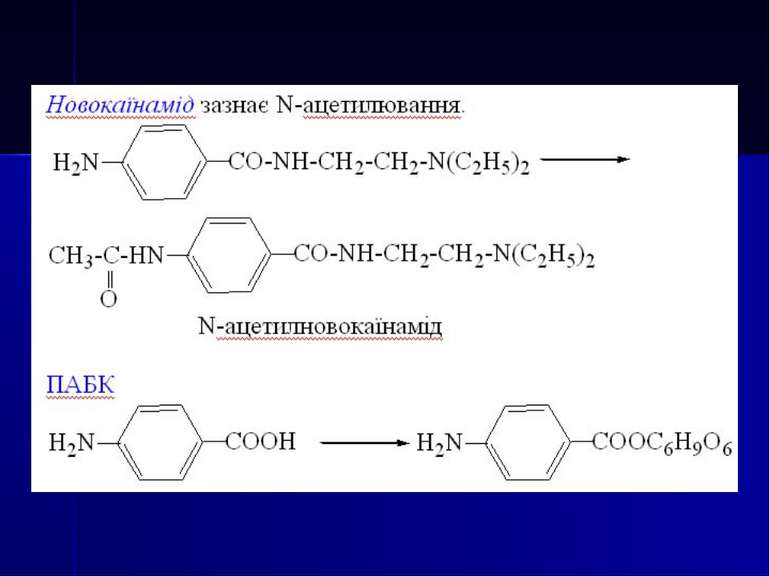
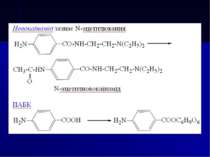
1. ЗАСТОСУВАННЯ, ТОКСИКОЛОГІЧНА ХАРАКТЕРИСТИКА, МЕТОДИ ВИДІЛЕННЯ З БІОЛОГІЧНОГО МАТЕРІАЛУ І МЕТОДИ АНАЛІЗУ ПОХІДНИХ п-АМІНОБЕНЗОЙНОЇ КИСЛОТИ (ПАБК)
Токсична дія У терапевтичних дозах вони викликають алергічні ускладнення (висипи на шкірі), запаморочення, диспепсичні явища, набряк шкіри, слизових оболонок, бронхоспазм. У токсичних дозах спричиняють порушення, а згодом параліч центральної нервової системи. Клінічна картина характеризується психомоторними порушеннями, судомами, втратою свідомості, зниженням артеріального тиску, брадикардією. За токсичністю дикаїн перевершує новокаїн (летальна доза 1 г) і новокаїнамід (летальна доза 1,5 г).
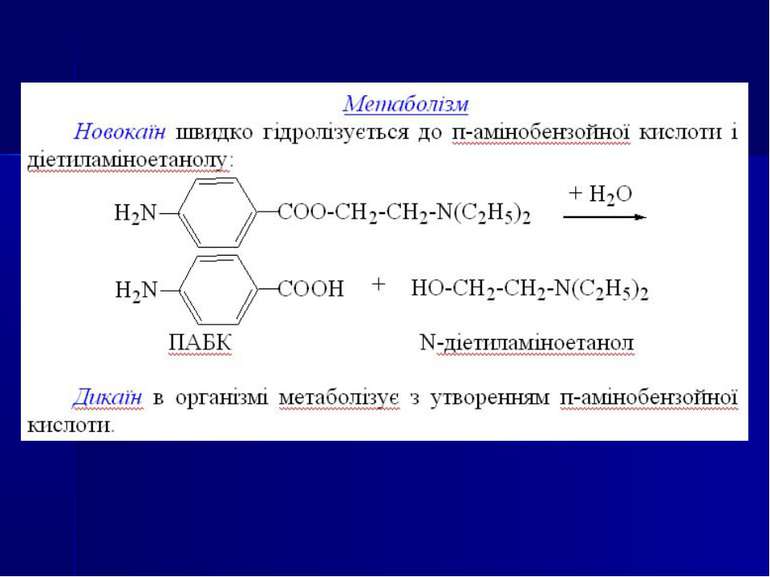
Направлений хіміко-токсикологічний аналіз на похідні ПАБК Об’єкти дослідження. Печінка, нирки, кров, сеча. Ізолювання – при ненаправленому аналізі – загальними методами (Васильєвої, Стаса-Отто), при направленому аналізі ізолювання з біологічних об’єктів (тканин органів) проводиться водою, підкисленою до рН = 2-3 хлоридною кислотою, при цьому солі препаратів добре розчиняються у воді. З водної фази препарати у вигляді основ екстрагуються хлороформом при рН = 11 (підлужнення водної фази проводять розчином NaOH). Домішки залишаються у водній фазі.
ТШХ-скринінг: у загальній системі розчинників хлороформ-діоксан-ацетон-25 %-вий розчин аміаку (45:47,5:5:2,5); сорбент - силікагель КСК – виявляються похідні ПАБК в 3-й зоні (Rf = 0,63-0,83). Після елюювання препаратів сумішшю розчинників метанол-25 %-вий розчин аміаку (9:1) проводять ТШХ-скринінг у окремій системі хлороформ-етанол (20:1), сорбент - алюмінію оксид. Для проявлення препаратів на пластинках використовують реактив Драгендорфа за Муньє (оранжево-коричневі плями) або ідентифікують за реакцією утворення азобарвника з -нафтолом (оранжеві плями).
Хімічні методи аналізу: 1. Реакції осадження із загальноалкалоїдними осадовими реактивами, в результаті яких утворюються кристалічні або аморфні осади. Реакції високочутливі, неспецифічні. 2. Мікрокристалоскопічні реакції - високочутливі, специфічні: - з реактивом Драгендорфа - кристали у вигляді тонких голок, зібраних у пучки (новокаїн) або ромбовидні пластинки (новокаїнамід); - з розчином тетрабромоауратної кислоти - кристали у вигляді пластинок і голок (новокаїн); - з розчином гексахлороплатинатної кислоти - щільні розетки (новокаїнамід); - з розчином натрій нітриту - призми, роздвоєні на кінцях (дикаїн).
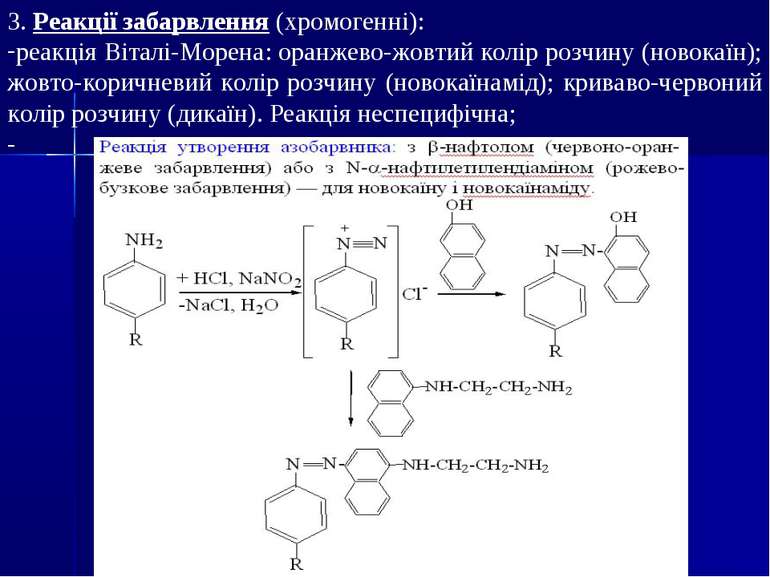
3. Реакції забарвлення (хромогенні): реакція Віталі-Морена: оранжево-жовтий колір розчину (новокаїн); жовто-коричневий колір розчину (новокаїнамід); криваво-червоний колір розчину (дикаїн). Реакція неспецифічна; -
4. Фізико-хімічні методи ідентифікації: за УФ- та ІЧ-спектрами, методами ТШХ, ГРХ, ВЕРХ Кількісне визначення проводиться спектральними (УФ-спектрофотометрія, фотоелектроколориметрія, екстракційна фотометрія) і хроматографічними (ТШХ - планіметричний і денситометричний методи; газо-рідинна та рідинна хроматографії) методами.
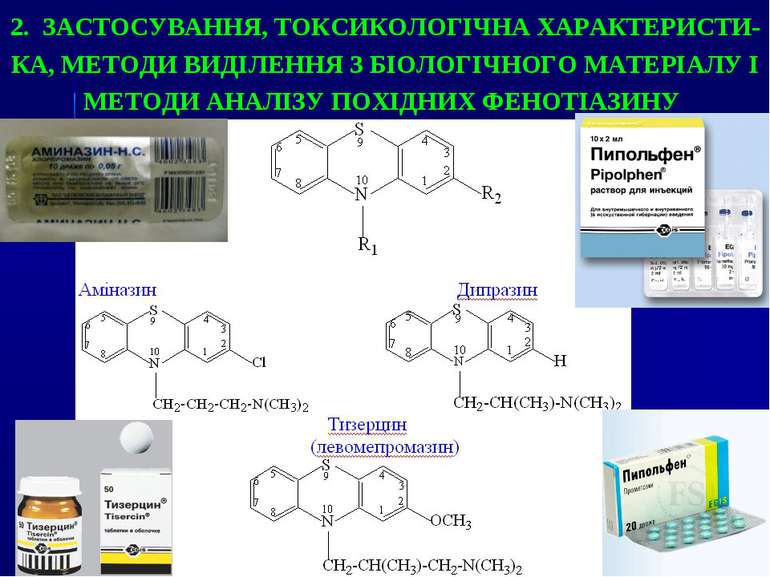
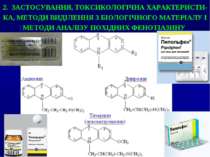
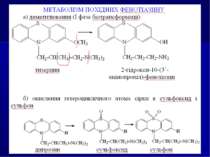
2. ЗАСТОСУВАННЯ, ТОКСИКОЛОГІЧНА ХАРАКТЕРИСТИ-КА, МЕТОДИ ВИДІЛЕННЯ З БІОЛОГІЧНОГО МАТЕРІАЛУ І МЕТОДИ АНАЛІЗУ ПОХІДНИХ ФЕНОТІАЗИНУ
Токсична дія Препарати характеризуються нейротоксичним ефектом, викликають порушення психіки, діяльності серцево-судинної системи, диспептичні явища, порушення гемодинаміки. При вживанні терапевтичних доз можливі ускладнення: падіння артеріального тиску, почастішання серцебиття, сухість у роті, світлобоязнь, сонливість. При гострих отруєннях похідними фенотіазину настає коматозний стан, який характеризується розширенням зіниць, зниженням температури тіла; відбувається різке пригнічення дихального і судиннорухового центрів; з’являються тахікардія, ниткоподібний пульс. Смерть настає при легенево-серцевій недостатності. Смертельна доза аміназину (для дорослих) 5-10 г.
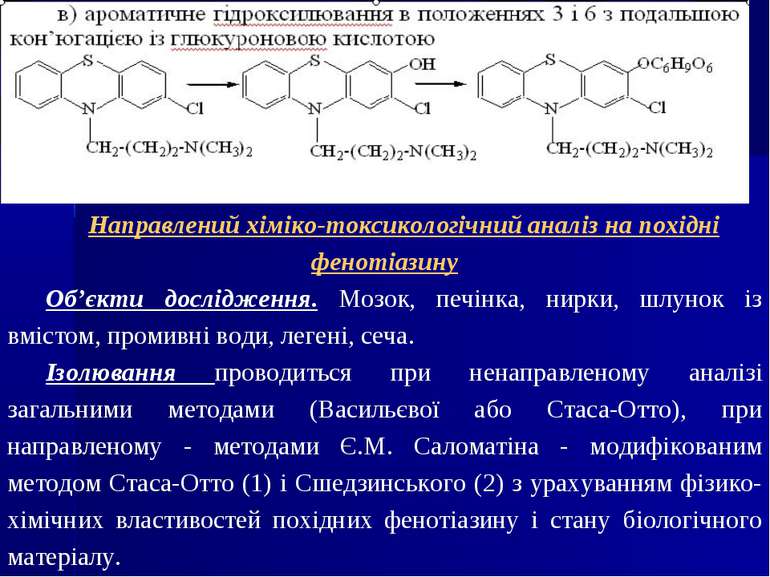
Направлений хіміко-токсикологічний аналіз на похідні фенотіазину Об’єкти дослідження. Мозок, печінка, нирки, шлунок із вмістом, промивні води, легені, сеча. Ізолювання проводиться при ненаправленому аналізі загальними методами (Васильєвої або Стаса-Отто), при направленому - методами Є.М. Саломатіна - модифікованим методом Стаса-Отто (1) і Сшедзинського (2) з урахуванням фізико-хімічних властивостей похідних фенотіазину і стану біологічного матеріалу.
ТШХ-скринінг проводиться в загальній системі розчинників хлороформ-діоксан-ацетон-25 %-вий розчин аміаку (45:47,5:5:2,5); сорбент - силікагель КСК; проявники - концентровані кислоти (H2SO4, HNO3, HC1), а також розчини окисників НС1О4 і NaNO2; реактиви Маркі, Манделіна. Наявність плям рожевого і бузкового кольорів у 3-й зоні (Rf = 0,63-0,83) вказує на можливу присутність похідних фенотіазину. Елювання проводять сумішшю метанол-25 % розчин аміаку (9:1) з подальшим проведенням підтверджуючого етапу в окремій системі розчинників хлороформ-етанол (20:1) і циклогексан-ацетон (5:1); сорбент - алюмінію оксид. Як “свідки” використовуються хлороформні розчини препаратів даної групи. Для подальшого аналізу фенотіазини вилучають з хроматограми елюентом метанол- 25 % розчин аміаку (9:1).
Хімічні методи аналізу: 1. Реакції осадження із загальноалкалоїдними осадовими реактивами (пікринова кислота, сіль Рейнеке, реактиви Драгендорфа, Марме, Майєра, Зонненшейна та ін.). 2. Реакції забарвлення засновані переважно на хімічних процесах окиснення, дегідратації, конденсації з альдегідами з використанням концентрованих кислот H2SO4, HNO3, HC1, НС1О4; реактивів Фреде, Манделіна, Маркі; розчинів солей FeCl3, NaNO2. Продукти реакцій забарвлені в червоно-фіолетовий, синюва то-червоний кольори. Реакції забарвлення чутливі, неспецифічні.
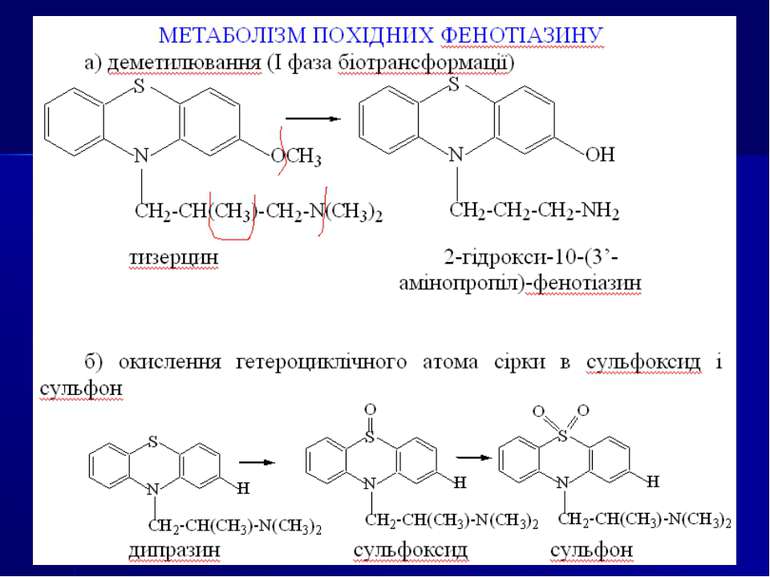
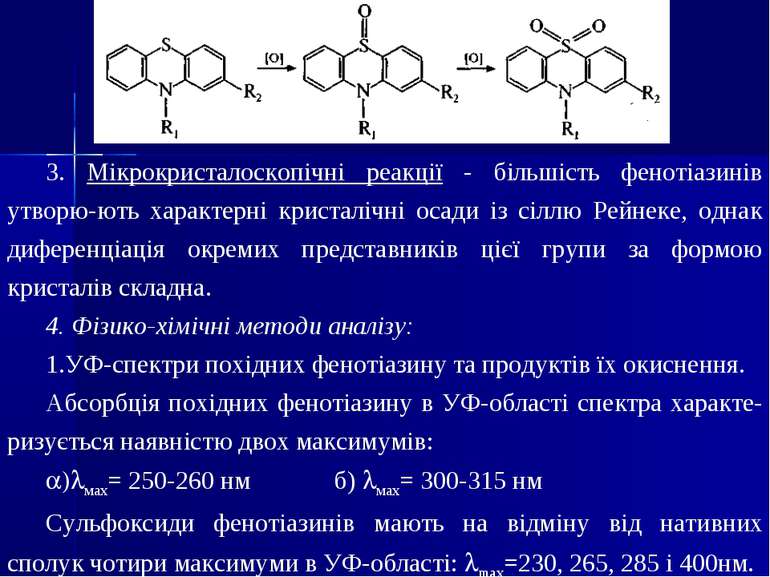
3. Мікрокристалоскопічні реакції - більшість фенотіазинів утворю ють характерні кристалічні осади із сіллю Рейнеке, однак диференціація окремих представників цієї групи за формою кристалів складна. 4. Фізико-хімічні методи аналізу: УФ-спектри похідних фенотіазину та продуктів їх окиснення. Абсорбція похідних фенотіазину в УФ-області спектра характе ризується наявністю двох максимумів: мах= 250-260 нм б) мах= 300-315 нм Сульфоксиди фенотіазинів мають на відміну від нативних сполук чотири максимуми в УФ-області: maх=230, 265, 285 і 400нм.
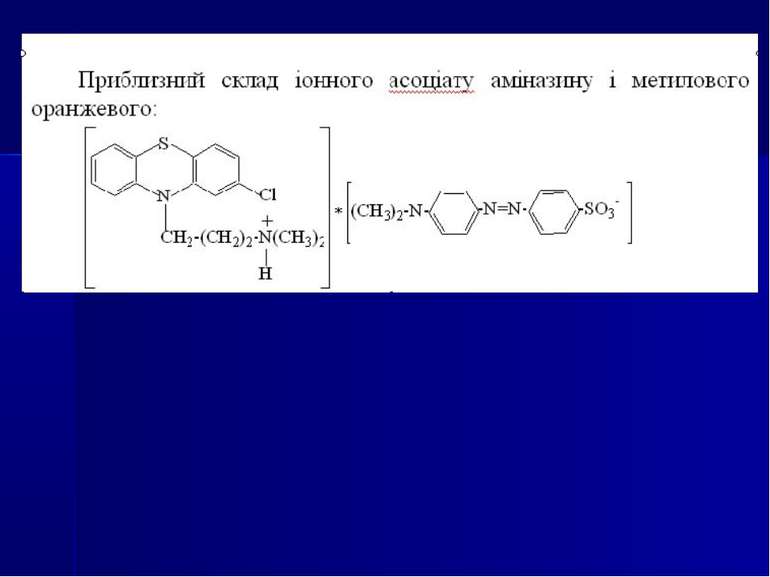
Кількісне визначення проводиться спектральними (УФ-спектрофотометрія, фотоелектроколориметрія, екстракційна фотометрія) і хроматографічними (ТШХ - планіметричний і денситометричний методи; газо-рідинна та рідинна хроматографії) методами. Екстракційна фотометрія заснована на екстракції хлорофор мом іонних асоціатів фенотіазинів з кислотним індикатором (метиловим оранжевим) із подальшим вимірюванням оптичної густини забарвленого органічного шару. Метод чутливий, не вимагає високого ступеня очистки від домішок.
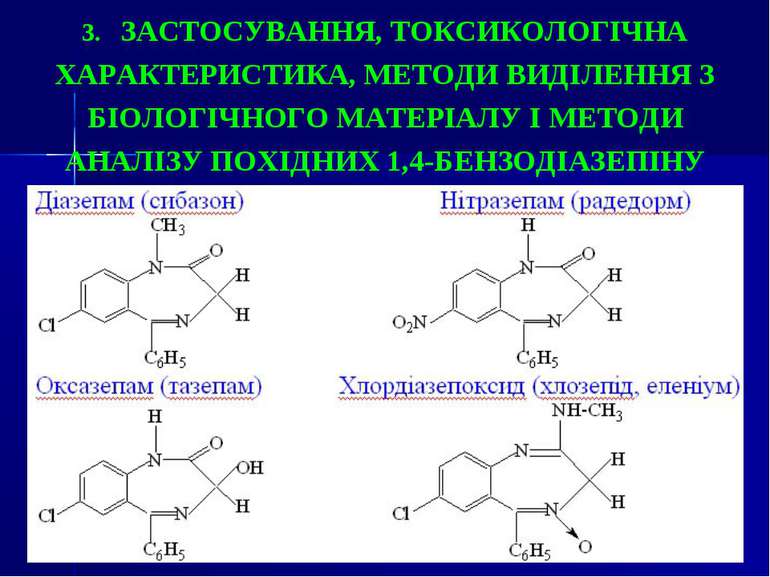
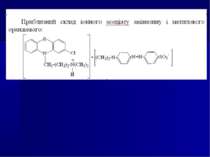
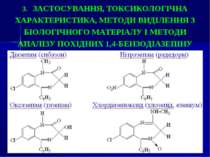
3. ЗАСТОСУВАННЯ, ТОКСИКОЛОГІЧНА ХАРАКТЕРИСТИКА, МЕТОДИ ВИДІЛЕННЯ З БІОЛОГІЧНОГО МАТЕРІАЛУ І МЕТОДИ АНАЛІЗУ ПОХІДНИХ 1,4-БЕНЗОДІАЗЕПІНУ
Токсична дія Вибіркова токсична дія - психотропна, нейротоксична. При вживанні терапевтичних доз можливі ускладнення: розлад травлення, серцево-судинні, нервово-психічні порушення, алергічні реакції. Легкий ступінь отруєння характеризується млявістю, загальмованістю, сонливістю, розширенням зіниць, зниженням м’язового тонусу. При отруєнні середнього ступеня зазначені вище симптоми більш виражені, а також спостерігаються гіперемія обличчя, сухість шкіри, тахікардія. У ряді випадків відзначається ейфорія, м’язева гіпотонія. Важка форма отруєння характеризується плутаною свідоміс тю, появою судом, галюцинації. Смерть настає у зв’язку з дихальною і серцево-судинною недостатністю - судинний колапс, зупинка дихання, набряк легень. Смертельна доза хлордіазепоксиду 1-2 г. Токсична концентрація в крові – 5-20 мг/л, смертельна - понад 50 мг/л.
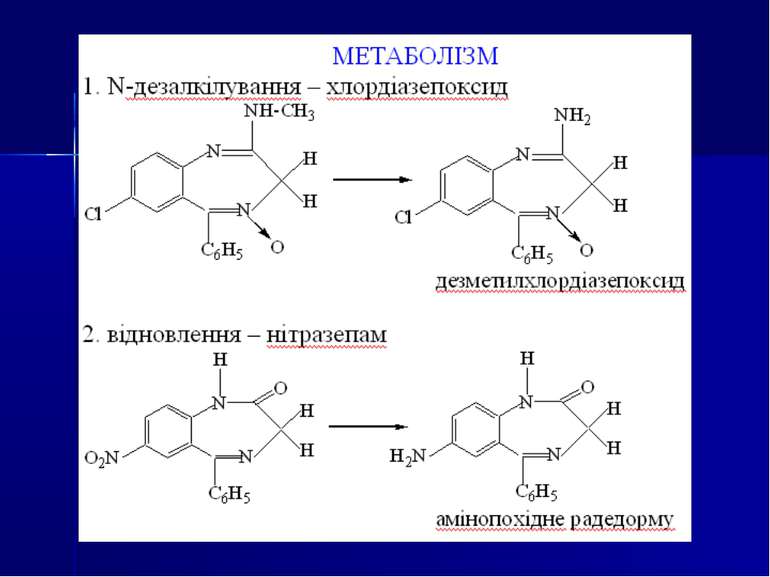
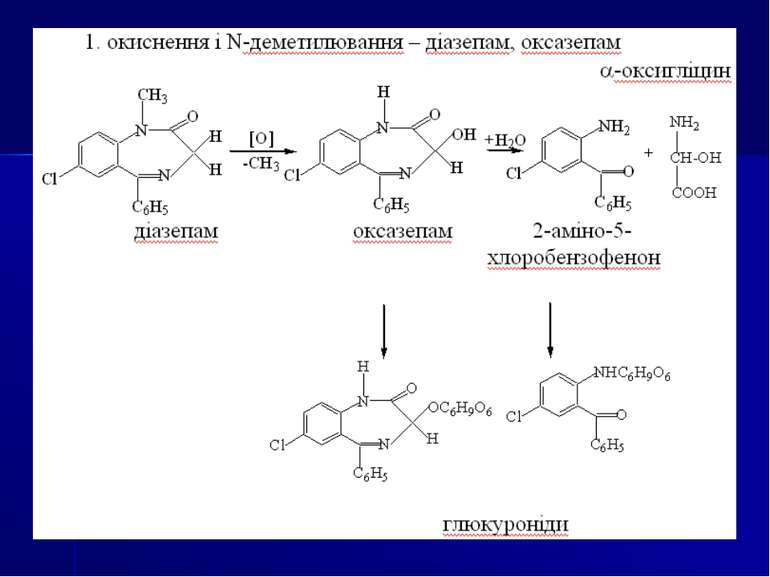
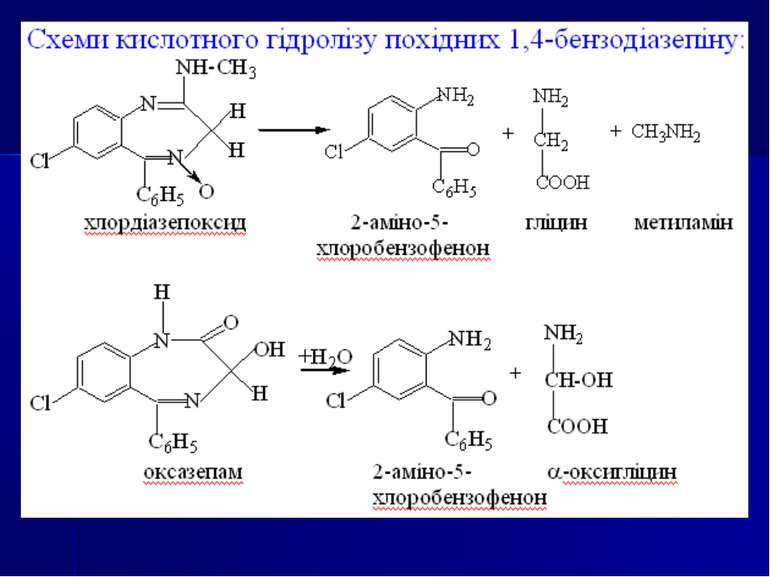
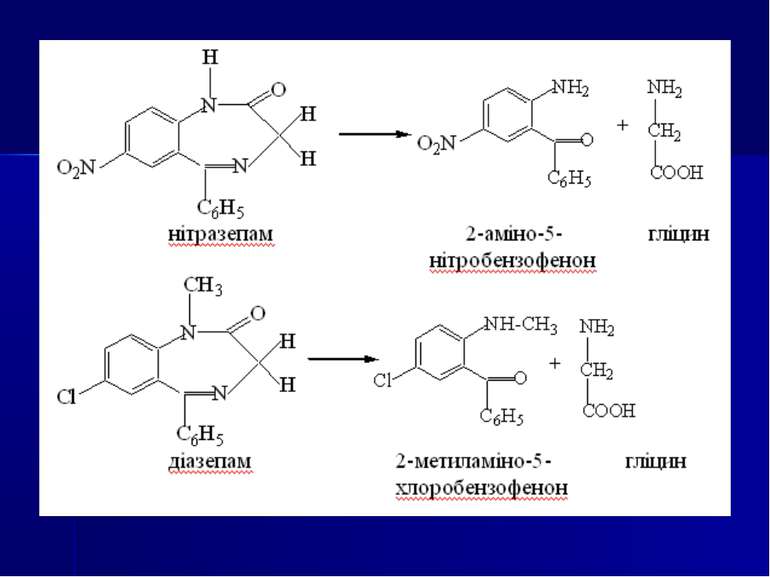
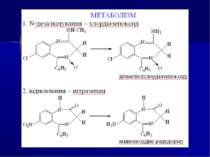
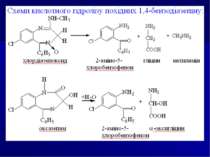
Направлений хіміко-токсикологічний аналіз на похідні 1,4-бензодіазепіну Об’єкти дослідження. Шлунок і тонкий кишечник із вмістом, головний мозок, печінка, нирки, кров, сеча. Аналіз біологічного матеріалу на похідні 1,4-бензодіазепіну та їхні метаболіти виконується за двома напрямками: напрямок І - за продуктами гідролізу - 2-амінобензофенонами (метод Б. М. Ізотова); напрямок II - за вмістом в об’єктах дослідження нативних сполук разом із метаболітами (методи Васильєвої або Стаса-Отто).
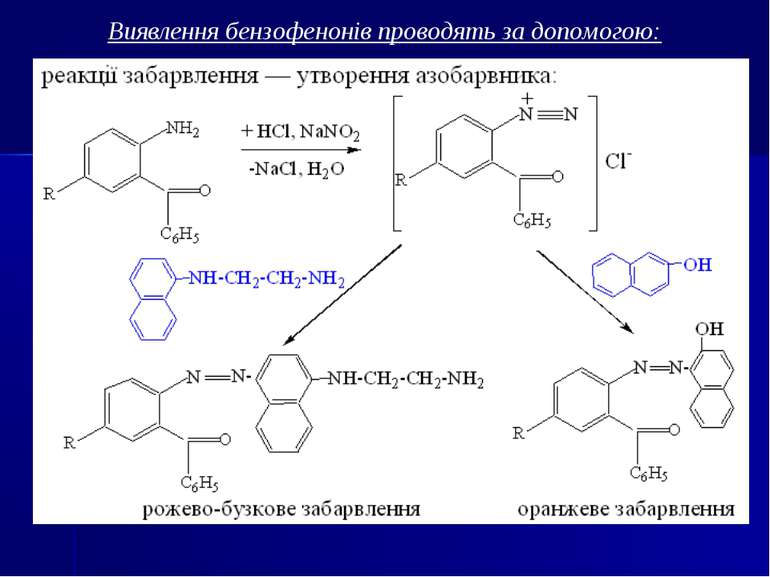
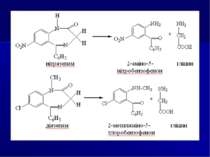
Аналіз безофенонів (І напрямок) ТШХ-скринінг. 1-й етап - у загальній системі розчинників хлороформ-діоксан-ацетон-25%-ий розчин аміаку (45:47,5:5:2,5); сорбент - силікагель КСК. Виявлення бензофенонів проводиться за власним жовтим забарвленням плям; за реакцією утворення азо барвника (2-амінобензофенони) з -нафтолом (оранжеві плями) або з N- -нафтилетилендіаміном (рожево-бузкові плями). Бензофенони (Rf = 0,63-0,70) із сорбенту елююють бензолом. 2-й етап - у окремій системі розчинників хлороформ-ета нол (20:1); сорбент - алюміній оксид; Rf= 0,60-0,63; елюент - бензол.
Кількісний аналіз бензофенонів проводиться фотометричне у видимих межах спектра, в УФ-області спектра, екстракційно-фотометрично, з кислотними барвниками. Хроматографічні методи ГРХ і ВЕРХ застосовуються для ідентифікації і кількісного аналізу продуктів гідролізу похідних 1,4-бензодіазепіну в біологічних витяжках після очистки від домішок.
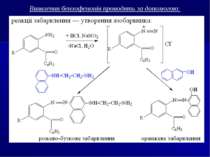
Аналіз за ІІ напрямком Ізолювання проводиться загальними методами. ТШХ-скринінг у загальній системі розчинників (для речовин основного характеру); проявник - реактив Драгендорфа за Муньє (оранжево-коричневі плями з Rf = 0,63-0,77). Речовини елююють розчинниками метанол-25 %-вий розчин аміаку (9:1) і хроматографують у окремій системі розчинників хлороформ-етанол (20:1). Після проявлення плям реактивом Драгендорфа ідентифікують нативні речовини, порівнюючи їх за “свідками”, з подальшим елююванням отрут (елюент метанол-25 %-вий розчин аміаку (9:1)) і проведенням підтверджуючих досліджень.
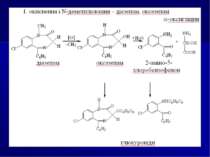
Хімічні методи: 1. Реакції осадження. Похідні 1,4-бензодіазепіну утворюють осади із загальноалкалоїдними осадовими реактивами Драгендорфа, Бушарда, пікриновою кислотою, сіллю Рейнеке та ін. 2. Реакції забарвлення на нативні речовини: Хлордіазепоксид: реактив Маркі (жовте забарвлення), реактив Фреде (оранжеве забарвлення) реактив Віталі-Морена (жовте забарвлення) Діазепам і хлордіазепоксид з нінгідрином дають жовто-коричневе забарвлення. 3. Реакції забарвлення на метаболіти (продукти гідролізу) - 2-амінобензофенони, утворені при гідролізі хлордіазепоксиду, нітразепаму, оксазепаму, дають реакцію утворення азобарвника (за винятком 2-метиламінобензофенону).
4. Фізико-хімічні методи ідентифікації: за УФ- та ІЧ-спектрами, методами ТШХ, ГРХ, ВЕРХ Кількісне визначення проводиться спектральними (УФ-спектрофотометрія, фотоелектроколориметрія, екстракційна фотометрія) і хроматографічними (ТШХ - планіметричний і денситометричний методи; газо-рідинна та рідинна хроматографії) методами.
Схожі презентації
Категорії












































![Звуки [б][б’], позначення їх буквою «бе». Звуко-буквений аналіз слів Звуки [б][б’], позначення їх буквою «бе». Звуко-буквений аналіз слів](/images/1/880/210/img0.jpg)