Презентація на тему:
Масова частка елементів у речовині
Завантажити презентацію
Масова частка елементів у речовині
Завантажити презентаціюПрезентація по слайдам:
Повтоення вивченого: 1)На які два класи поділяються речовини за складом? 2)Які речовини називаються простими? 3)Які речовини називаються складними? 4)Що таке хімічна формула? 5)Що виражає хімічна формула? 6)Що таке відносна атомна маса? 7)Що таке відносна молекулярна маса? 8)Як, знаючи формулу речовини, обчислити відносну молекулярну масу?
Перевірка домашнього завдання: Mr (PbO) = 223; Mr (BaSO4) = 233; Mr (KCl) = 74,5; Mr (AgNO3) = 170.
1)Чи можна стверджувати, що маси кожного атома в молекулі речовини однакові? 2)Співвідношення мас атомів у складі молекули складної речовини постійне чи змінне? 3)Як обчислити співвідношення мас атомів у молекулі? Як можна виразити склад речовини у відсотках? Наприклад: Mr (CaO) = 56 - 100 % Mr (Ca) = 40 - х Виражена у відсотках, ця величина є масовою часткою елемента в складі речовини (ω).
де n - число атомів елемента в молекулі; Ar - відносна атомна маса елемента; Mr - відносна молекулярна маса. Наприклад: Na2O. Ar (Na) = 23. Mr (Na2O) = 62.
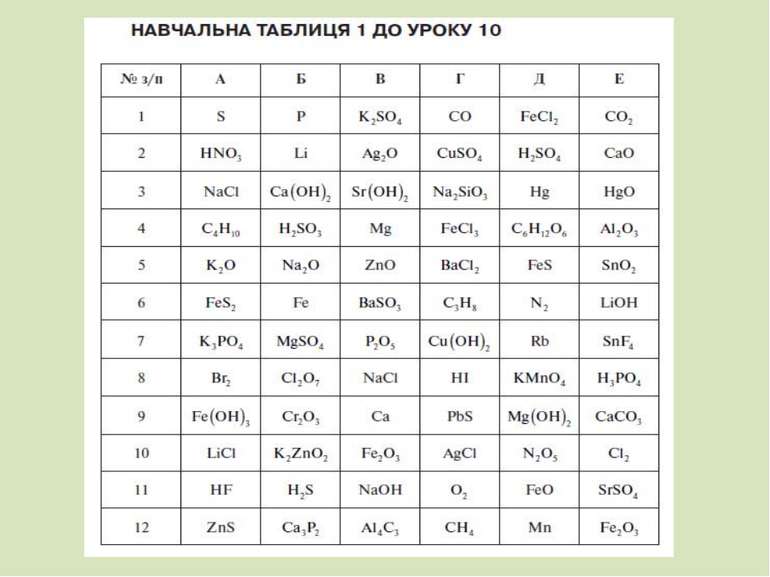
Завдання 1. Обчисліть масові частки елементів у молекулі вуглекислого газу CO2. Завдання 2. Самостійна робота з навчальною таблицею 1 до уроку 10 з перевіркою і коригуванням результатів. Обчисліть масові частки елементів у складних речовинах з ряду 12 у навчальній таблиці: ZnS, Ca3P2, Al4C3, CH4, Fe2O3.
Домашнє завдання Прочитати параграф, відповісти на запитання. Обчислити масові співвідношення елементів і масові частки елементів у молекулах: MgCl2, NaBr, PH3, CrO3.
Схожі презентації
Категорії