Презентація на тему:
Вуглеводи. Глюкоза й сахароза. Будова, властивості, застосування
Завантажити презентацію
Вуглеводи. Глюкоза й сахароза. Будова, властивості, застосування
Завантажити презентаціюПрезентація по слайдам:
Завдання для обговорення 1) З перелічених сполук виберіть ті, що можуть утворюватися в результаті гідролізу жирів: а) одноатомні спирти; б) гліцерин; в) етиленгліколь; г) мурашина кислота; д) пальмітинова кислота.
2) Як зміниться температура плавлення жиру зі збільшенням умісту ненасичених кислот? 3) Масляноізоаміловий естер має запах ананасів. Напишіть формулу цього естеру, запропонуйте спосіб його практичного використання. 4) Напишіть структурні формули двох можливих ізомерів жиру, до складу якого входять один залишок пальмітинової та два залишки стеаринової кислоти.
5) Поясніть, чому після висихання розлитої рослинної олії вона не змивається водою та звичайними мийними засобами. Де використовується ця властивість рослинної олії? 6) Чому жири належать до біологічно активних речовин? 7) Які ще біологічно активні речовини ви знаєте з курсу біології?
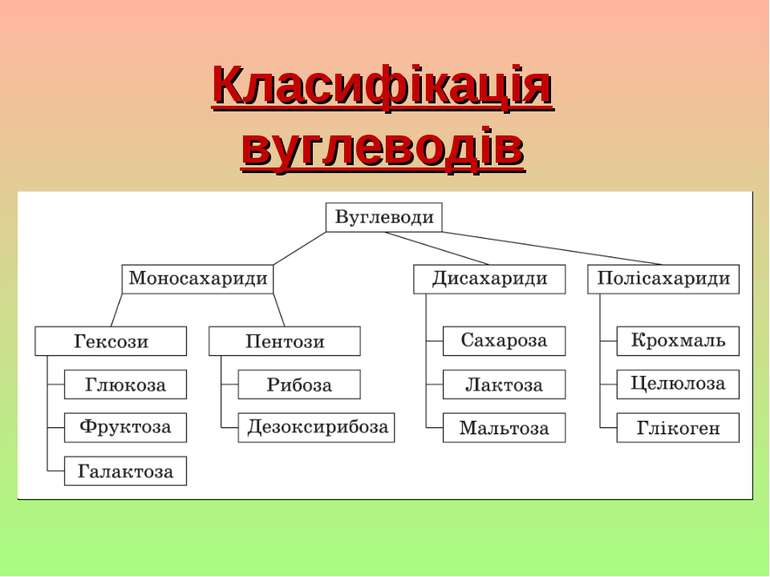
Вуглеводи. Будова, фізичні властивості Вуглеводи — найважливіші природні сполуки, що характеризуються біологічною активністю, відіграють важливу роль у житті рослин, тварин, людини.
У рослинах міститься до 80 % вуглеводів, в організмі тварин і людини — до 20 %. Їжа людини на 70 % складається з вуглеводів.
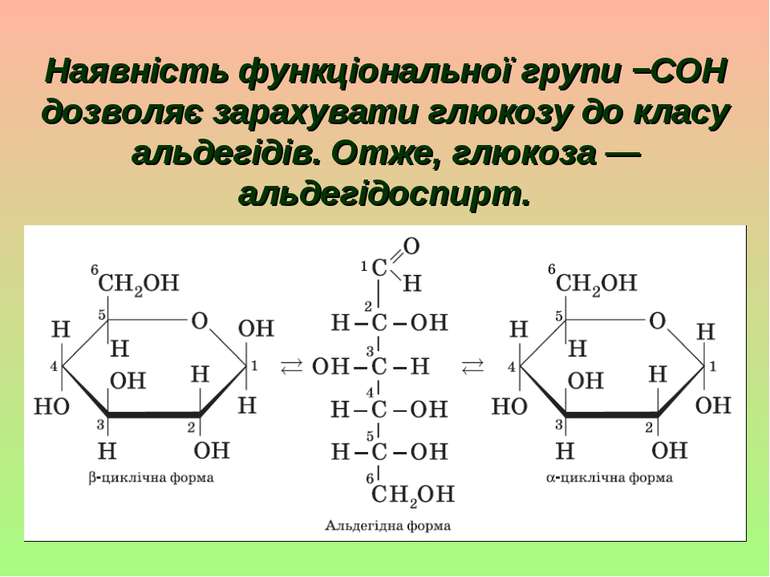
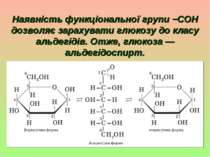
Глюкоза C6H12O6. За своєю будовою глюкоза — складна багатофункціональна сполука, що містить п’ять гідроксильних груп і одну альдегідну групу (−COH):
Наявність функціональної групи −COH дозволяє зарахувати глюкозу до класу альдегідів. Отже, глюкоза — альдегідоспирт.
Глюкоза — цінна поживна речовина. У результаті її окиснення в тканинах вивільняється енергія, необхідна для нормальної життєдіяльності організмів. Реакцію окиснення можна описати сумарним рівнянням: C6H12O6 + 6O2 → 6CO2 + 6H2O
Лабораторний дослід 11. Взаємодія глюкози з купрум(II) гідроксидом Приготуємо купрум(II) гідроксид, додамо до одержаного осаду розчин глюкози. Купрум (I) оксид яскраво-оранжевого кольору. Цю реакцію використовують як якісну реакцію на глюкозу.
Глюкоза завдяки наявності альдегідної групи окиснюється амоніаковим розчином аргентум оксиду (реакція «срібного дзеркала») або купрум (ІІ) гідроксидом (якісні реакції): Як альдегід глюкоза вступає в реакції приєднання (відновлюється):
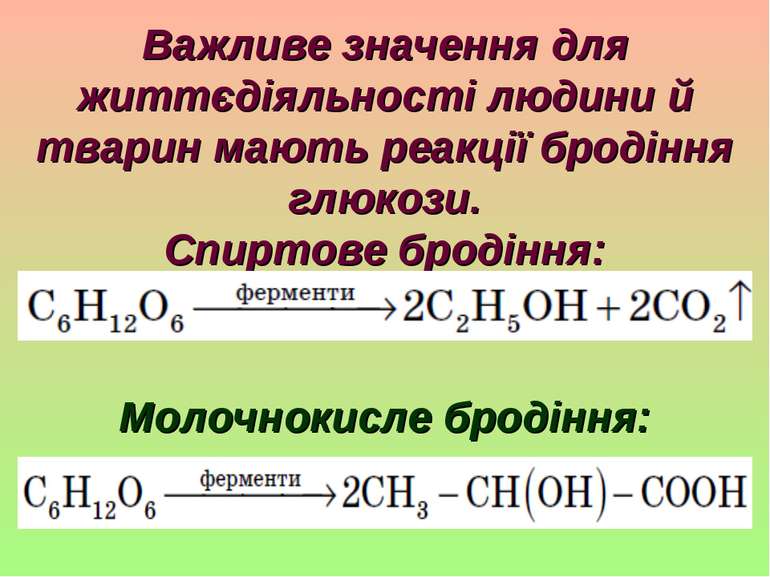
Важливе значення для життєдіяльності людини й тварин мають реакції бродіння глюкози. Спиртове бродіння: Молочнокисле бродіння:
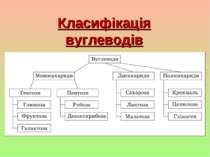
Сахароза — представник дисахаридів, має молекулярну формулу C12H22O11 і являє собою сполучення двох молекул: глюкози та фруктози Її важлива властивість — здатність до гідролізу з утворенням глюкози й фруктози:
Фізичні властивості глюкози й сахарози Білі кристалічні речовини, добре розчинні у воді, мають низькі температури плавлення (tпл(глюкоза) = 146°С, tпл(сахароза) = 186°С (розклад)).
Домашнє завдання Опрацювати матеріал параграфа, відповісти на запитання до нього, виконати вправи. Творче завдання. Підготуйте повідомлення про застосування вуглеводів.
Схожі презентації
Категорії