Презентація на тему:
Амоніак: властивості, використання. Солі амонію. Якісна реакція на йон амонію
Завантажити презентацію
Амоніак: властивості, використання. Солі амонію. Якісна реакція на йон амонію
Завантажити презентаціюПрезентація по слайдам:
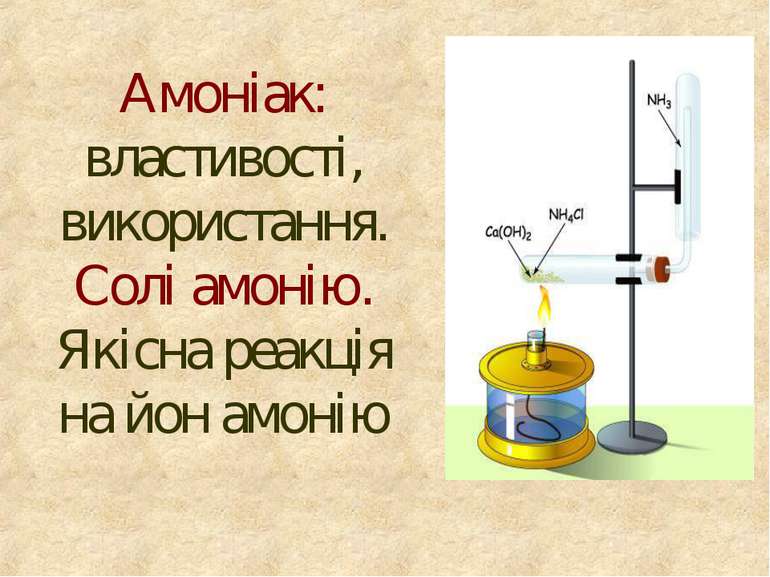
1. Напишіть рівняння одержання амоніаку, укажіть окисник і відновник. 2. Охарактеризуйте цю реакцію, назвіть умови, необхідні для перебігу цієї реакції.
Молекула NH₃ має структуру трикутної піраміди з атомом Нітрогену у вершині. Хімічний зв’язок утворюється шляхом перекривання s-орбіталей трьох атомів
Фізичні властивості: безбарвний газ із різким запахом, добре розчинний у воді (до 700 л амоніаку в 1 л води). Температура плавлення дорівнює –77,7 °С, температура кипіння — –33,4 °С.
У розчині амоніаку індикатори змінюють колір: лакмус — на синій, фенолфталеїн — на малиновий, що вказує на лужне середовище розчину амоніаку.
Запишіть рівняння взаємодії амоніаку із сульфатною кислотою в молекулярній та йонній формах: А) Б)
Поясніть механізм утворення йона амонію у реакціях. Варіант І: розчинення амоніаку у воді. Варіант ІІ: взаємодія амоніаку з хлоридною кислотою.
Домашнє завдання Опрацювати матеріал параграфа, відповісти на запитання до нього, виконати вправи.
Схожі презентації
Категорії