Презентація на тему:
Патогенні клостридії.
Завантажити презентацію
Патогенні клостридії.
Завантажити презентаціюПрезентація по слайдам:
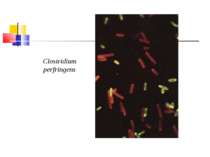
Патогенні клостридії. Кафедра медичної біології, мікробіології, вірусології та імунології Лектор ст. викладач Малярчук Г.Р.
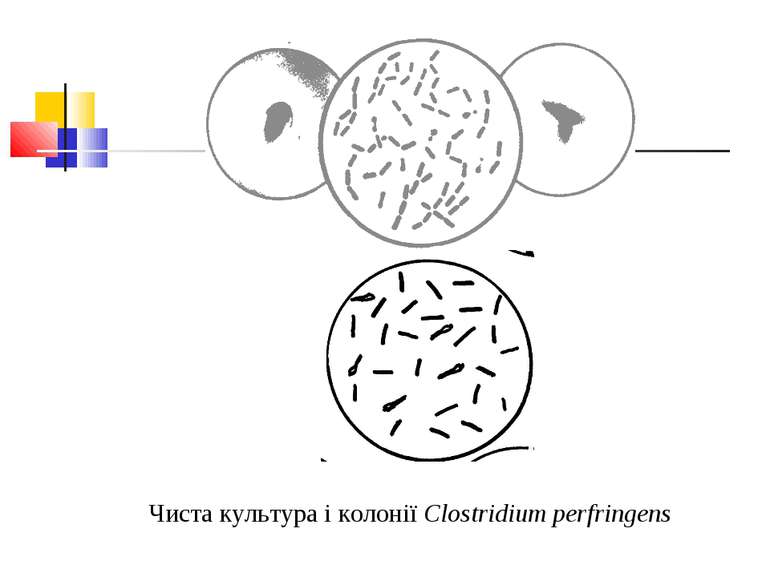
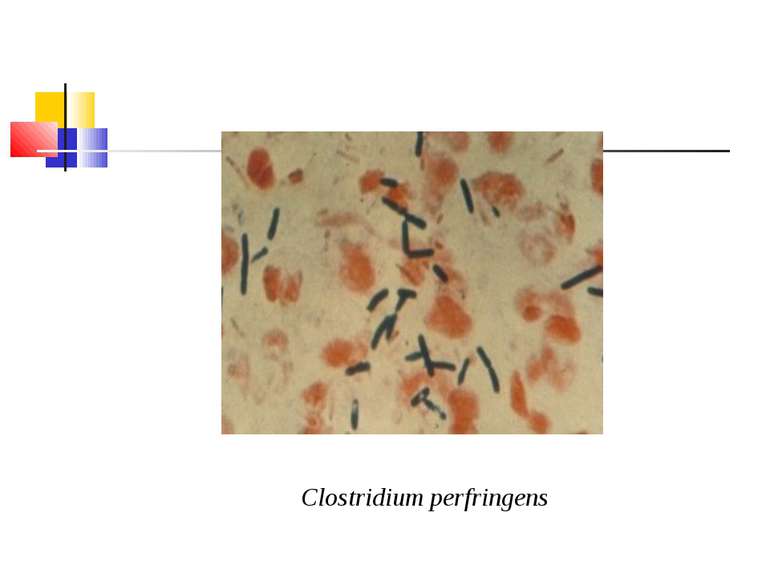
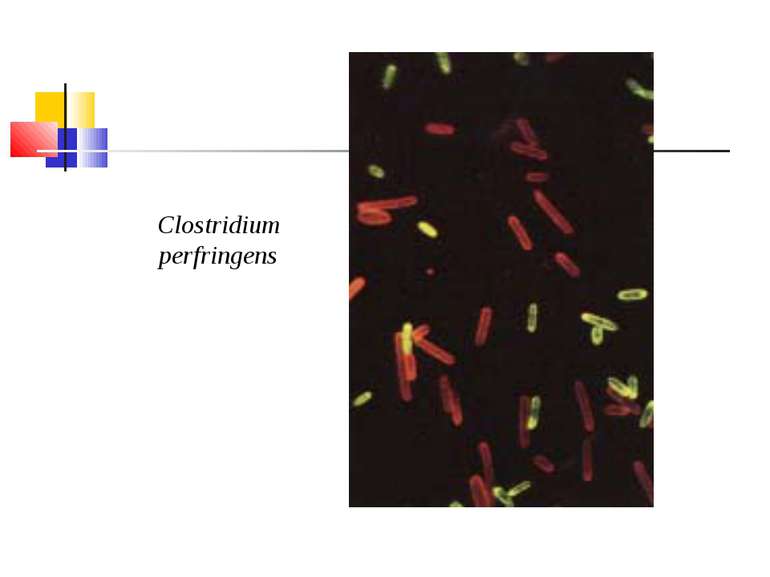
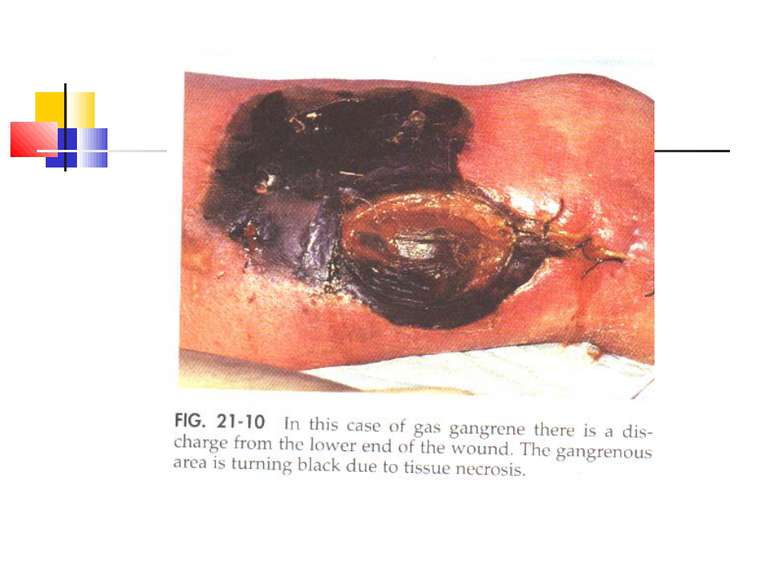
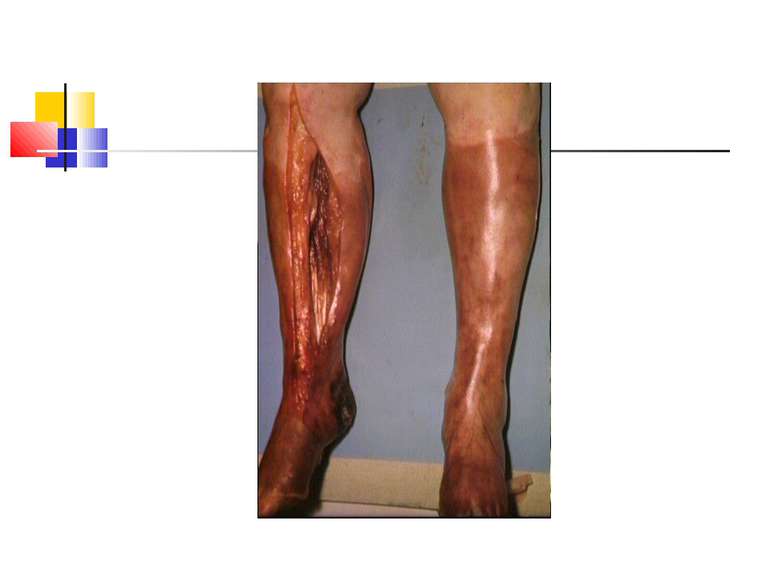
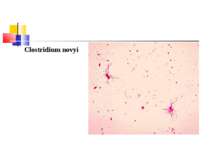
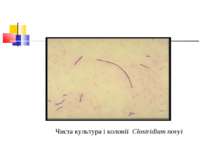
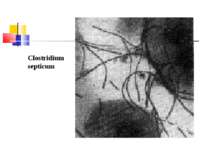
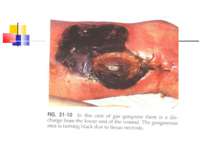
Газова гангрена (анаеробна інфекція) або злоякісний набряк - захворювання, яке викликається патогенними клостридіями (C. perfringens, C. novyi (oedematiens), C. septicum, C. histolyticum, C. bifermentans, C. ramnosum, C. sporogenes, С. sordellii, C. fallax), які мешкають у грунті і попадають в рану із зовнішнього середовища з чужорідними тілами - кулями, осколками, кусочками одягу, занозами тощо.
Мікроорганізми, що викликають газову анаеробну інфекцію, входять до 18 групи Визначника Берджі “Грампозитивні палички і коки, що утворюють ендоспори” і роду Clostridium.
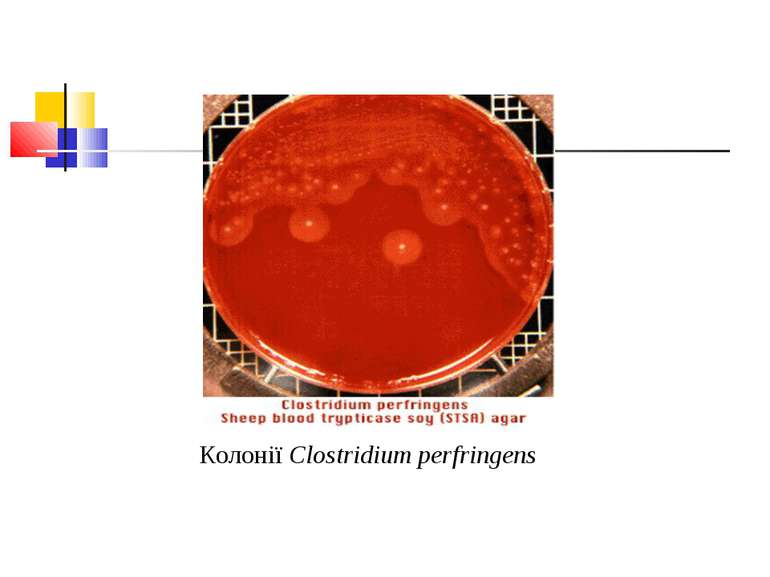
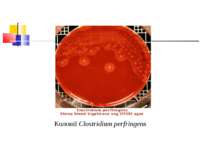
Культивування. Росте у всіх живильних середовищах, на кровяному МПА утворює гладенькі дископодібні колонії сірого кольору з рівними краями і підвищенням у центрі. Ферментативні властивості. Ферментує всі вуглеводи, крім маніту і саліцину. Утворює протеїназу, колагеназу, гіалуронідазу, нейрамінідазу, ДНК-зу. Антигенна структура. С. perf. Має шість сероварів: А, В, С, В, E, F. які різняться між собою серологічно і специфічністю своїх токсинів.
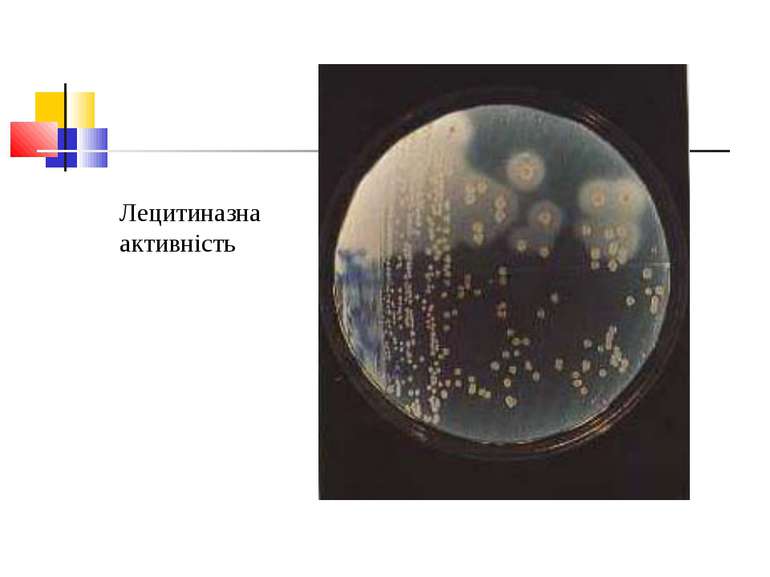
Токсиноутворення збудників Назва ток-сину і фер-менту Активність токсинів і ферментів Типи C. perfringens A B C D E F (альфа) Лецитиназа С, летальний, некротичний, гемолітичний фактор +++ + + + + + (бета) Летальний, некротичний фактор - +++ +++ - - +++ (гамма) Летальний фатор - + + - - + (дельта) Гемолітичний, летальний фактор - + ++ - - - (епсілон) Летальний, некротичний протоксин, який активується трипсином - ++ - +++ - -
Отже, всі 6 типів C. perfringens здатні викликати захворювання у людини і тварин у тому випадку, якщо збудник продукує лецитиназу.
Патогенез Для розвитку збудників анаеробної інфекції, що проникли в організм, потрібні некроз або ушкодження тканин.Надалі некроз здорової тканини спричиняють патогенні анаероби.Цей процес особливо активно розвиваеться в мязовій тканині.Перша фаза інфекційного процесу характеризується утворенням набряку, друга – гангреною мязової і солучної тканин. Імунітет. Після перенесеногозахворювання розвиваеться нестійкий і недовготривалий імунітет.
C. histolyticum Мікроорганізми були вперше виділені у 1916 р. М. Вайнбергом і Е. Сегеном. Це невеличкі грампозитивні рухомі (перитрихи) палички довжиною 3-8 мкм і шириною 0,5-0,8 мкм, здатні до утворення овальних субтермінально розміщених спор.
Особливістю C. histilyticum полягає у тому, що цей мікроорганізм не ферментує жоден з цукрів, проте в той же час має сильні протеолітичні властивості, розкладаючи желатину і згорнуту сироватку. Кусочки мяса, які кладуть у рідке поживне середовище з культурою, яка інтенсивно росте, швидко протеолізуються. Індол при цьому не утворюється, а сірководень виділяється у великій кількості. Основний летальний і некротичний фактор - -токсин відносно стійкий до прогрівання при температурі 60 С і може тривалий час зберігати свої властивості. -антиген, або колагеназа, руйнує нативний і денатурований колаген, желатину, азокол. З відомих бактеріальних колагеназ він найактивніший фермент, має високу специфічність. Препарати очищеної колагенази при внутрішньовенному введенні вбивають мишей. C. histolyticum продукують -антиген, протеїназу, яка активується цистеїном, руйнує желатину, азокол, казеїн, але не діє на колаген.
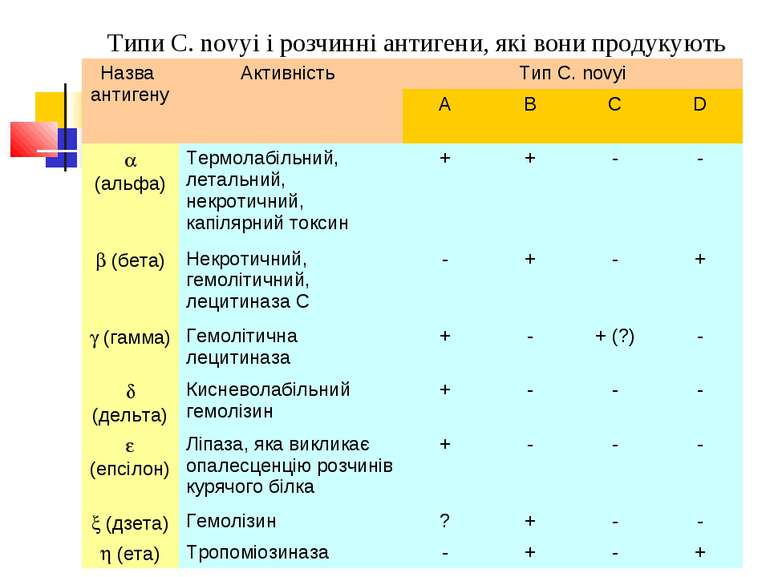
Типи C. novyi і розчинні антигени, які вони продукують Назва антигену Активність Тип C. novyi A B C D (альфа) Термолабільний, летальний, некротичний, капілярний токсин + + - - (бета) Некротичний, гемолітичний, лецитиназа С - + - + (гамма) Гемолітична лецитиназа + - + (?) - (дельта) Кисневолабільний гемолізин + - - - (епсілон) Ліпаза, яка викликає опалесценцію розчинів курячого білка + - - - (дзета) Гемолізин ? + - - (ета) Тропоміозиназа - + - +
Лабораторна діагностика Необхідно також прийняти до уваги факт, що інкубаційний період газової гангрени триває від декількох годин до 2-5 діб, тобто такий час необхідний для досить складного бактеріологічного аналізу. Тому дослідження на патогенні анаероби слід проводити не у всіх випадках поранень, а тільки за клінічними показами. Метою бактеріологічного дослідження є підтвердження клінічного діагнозу газової гангрени. Результати бактеріологічного діагнозу можуть мати значення для своєчасного вибору засобів антитоксичної терапії, а також для лікування антибіотиками. Як матеріал для дослідження збирають виділення з рани, набрякову рідину, кусочки змертвілих тканин, кістки, перев язочний матеріал, а також кров з вени (5-10 мл) тощо.
Лікування і профілактика . Найсуттєвішим заходом є своєчасна та інтенсивна хірургічна обробка ураженої зони, видалення всіх пошкоджених і некротизованих тканин, в яких мікроби легко розмножуються. У важких випадках роблять ампутації кінцівок без джгута і накладання швів. Рану обробляють розчинам хімічних антисептиків-окислювачів - перманганат калію, перекис водню. Одночасно починають застосування протимікробних препаратів, особливо пеніциліну, аміноглікозидів, групи тетрацикліну. Корисною гіпербарична оксигенація, вважають, що вона сприяє швидкій детоксикації організму. Однак вона не може замінити основних принципів хірургічного лікування анаеробної спороутворюючої інфекції. Специфічне лікування починають відразу. Під час операції під наркозом внутрішньовенно крапельно повільно (1мл хв) вводять лікувальну дозу антитоксичної очищеної або концентрованої сироватки “Діаферм” (150 000 МО - по 50 000 МО сироватки проти трьох основних збудників - C. perfringens, C. novyi, C. septicum; за 1 міжнародну одиницю активності сироватки приймають її найменшу кількість, яка нейтралізує 100 Dlm токсину для білих мишей вагою 15-18 г). Одночасно внутрішньом язово вводять п ять профілактичних доз сироватки. При встановленні збудника газової анаеробної інфекції вводять відповідну гомологічну сироватку з попередньою пробою на індивідуальну чутливість до чужерідного білку.
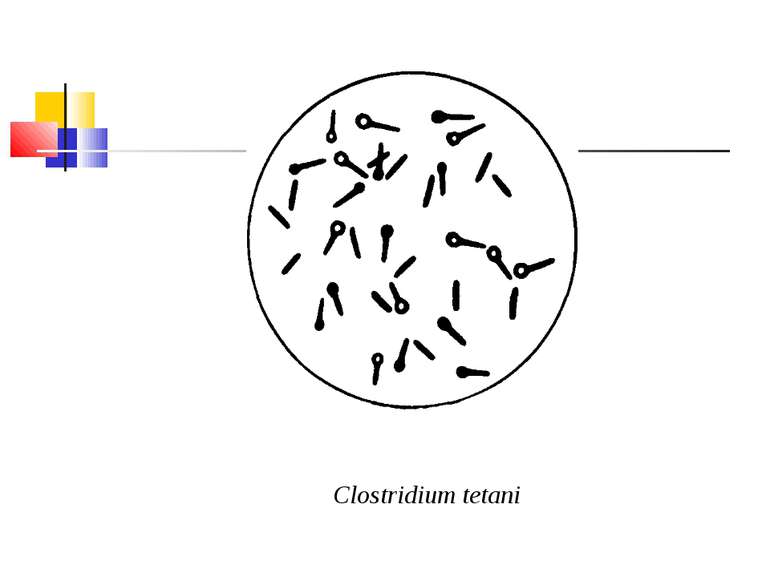
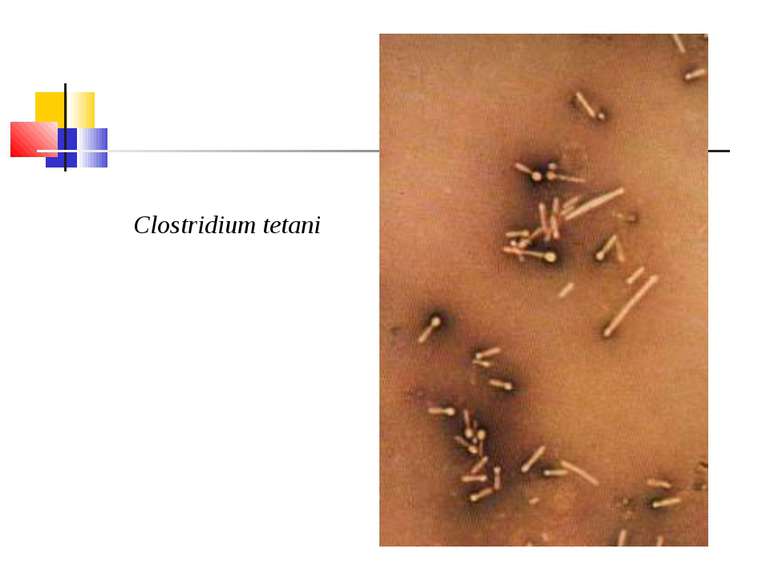
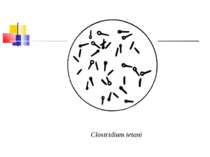
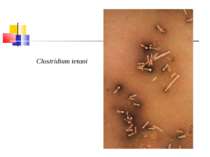
Збудник правця (Clostridium tetani) Правцева паличка вперше описана М.Д. Монастирським (1883) та А. Ніколаєром (1884), чисту культуру виділив С. Кітазато в 1889 р. C. tetani (tetanos - судоми, заціпеніння) - тонка, довга, рухлива, безкапсульна грампозитивна паличка з термінально розташованою круглою спорою, що надає їй характерного вигляду барабанної палички.
КУЛЬТИВУВАННЯ Клостридії правця - дуже строгі анаероби. На середовищі Кітта-Тароцці вони ростуть у вигляді легкого помутніння без виділення газу, на дні пробірки поступово виникає осад. На цукрово-кров’яному агарі утворюють колонії з компактним центром і ниткоподібними відростками, що химерно переплітаються (колонії-павучки). Іноді ростуть у вигляді круглих колоній із зонами гемолізу.
Паличка правця продукує надзвичайно сильний екзотоксин, який часто називають тетанотоксином. Він має дві фракції: тетаноспазмін, який викликає ураження рухових центрів нервової системи й спричиняє спастичне скорочення м’язів, і тетанолізин, який лізує еритроцити.
Правець у миші За 1 DLM приймають ту найменшу його дозу, яка при внутрішньовенному введенні білій миші викликає її загибель. Ця доза може дорівнювати 0,000001-0,000005 мл.
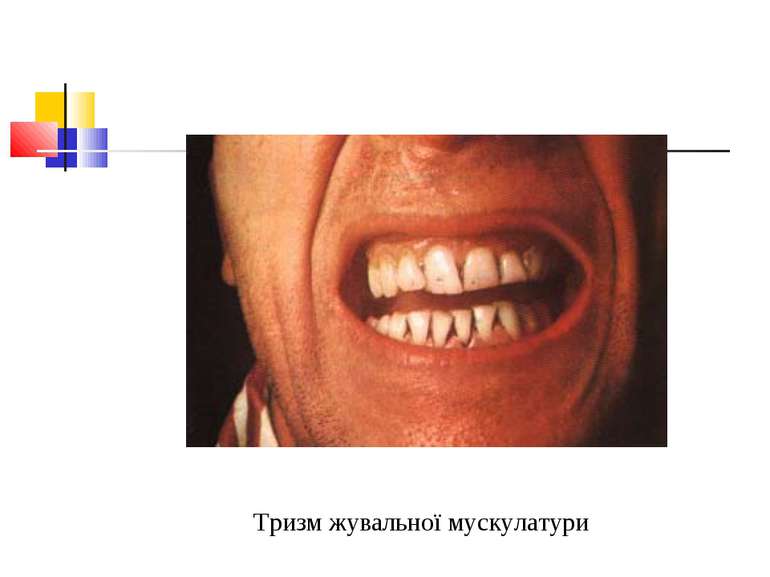
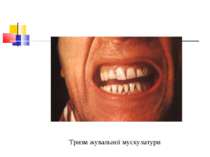
Захворювання людини Основна умова виникнення правця - наявність рани й інфікування її спорами правцевих паличок. Інкубаційний період триває від 4 до 30 днів і довше. У рані спори клостридій перетворюються у вегетативні форми. Вони виробляють екзотоксин, який викликає всі клінічні симптоми хвороби. Процес починається судомними скороченнями м’язів у місці вхідних воріт, потім скорочуються жувальні і потиличні м’язи, мімічна мускулатура обличчя, від чого на ньому з’являється одночасно гримаса болю й посмішка (risus sardonicus).
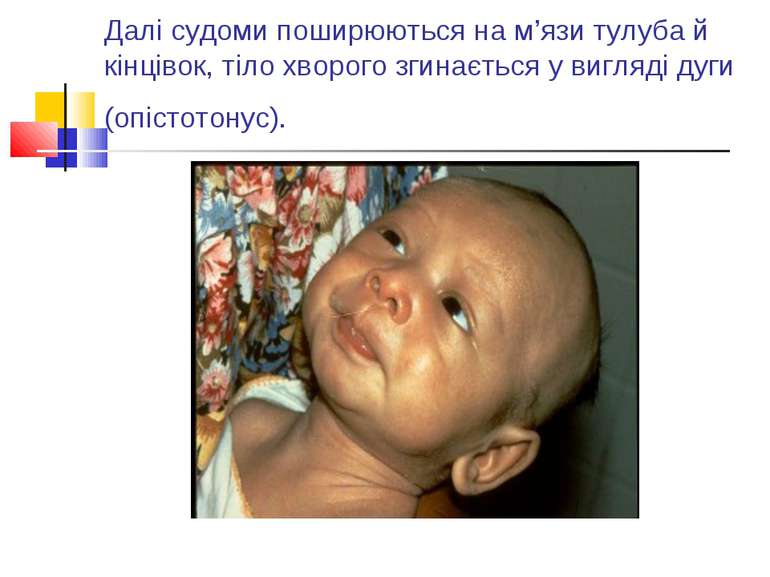
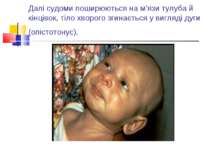
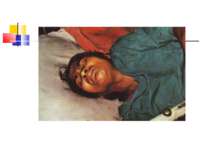
Далі судоми поширюються на м’язи тулуба й кінцівок, тіло хворого згинається у вигляді дуги (опістотонус).
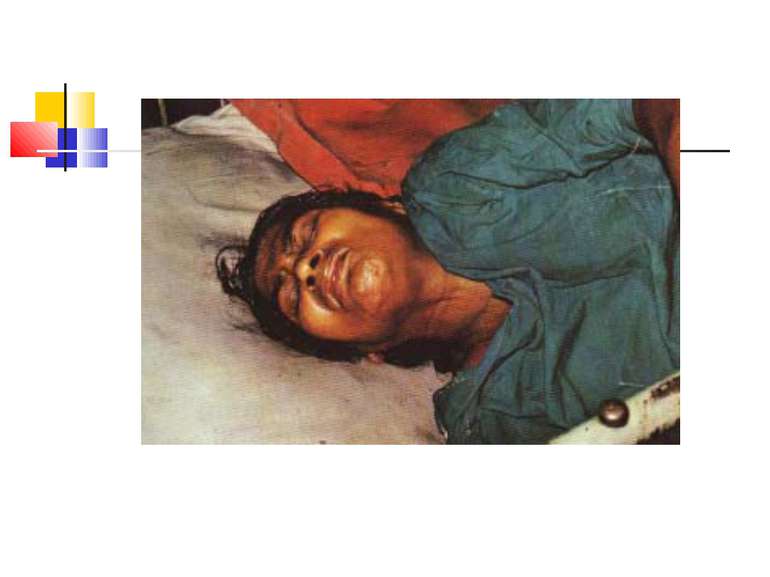
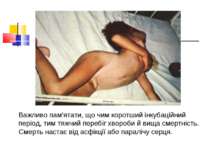
Важливо пам’ятати, що чим коротший інкубаційний період, тим тяжчий перебіг хвороби й вища смертність. Смерть настає від асфікції або паралічу серця.
Діагностика Діагноз правця лікар встановлює на основі характерних клінічних симптомів. Мікробіологічне дослідження з діагностичною метою проводять не часто. Здебільшого його використовують для вия-влення спор у грунті, перев’язних матеріалах, ліках парентерального введення. При дослідженні ранового вмісту після бактеріоскопії його сіють на середовище Кітта-Тароцці. Через 3-7 діб визначають наявність токсину в біопробах на білих мишах. Для цього двом тваринам вводять по 0,5-1 мл фільтрату культури і ще двом - такі ж дози фільтрату, нейтралізованого протиправце-вою антитоксичною сироваткою протягом 40 хв. При наявності тетанотоксину перші дві миші гинуть, а інші залишаються живими.
Профілактика і лікування З метою попередження виникнення правця в поранених після первинної хірургічної обробки рани вводять за методом Безредки 3000 МО антиправцевої сироватки внутрішньом’язово. Специфічну профілактику проводять шляхом активної імунізації дорослих правцевим анатоксином або коклюшно-дифтерійно-правцевою вакциною в дітей, починаючи з 3 місяців до 12 років. Вакцинують також усіх військовослужбовців, працівників залізничного транспорту, механізаторів сільського господарства, будівельників, лісозаготівників. При пораненні нещеплених осіб необхідно проводити активно-пасивну імунізацію: вводять підшкірно 0,5 мл правцевого анатоксину і внутрішньом’язово 3000 МО протиправцевої сироватки або 3 мл протиправцевого імуноглобуліну. Специфічне лікування проводять внутрішньом’язовим введенням 100000-150000 МО протиправцевої антиток-сичної сироватки. Кращі результати отримують при ін’єкціях протиправцевого людського імуноглобуліну, який вводять дозою 6 мл (900 МО).
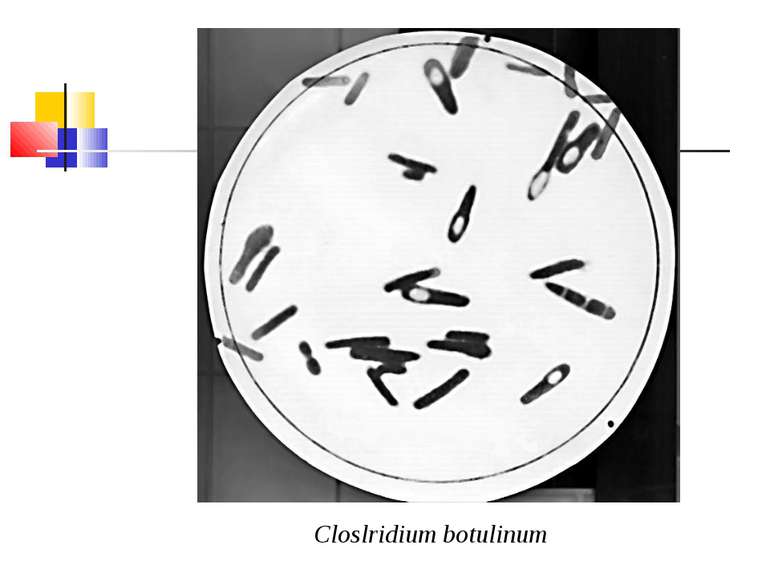
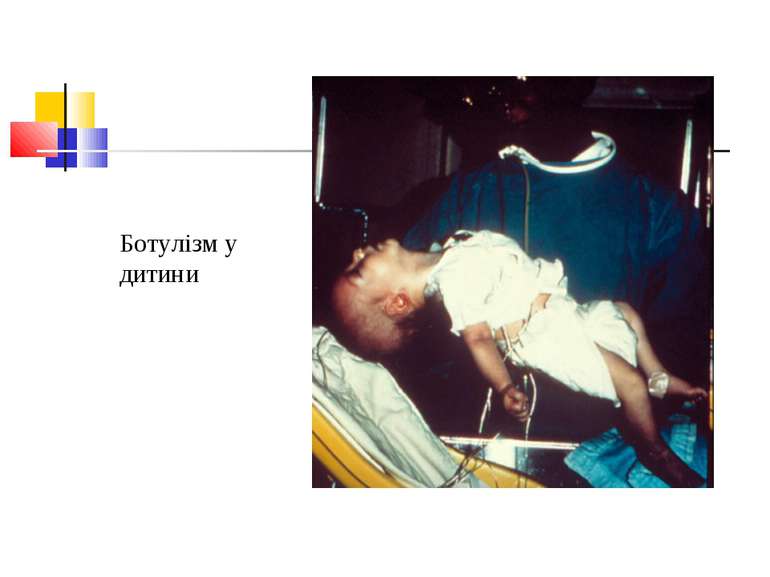
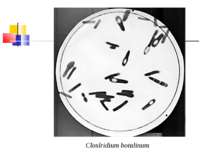
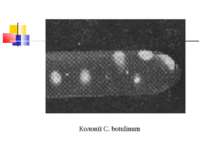
Збудник ботулізму (Clostridium botulinum) Ботулізм (botulus - ковбаса) - тяжка інтоксикація, яка виникає від вживання в їжу продуктів, отруєних токсинами С. botulinum, і характеризується ураженням центральної й вегетативної нервових систем. Збудник захворювання виділив Е. ван Ерменгем у 1896 р. з шинки, яка стала причиною масового отруєння, і з селезінки померлих від ботулізму. C. botulinum - велика грампозитивна паличка завдовжки 4-10 мкм і завширшки 0,6-1,5 мкм з округленими кінцями й перитрихіально розташованими джгутиками
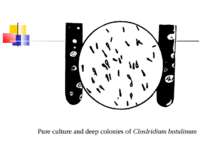
Культивування Клостридії ботулізму - строгі анаероби, невибагливі до живильних середовищ, оптимальна температура росту для різних сероварів коливається від 25 до 40 °С. На середовищі Кітта-Тароцці утворюють каламуть та осад на дні, мають гострий запах згірклого масла. На цукрово-кров’я-ному агарі виростають неправильної форми колонії з фестончастими краями або ниткоподібними відростками із зонами гемолізу навколо них.
Вегетативні форми збудників ботулізму мало стійкі до дії різних факторів нашого довкілля. Вони гинуть при нагріванні до 80 °С через 30 хв. Спорові форми дуже резистентні, насамперед до дії високої температури - окремі серовари (А, В, С, F) витримують кип’ятіння протягом 1-6 годин.
Збудник ботулізму має сім серологічних варіантів: А, В, С (С1, С2), D, E, F, G, які відрізняються за характером продукованих ними токсинів. Токсин кожного серовару нейтралізується тільки гомологічною сироваткою. Найбільше значення в патології людини мають серовари А, В, С, Е. Усі серовари паличок ботулізму виробляють екзотоксин, який є найсильнішою отрутою біологічного походження.
Виділення токсину відбувається в анаеробних умовах як у культурах на середовищах, так і в харчових продуктах, особливо в м’ясних, рибних та овочевих. На відміну від правцевого екзотоксину ботулотоксин стійкий до дії ферментів кишкового тракту та всмоктується в кров незміненим. Тепер отримані очищені екзотоксини окремих сероварів, в 1 мг яких міститься від 10 до 100 млн DLM для білих мишей. Ботулотоксин має нейротропну дію. Найбільш чутливі до нього коні, кролі, гвінейські свинки, кури. Дуже чутлива до нього людина. У складі ботулінового екзотоксину знайдено ряд отруйних фракцій: нейротоксин, гемотоксин, лейкоцидин, ферменти лецитиназу, гіалуронідазу.
Лабораторна діагностика Для виявлення ботулінового токсину в хворого беруть кров, промивні води шлунка, блювотиння, кал, сечу й залишки підозрілого харчового продукту, в разі смерті - вміст шлунка й кишок, лімфатичні вузли, головний і спинний мозок.
Матеріал від хворого потрібно забирати якнайшвидше, до введення протиботулінової сироватки й антибіотиків. Ботулотоксин визначають за допомогою біологічної проби на білих мишах. Одній групі тварин вводять у черевну порожнину фільтрат досліджуваного матеріалу або витяжки із залишків їжі. Другій - досліджуваний матеріал із полівалентною діагностичною протиботуліновою сироваткою типів А, В, С, Е.
При підозрінні на захворювання ботулізмом після промивання шлунка необхідно негайно ввести антитоксичну протиботулінову сироватку типів А, В, С, Е, а після визначення типу токсину перейти на введення гомологічної сироватки. Сироватку типів А, С і Е вводять по 10000 МО, типу В - 5000 МО за методом Безредки 4-6 разів на добу протягом 2-4 днів. Сироватка - єдиний препарат, який може врятувати життя хворого.
Профілактика і лікування Усім людям, які споживали продукти, що послужили причиною отруєння хоча б однієї людини, вводять із профілактичною метою по 1000-2000 МО протибутулінової сироватки типів A,B,C і E. Для активної імунізації людей вживають полівалентний ботуліновий анатоксин. При підозрінні на захворювання ботулізмом після промивання шлунка необхідно негайно ввести антитоксичну протиботулінову сироватку типів А, В, С, Е, а після визначення типу токсину перейти на введення гомологічної сироватки. Сироватку типів А, С і Е вводять по 10000 МО, типу В - 5000 МО за методом Безредки 4-6 разів на добу протягом 2-4 днів. Сироватка - єдиний препарат, який може врятувати життя хворого.
Патогенні спірохети Серед патогенних представників порядку Spirochaetales найбільше значення мають три роди - Treponema, Borrelia, Leptospira. Це тонкі, довгі, звивисті, рухомі мікроорганізми, які відрізняються між собою розмірами, амплітудою, глибиною спіралі, кількістю завитків, різним забарвленням. За методом Романовського-Гімзи краще забарвлюються борелії, гірше лептоспіри і дуже слабо - трепонеми. У живому стані всі спірохети можна виявити в темному полі зору.
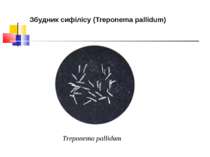
Морфологія і фізіологія. Трепонеми сифілісу - тонкі спіралеподібні бактерії довжиною 10-15 мкм і шириною 0,1-0,2 мкм. Вони мають 8-14 рівномірних завитків, тришарову зовнішню мембрану. У середині цитоплазми розшаровані нуклеоїд, мезосоми, рибосоми, фібрили і базальні тіла, видимі лише під електронним мікроскопом. Розмножуються шляхом поперечного поділу. Можуть утворювати шароподібні цистоподібні форми, покриті міцною муциноподібною оболонкою, і L-форми. Погано фарбуються аніліновими барвниками, тому називаються блідими трепонемами, грамнегативні. При забарвленні за Романовським-Гімзою набувають блідо-рожевого кольору. Спор не утворюють, джгутиків не мають, але активно рухливі. Для трепонем властиві поступальні, обертові, згинальні й хвилеподібні рухи.
Культуральні властивості Трепонеми сифілісу дуже вибагливі до живильних середовищ. Із великими труднощами їх вдається виростити в анаеробних умовах на середовищах із мозковою тканиною або на хоріоналантоїсній оболонці курячого зародка. Але всі культури, вирощені штучно в лабораторії, втрачають патогенні властивості, тому одержали назву культуральних трепонем.
Антигенна структура Антигенна структура їх складна. Виявлені протеїнові, ліпідні й полісахаридні комплекси, але серологічних варіантів немає. Екзотоксину спірохети сифілісу не продукують, містять у цитоплазмі ендотоксин. Бліда трепонема для лабораторних тварин малопатогенна. Чутливі лише мавпи. І.І. Мечніков і Д.К. Заболотний відтворили на них захворювання, подібне за клінічною картиною до сифілісу людини. Краще всього розмножувати трепонем у паренхімі яєчка кролика, що дозволяє завжди мати їх при проведенні лабораторної діагностики захворювання.
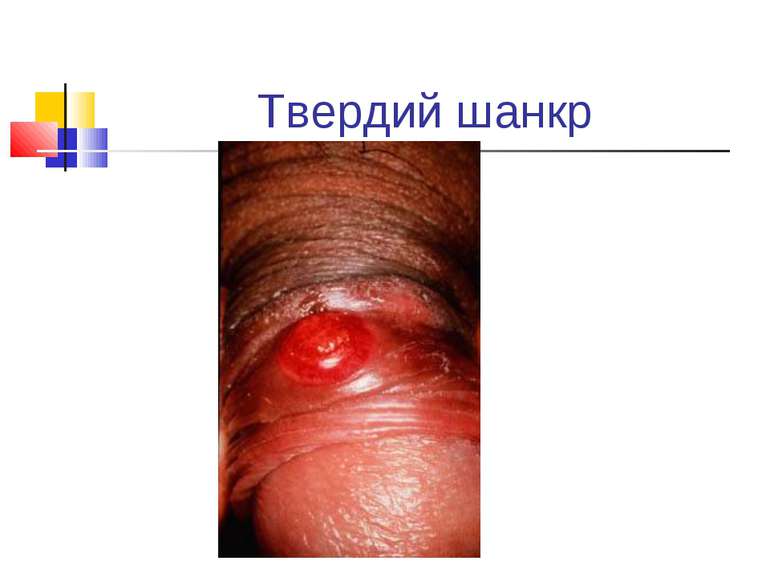
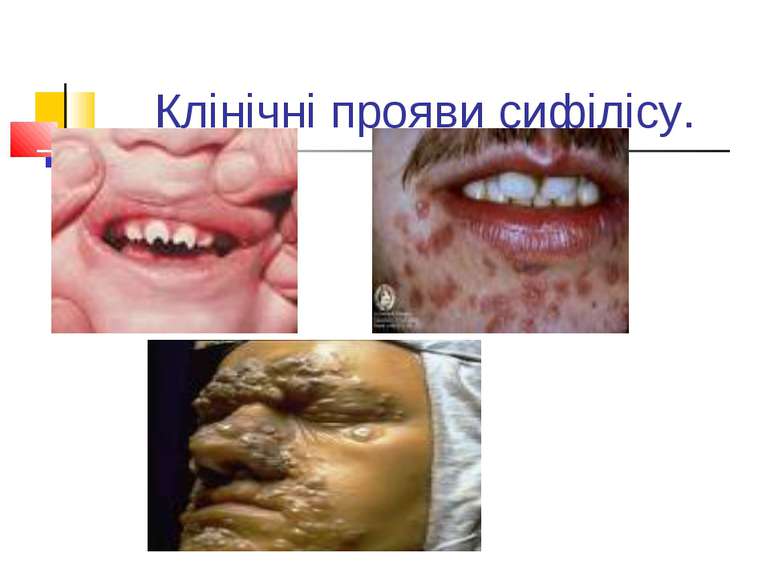
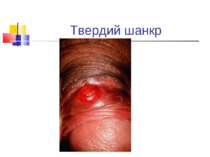
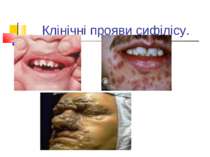
Захворювання людини. Інкубаційний період при сифілісі триває в середньому 20-30 днів. На місці проникнення трепонем виникає первинна сифілома - невелика безболісна виразка з твердим дном (ulcus durum). Регіональні лімфатичні вузли збільшуються і стають твердими. Цей первинний сифіліс триває близько 6 тижнів. Вторинний сифіліс характеризується висипом на шкірі, слизових оболонках, розвитком уражень внутрішніх органів, кісток і триває 2-3 роки. Якщо лікування не проводиться, може настати третинний сифіліс із утворенням у паренхіматозних органах щільних інфільтратів, папул, горбків, гум, які схильні до розпаду. Цей період триває 9-10 років, після чого може виникнути ураження головного, спинного мозку і серцево-судинної системи.
Лабораторна діагностика. Основними методами мікробіологічної діагностики сифілісу є бактеріоскопічний і серологічний. При первинному і вторинному сифілісі матеріалом для мікроскопії служать виділення з виразок, папул, ерозій або пунктат лімфатичних вузлів. Поверхню виразки очищають від нальоту стерильним ватним тампоном, змоченим в ізотонічному розчині хлориду натрію, потім її подразнюють, легко поскрібуючи скальпелем або гострою ложечкою. Рідину відсмоктують пастерівською піпеткою і досліджують у темному полі зору, де чітко видно яскраво освітлені спірохети і характерний рух. Для забарвлення трепонем краплю рідини наносять на предметне скло, виготовляють мазок (як мазок крові), висушують, фіксують метиловим спиртом і декілька годин забарвлюють за Романовським-Гімзою. Бліда спірохета стає блідо-рожевою, а сапрофітні спірохети - голубими. Можна фарбувати трепонеми і за методом сріблення.
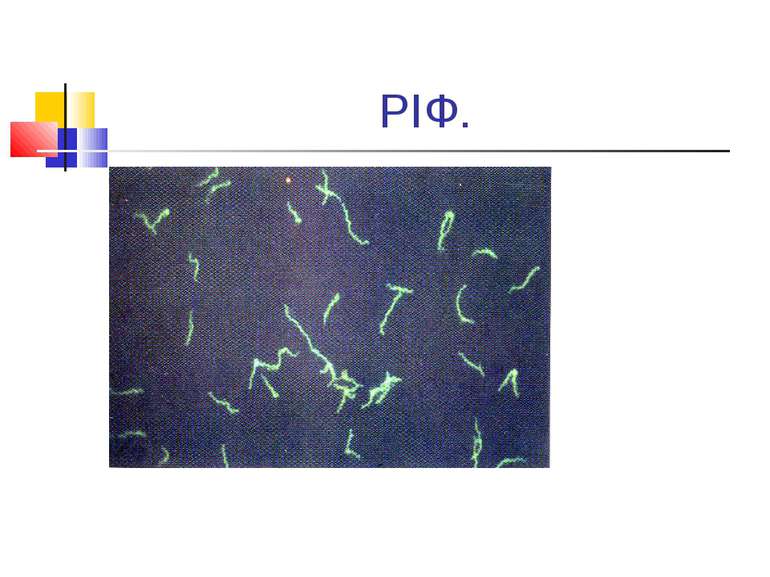
Серологічна діагностика Серологічна діагностика сифілісу грунтується на постановці реакції Вассермана й осадових реакцій Кана і Закса-Вітебського. Методика постановки реакції Вассермана не відрізняється від постановки реакції зв’язування комплементу. Необхідно пам’ятати, що вона може бути негативною протягом трьох тижнів первинного (серонегативного) періоду. Позитивна реакція Вассермана, крім сифілісу, зрідка буває і при інших гострих інфекційних хворобах (бруцельоз, кір, малярія), туберкульозі й лепрі, в пізній період вагітності й після пологів. Для серологічної діагностики сифілісу широко використовують реакцію імобілізації трепонем і непряму реакцію імунофлуоресценсії, які вважаються найбільш специфічними в лабораторній діагностиці захворювання.
Профілактика і лікування. Важливе значення мають рання діагностика, своєчасне лікування хворих і санітарно-освітня робота серед населення. Індивідуальну профілактику проводить середній медичний персонал у шкірно-венеричних диспансерах, стаціонарах і профілактичних пунктах. Для лікування сифілісу використовують антибіотики (пеніцилін, еритроміцин, тетрациклін тощо) і препарати вісмуту (бійохінол, бісмоверол, пентабісмол), відповідно до розроблених інструкцій.
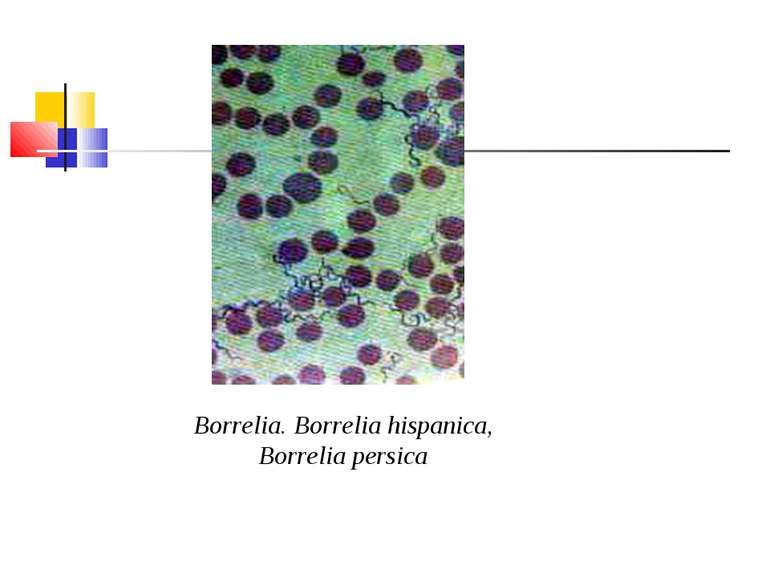
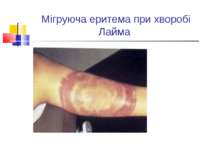
Збудники поворотних тифів і бореліозів Розрізняють епідемічний поворотний (вошивий) і ендемічний поворотний (кліщовий) тифи. Збудником першого з них є відкрита в 1868 р. О. Обермейєром Borrelia recurrentis. Кліщовий поворотний тиф спричиняється близько 20 різновидами борелій, розповсюджених у певних географічних регіонах, де вегетують відповідні види кліщів. У нашій країні захворювання викликають переважно B. caucasica i B. lathyshewi.
Морфологія і фізіологія. B. recurrentis - тонкі спіралеподібні мікроорганізми завдовжки 20-40 мкм і завширшки 0,3-0,6 мкм, мають від 3 до 8 великих нерівномірних завитків, кінці їх трохи загострені. За Грамом забарвлюються в червоний колір, за Романовським-Гімзою - в синьо-фіолетовий. Спірохети поворотного тифу мають енергійну і різноманітну рухливість. Морфологічно борелії вошивого і кліщового поворотного тифу не відрізняються між собою. Борелії культивують в анаеробних умовах на рідких живильних середовищах, до яких додають сироватку і шматочки тканин або органів. Ріст виявляють через 3-6 днів при виготовленні висячої краплі й мікроскопії в темному полі. Можливе успішне культивування борелій і в курячому ембріоні. Розмножуються вони шляхом поперечного поділу.
Антигени. Поверхневі антигени борелій легко змінюються з кожним наступним гарячковим приступом, але серологічні їх варіанти в лабораторії не визначають. Екзотоксинів борелії не виділяють, містять ендотоксини, які зумовлюють ураження центральної нервової системи, гарячку, явища інтоксикації організму.
Захворювання людини. Інфікування людини відбувається при роздавленні заражених вошей під час чухання і втиранні їх гемолімфи разом із бореліями в ранки від укусів або розчіси шкіри. Далі збудник проникає у клітини лімфоїдно-макрофагальної системи, розмножується і потрапляє у кров, зумовлюючи бактеріємію і токсинемію. Це співпадає з появою гарячки й інших симптомів хвороби. Завдяки фагоцитозу і дії антитіл значна маса борелій гине, що призводить до закінчення приступу гарячки. Деяка частина збудників, які збереглися у ЦНС, селезінці, продовжують розмножуватись, одночасно змінюючи свої антигенні властивості. Такі борелії спричиняють новий приступ лихоманки. На них знову виробляються антитіла. Після 4-5 приступів у крові нагромаджуються антитіла проти всіх антигенних варіантів борелій і настає видужання. Захворювання характеризується високою температурою, нудотою, блюванням, збільшеннями печінки, селезінки, ураженням нервової і кровоносної систем. Тепер поворотний вошивий тиф на Україні не зустрічається.
Лабораторна діагностика. Основою мікробіологічної діагностики поворотного тифу є бактеріоскопічне і серологічне дослідження. Для цього під час температурного приступу виготовляють товсту краплю і мазок крові, забарвлюють за Романовським-Гімзою (або фуксином) і мікроскопують. Краплю крові можна досліджувати і в темному полі, спостерігаючи характерний рух спірохет. Для серологічної діагностики інколи ставлять реакцію лізису і РЗК. Із метою диференціації епідемічного й ендемічного поворотного тифу кров’ю хворого заражають гвінейську свинку. Борелії епідемічного поворотного тифу захворювання тварин не викликають.
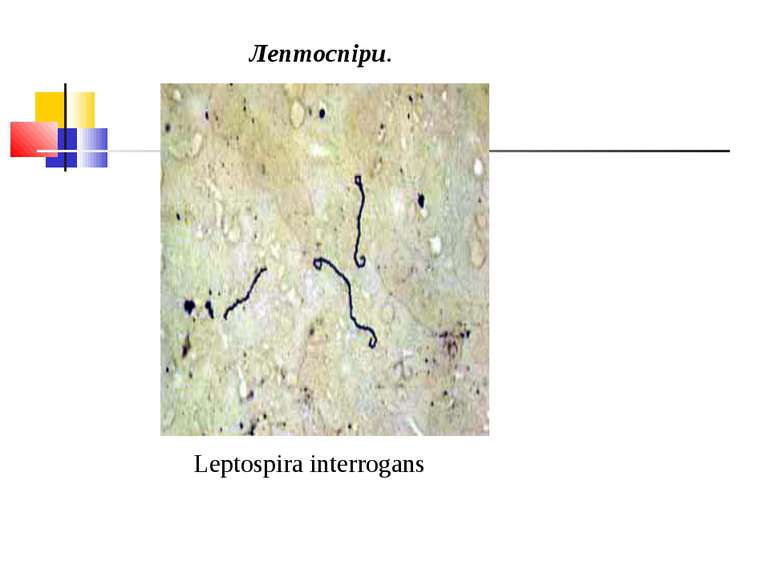
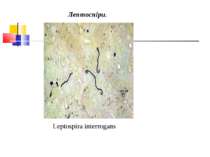
Збудник лептоспірозу (Leptospira interrogans) Морфологія і фізіологія. Лептоспіри - довгі, тонкі, спіралеподібні мікроорганізми довжиною 10-20 мкм, шириною 0,1-0,25 мкм, з 12-18 дрібними завитками. Кінці їх загнуті у вигляді крючків і стовщені. На фіксованих препаратах виявляють вторинні завитки, які надають їм вигляд, що нагадує латинські літери S або С. Окремі штами не мають крючків. Лептоспіри погано забарвлюються аніліновими барвниками, грамнегативні, за Романовським-Гімзою фарбуються у блідо-рожевий колір. Частіше їх вивчають у живому стані в темному полі Вони надзвичайно рухливі, роблять обертальні й поступальні рухи.
Культуральні властивості Збудник лептоспірозу - облігатний аероб, краще культивується при температурі 28-30 °С на рідких і напіврідких живильних середовищах, які містять 10 % кролячої сироватки. Лептоспіри ростуть повільно і не каламутять бульйон. Їх виявляють на 7-10 день за допомогою дослідження краплі середовища в темному полі.
Антигенна структура. L. interrogans - єдиний вид лептоспір, патогенний для людини. За білковими і ліпоїдними антигенами розрізняють 19 серогруп і 180 сероварів, які визначають у реакції аглютинації з відповідними сироватками. У нашій країні виявили всього 20 сероварів. Екзотоксину лептоспіри не продукують, мають ендотоксин, який зумовлює інтоксикацію організму.
Захворювання людини. Зараження відбувається через пошкоджену шкіру і слизові оболонки. Інкубаційний період триває 7-14 днів. Хвороба починається гостро, з ознобом, швидким підвищенням температури тіла до 39-40 °C. У хворих розвивається загальна слабість, головний біль, інтенсивний біль у м’язах, особливо литкових. На місці вхідних воріт ніяких змін не виникає. Із током лімфи лептоспіри проникають у загальний кровоток і поширюються по всьому організму, уражаючи паренхіматозні органи, особливо печінку. В тяжких випадках розвиваються жовтяниця і жирове переродження цього органа. Можуть також уражатися нирки, тоді лептоспіри довго виділяються із сечею. Перебіг патологічного процесу часто має хвилеподібний характер.
Лабораторна діагностика. Від хворого беруть кров, ліквор, сечу. Проводять пряму бактеріоскопію краплі досліджуваного матеріалу в темному полі зору. Метод простий, зручний, дає змогу швидко і в ранні строки встановити діагноз. Але лептоспіри не завжди можна виявити при мікроскопії. Більш достовірним методом є бактеріологічне дослідження. У перші дні хвороби 5-8 мл крові висівають по 1 мл у декілька пробірок із рідким середовищем, яке містить сироватку кроля, і вирощують при 28 °С 7-10 днів, виявляючи лептоспір у темному полі. Культуру із сечі можна отримати таким самим способом, починаючи з другого тижня хвороби. Раннім методом лабораторної діагностики лептоспірозу є біологічна проба. Кільком молодим гвінейським свинкам вводять внутрішньоочеревинно по 3-5 мл крові хворого. Через 2-3 дні досліджують ексудат черевної порожнини в темному полі. У практичних лабораторіях найчастіше проводять серологічну діагностику. Ставлять реакцію мікроаглютинації і лізису із сироваткою хворого і живими еталонними штамами лептоспір різних серогруп і через дві години проводять облік реакції в темному полі.
Схожі презентації
Категорії