Презентація на тему:
вода жива
Завантажити презентацію
вода жива
Завантажити презентаціюПрезентація по слайдам:
Вода, яка біжить крізь гірські породи, взаємодіє з природнім вуглекислим газом, що є в повітрі і перетворює нерозчинні карбонати на розчинні гідрогенкарбонати. CaCO3+CO2+H2O=Ca(HCO3)2; MgCO3+CO2+H2O=Mg(HCO3)2.
Мета Поглибити знання учнів про будову та склад води, її походження та різноманітність; Ознайомитися із поняттями “твердість води”, вивчення видів твердості води та методів її усунення; Виховувати бережливе ставлення до природніх водних ресурсів України і місцевості зокрема.
Очікуванні результати: Учні: поглиблюють знання про воду; розкривають поняття твердість та її види; вивчають способи усунення твердості води; встановлюють причинно-наслідкові зв’язки позитивно-негативного впливу твердості і якості води на живі організми.
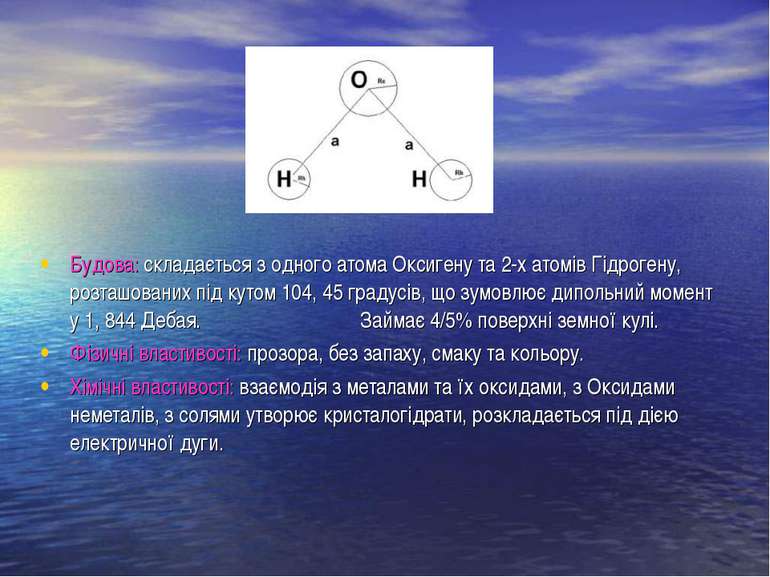
Будова: складається з одного атома Оксигену та 2-х атомів Гідрогену, розташованих під кутом 104, 45 градусів, що зумовлює дипольний момент у 1, 844 Дебая. Займає 4/5% поверхні земної кулі. Фізичні властивості: прозора, без запаху, смаку та кольору. Хімічні властивості: взаємодія з металами та їх оксидами, з Оксидами неметалів, з солями утворює кристалогідрати, розкладається під дією електричної дуги.
Запаси води 1386 млн. Км3 - запаси води на планеті; З них 97,5% - солона або мінералізована вода; 2,5% - прісна вода; З 2,5% - 71% льодовики; 60% суходолу відчуває дефіцит води.
Добова норма води для людини: 2,5л на добу; З їжею – 1,3л; Питна вода – 1,2л; За життя людина споживає50-60 тонн води; Вміст в організмі – понад 60%, в м’язах – 78%, в мозку 88%, в крові – 77,82%, в кістках – від 20%.
Вода – життєдайна сила Помиляється той – хто не п’є воду а лише чай та каву, адже ці напої сприяють виведеню рідини з організму.
Твердість води - властивість зумовлена наявністю в ній розчинних солей – Кальцію та Магнію. Розрізняють воду тверду, що містить розчинні солі, або м’яку яка цих солей не містить.
Загальна твердість води складається: Карбоатної (тимчасової). Спричинена наявністю у воді гідрогенкарбонатів, Кальцію та Магнію. Некарбонатної (сталої). Обумовлена наявністю у воді сульфатів, хлоридів та нітратів йонів Кальцію та Магнію.
Види твердості води. Одиниця твердості води. Одиниця твердості води –міліеквівалент,що включає 20,04 мг/г йонів Са2+ пбо 12.16 мг/г йонів Мg2+. Види твердості води: Мяка-вода з твердістю менше 4 міліеквівалент/л; Середньої твердості-вода з твердістю 4-8 міліеквівалент/л відповідних йонів; Дуже тверда-вода,з твердіст. 8-12 міліеквівалент/л йонів; Морська ж вода має загальну твердість 65 міліеквівалентів/л.
Способи усунення твердості води 1.Карбонатної твердості: а) кипіння: Ca (HCO3)2 = CaCO3 +H2O+СО2 ; б)додавання соди: Mg (HCO3)2+Na2CO3=Mg CO3 +2NaHCo3; в)додавання гашеного вапнау (у промисловості): Ca(HCO3)+ Ca(OH)2=2CaCO3 +2H2O; 2.Некарбонатної твердості: а)содовий метод: CaSO4+Na2CO3=CaCO3 +Na2SO4; б)фосфатний метод: 3MgSO4+2Na3Po4= Mg3(PO4)2 + 3Na2SO4.
Легенда У повісті Г.Хаггарда “Клеопатра – володарка зорі”, розповідається наступне: “Вона вийняла з вуха одну із величезних перлин...і... опустила її в оцет. Запала мовчанка, вражені гості, завмерши, спостерігали, як незрівняна перлина повільно розчиняється в міцному оцті. Коли від неї не залишилося й сліду, Клеопатра підняла кубок, покрутила його і випила все до останьої каплі”.
Демонстрації Демонстрація І: Порівняння розчинення мила в твердій та м’кій (дистильованій воді): беремо 2 колби, в першу наливаємо тверду воду, в другу - дистильвану. В обидві ємкості доливаємо окремими порціями мильний розчин, до утворення стійкої піни. Спостерігаємо... Демонстрація ІІ: беремо шкаралупу курячого яйця і пробуємо її розчинити в отцовій кислоті. Запитання: як можна очистити зварене яйце не розбиваючи шкаралупи? Білий щільний наліт з вапняного молока можна усунути?
Вимоги до якості води В Україні якість питної води визначається нормативними документами, зокрема міждержавним стандартом ГОСТ 2874 -82 Джерелом забруднення води є: отруйні відходи виробництв відходи тваринництва нерозчинні домішки змиті з полів потрапляння домішок миючих засобів вплив сміттязвалищ Для міста Тернополя залишається актуальний проблема Малашівського сміттєзвалища і Івачівського водозабору.
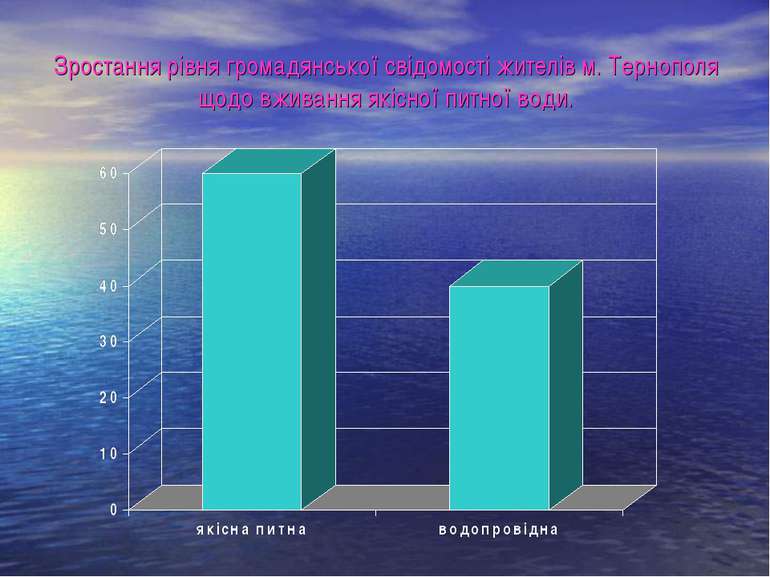
Зростання рівня громадянської свідомості жителів м. Тернополя щодо вживання якісної питної води.
Питна вода є джерелом Кальцію та Магнію для людського організму. Нестача Магнію в організмі людини зумовлює хронічну втому, гіпертонію, судинні порушення, інфаркт міокарда. Дефіцитом Кальцію викликано близько 150 захворювань, він є практично “людським клеєм”, що зміцнює весь організм. Важливим для організму є наявність атомарного Оксигену. З порушенням рівноваги метаболічних процесів в яких беруть участь Оксиген та Кальцій пов’язаний процес старіння. Ці знання необхідні людині для ведення правильного способу життя. Постійна твердість є шкідливою для людини?
Карбонатна твердість обумовлена присутністю у воді солей: а)CaSO4; MgSO4 ; б)Ca (HCO3)2 ; Mg (HCO3)2 Дуже тверда вода має: а)10-12 міліеквівалентів/л йонів; б)4-8 міліеквівалентів/л йонів; в)8-12 міліеквівалентів/л йонів.
Усунення карбонатної твердості кип’ятінням ілюструє іонне рівняння: а)Са2+ +CO32-=CaCO3; б)Са2+ 2HCO3 - = CaCO3 + H2O+CO2; в)2HCO3-=CO2+H2O+CO32-; г)Mg2+ + 2OH- =Mg (OH)2. Усунення некарбонатної твердості кип’ятінням ілюструє іонне рівняння: а)Са2+ +CO32-=CaCO3; б)Са2+ 2HCO3 - = CaCO3 + H2O+CO2; в)2HCO3-=CO2+H2O+CO32-; г)Mg2+ + 2OH- =Mg (OH)2.
Прислів’я та приказки які заставляють мислити: Щоб спрагу вгасити, треба води попити; Із брудної води ще ніхто чистим не вийшов; Зіпсував воду, не буде честі твоєму роду; Вода крапля по краплі і камінь довбе.
Схожі презентації
Категорії