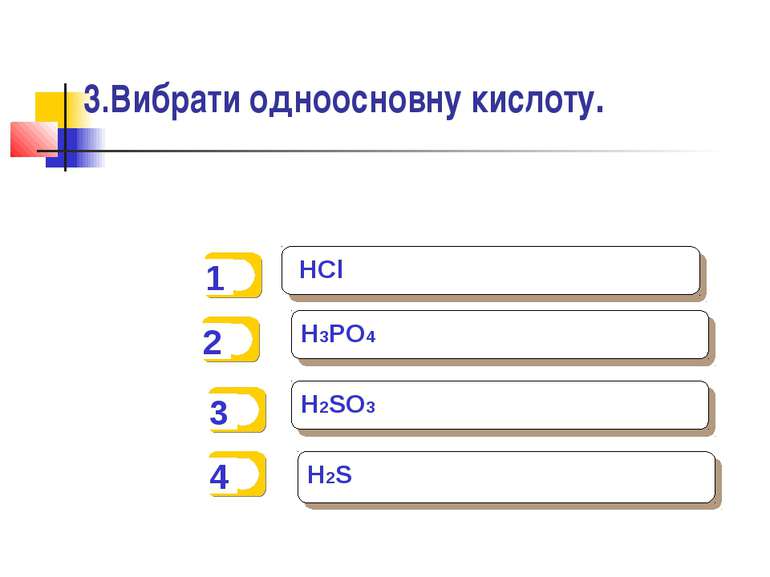
Презентація на тему:
Тест- тренажер з теми «Кислоти»
Завантажити презентацію
Тест- тренажер з теми «Кислоти»
Завантажити презентаціюПрезентація по слайдам:
Тема: «Загальна характеристика солей» 8 кл 900igr.net Учитель хімії Верховцевського НВК Кукса Наталія Миколаївна Україна. Дніпропетровська область
Мета уроку: Знати: визначення,склад, класифікацію,формули, номенклатуру ,фізичні та хімічні властивості солей,застосування та значення для життєдіяльності Вміти: Визначати солі, складати їх формули Записувати рівняння хімічних властивостей
Цілі: Склад,класифікація солей Поширення в природі Номенклатура,формули Фізичні властивості Хімічні властивості Добування Застосування
Загальна формула солей MenAm Солі – це складні речовини, які складаються з катіонів металів та аніонів кислотного залишку. .
Утворення солей Солі утворюются при заміщенні атомів гідрогену в кислоті на йони металів. Наприклад: HCl Na Cl HNO3 NaNO3 H2S Na2S H2SO4 Na2SO4
Поширення солей в природі. Поварена сіль NaCl Слово "сіль" пішло від грецького терміну "hals" – що означало "море", а мінералогічнкий термін повареної солі – галліт Це мінерал, який є основною необхідною речовиною для життєдіяльності, а також одним з найбільш важливих промислових сировинних мінералів
Вапняк CaCO3 тонкозернистий м’який, білий , складається з маленьких уламків та цілих вапняковых скелетів мікроорганізмів.
Корали КАЛЬЦИТ (вапняковий шпат минерал класу карбонатів, СаСО3. домішки Mg, Fe, Mn та ін. Різновиди: ісландський шпат, антраконит — черный кальцит. Будівельный материал; металургійний флюс.
Гіпс минерал класу сульфатів, CaSO4·2H2O. Різновиди: гіпсовый шпат (полупрозорі кристали); атласний шпат, або уральский селеніт (паралельно-волокнисті агрегати з шовковистим блиском), та алебастр (сніжно-білий тонкозернистый гіпс).
Номенклатура солей F – Cl – Br – I – S 2- SO3 2- SO4 2- Фторид Хлорид Бромід йодид Сульфід Сульфіт Сульфат
CO3 2- SiO3 2- NO3 – NO2 – PO4 3- PO3 – ClO4 Карбонат Сілікат Нітрат Нітрит Ортофосфат Метафосфат Хлорат
Алгоритм складання формул солей 1.На початку формули ставиться метал,а за ним кислотний залишок 2.Проставляються над йонами їх заряди 3.Знаходять найменше спільне кратне зарядів.(НСК) 4.При діленні НСК на заряди йонів отримуємо індекси. Ферум(ІІІ) сульфат VI III II III II FeSO4→ Fe2(SO4)3
Скласти формули солей Натрій хлорид Кальцій сульфат Ферум(ІІІ)карбонат Алюміній сілікат Купрум(ІІ)ортофосфат
Скласти формули солей Натрій хлорид Кальцій сульфат Ферум(ІІІ)карбонат Алюміній сілікат Купрум(ІІ)ортофосфат NaCl CaSO4 Fe2(CO3)3 Al2(SiO3)3 Cu3(PO4)2
Фізичні властивості Солі – кристалічні речовини, в основному білого кольору. Солі заліза – жовто - коричньового кольору. Солі міді – зеленовато-блакитного кольору. Солі хрому- зеленого та померанчового кольору.
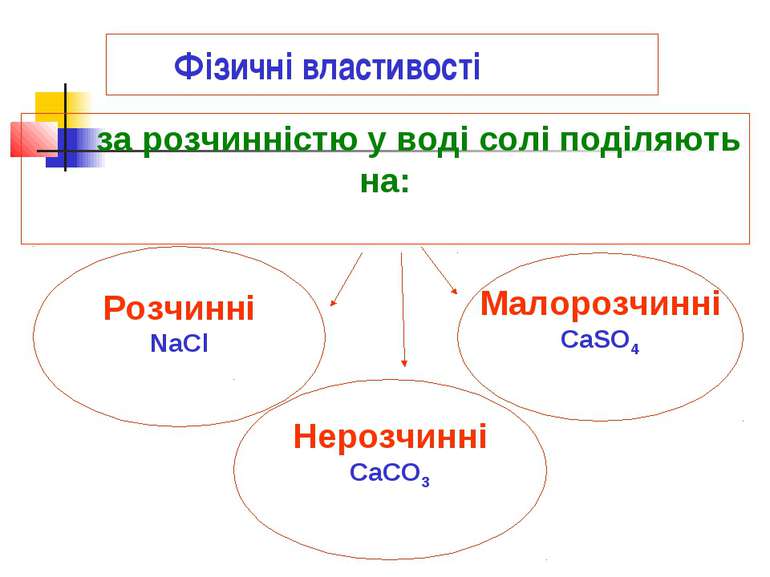
Фізичні властивості Розчинні NaCl за розчинністю у воді солі поділяють на: Нерозчинні CaCO3 Малорозчинні CaSO4
Хімічні властивості солей 1. Взаємодіють з металами: CuSO4 + Fe = FeSO4 + Cu (Метали,що стоять в РН лівіше,витісняють ті,що стоять правіше)
Схожі презентації
Категорії