Презентація на тему:
Карбонові кислоти
Завантажити презентацію
Карбонові кислоти
Завантажити презентаціюПрезентація по слайдам:
Карбонові кислоти – це похідні вуглеводнів, молекули яких містять одну або кілька функціональних карбоксильних груп –СООН.
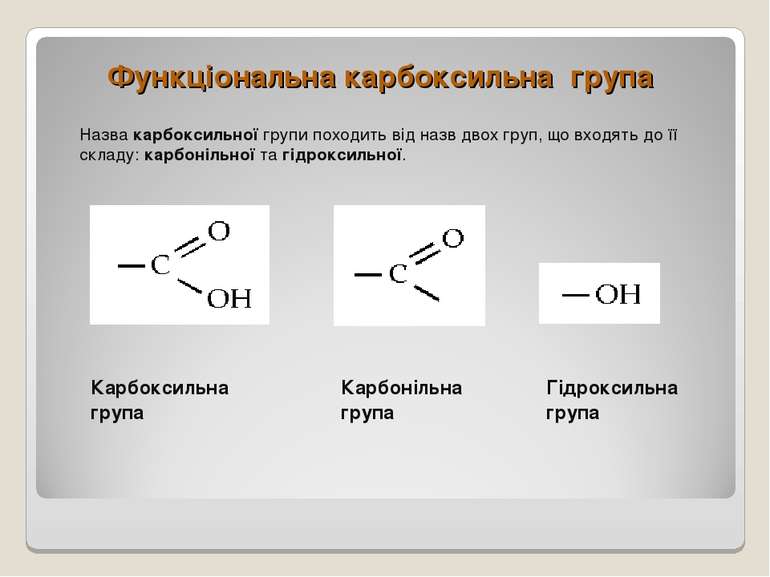
Функціональна карбоксильна група Назва карбоксильної групи походить від назв двох груп, що входять до її складу: карбонільної та гідроксильної. Карбоксильна група Карбонільна група Гідроксильна група
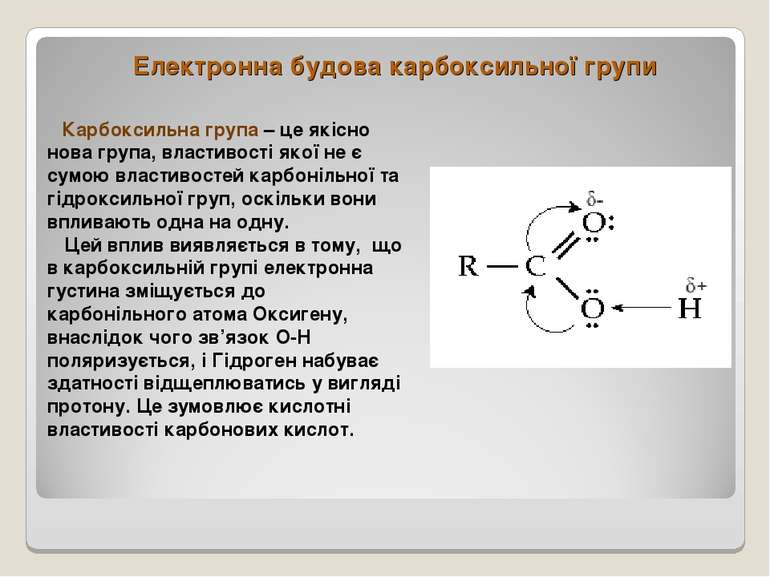
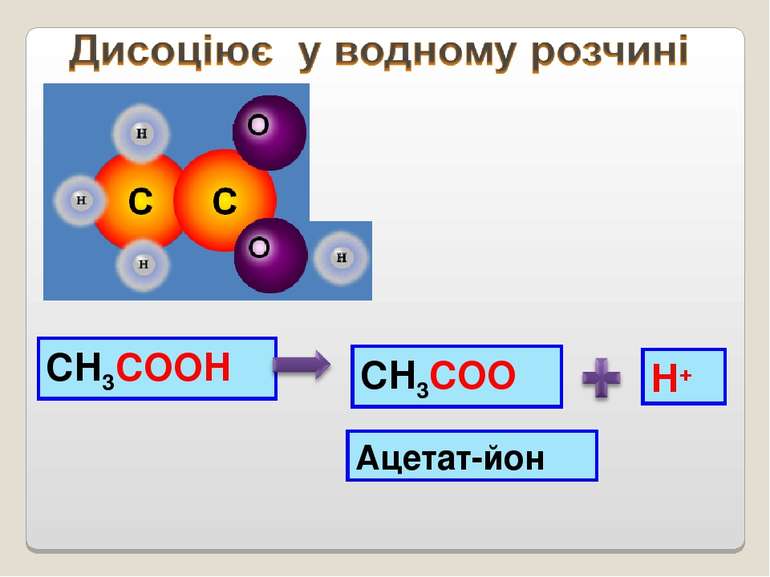
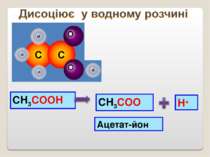
Електронна будова карбоксильної групи Карбоксильна група – це якісно нова група, властивості якої не є сумою властивостей карбонільної та гідроксильної груп, оскільки вони впливають одна на одну. Цей вплив виявляється в тому, що в карбоксильній групі електронна густина зміщується до карбонільного атома Оксигену, внаслідок чого зв’язок О-Н поляризується, і Гідроген набуває здатності відщеплюватись у вигляді протону. Це зумовлює кислотні властивості карбонових кислот.
Мурашина кислота H-COOH Бджолина отрута Залози комах Кропива Гусениці шовкопряду Соснова хвоя
Класифікація карбонових кислот Залежно від кількості карбоксильних груп Одноосновні (монокарбонові) Двохосновні (дикарбонові) Багатоосновні (полікарбонові) Залежно від вуглеводневого радикала Насичені Ненасичені Ароматичні Залежно від наявності інших функціональних груп Гідроксикислоти Амінокислоти Галогенокар-бонові кислоти Оксикарбо-нові кислоти
Гомологічний ряд насичених одноосновних кислот Загальна формула гомологічного ряду насичених одноосновних карбонових кислот: СnН2n+1СООН
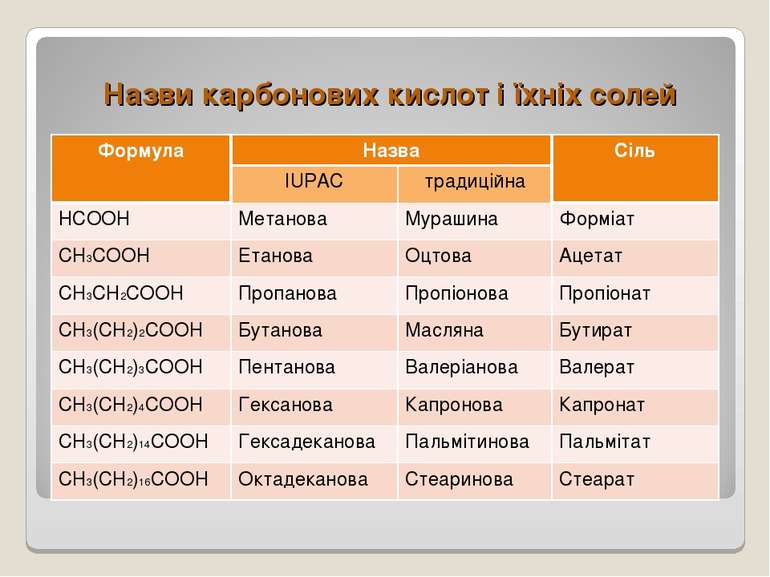
Назви карбонових кислот і їхніх солей Формула Назва Сіль IUPAC традиційна HCOOH Метанова Мурашина Форміат CH3COOH Етанова Оцтова Ацетат CH3CH2COOH Пропанова Пропіонова Пропіонат CH3(CH2)2COOH Бутанова Масляна Бутират CH3(CH2)3COOH Пентанова Валеріанова Валерат CH3(CH2)4COOH Гексанова Капронова Капронат CH3(CH2)14COOH Гексадеканова Пальмітинова Пальмітат CH3(CH2)16COOH Октадеканова Стеаринова Стеарат
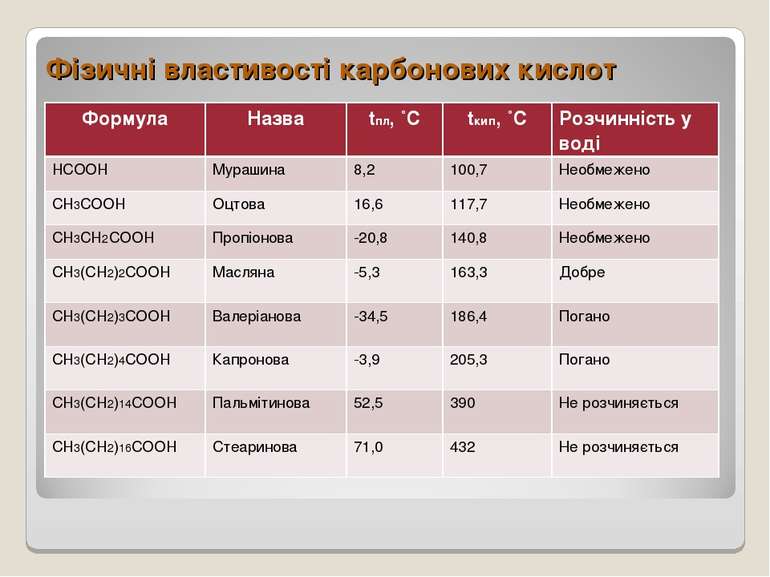
Фізичні властивості карбонових кислот Формула Назва tпл, ˚C tкип, ˚C Розчинність у воді HCOOH Мурашина 8,2 100,7 Необмежено CH3COOH Оцтова 16,6 117,7 Необмежено CH3CH2COOH Пропіонова -20,8 140,8 Необмежено CH3(CH2)2COOH Масляна -5,3 163,3 Добре CH3(CH2)3COOH Валеріанова -34,5 186,4 Погано CH3(CH2)4COOH Капронова -3,9 205,3 Погано CH3(CH2)14COOH Пальмітинова 52,5 390 Не розчиняється CH3(CH2)16COOH Стеаринова 71,0 432 Не розчиняється
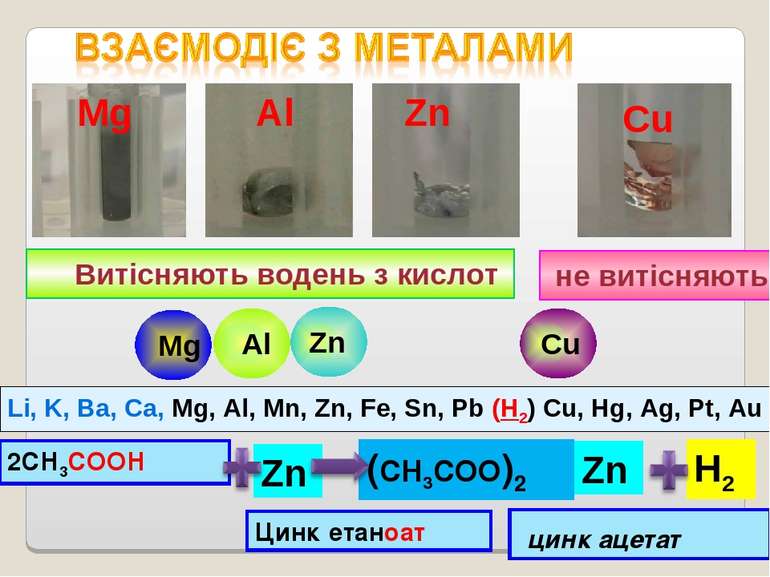
Витісняють водень з кислот Li, K, Ba, Ca, Mg, Al, Mn, Zn, Fe, Sn, Pb (H2) Cu, Hg, Ag, Pt, Au не витісняють Mg Al Cu Zn 2СН3СООН Zn Zn H2 (СН3СОО)2 Цинк етаноат цинк ацетат
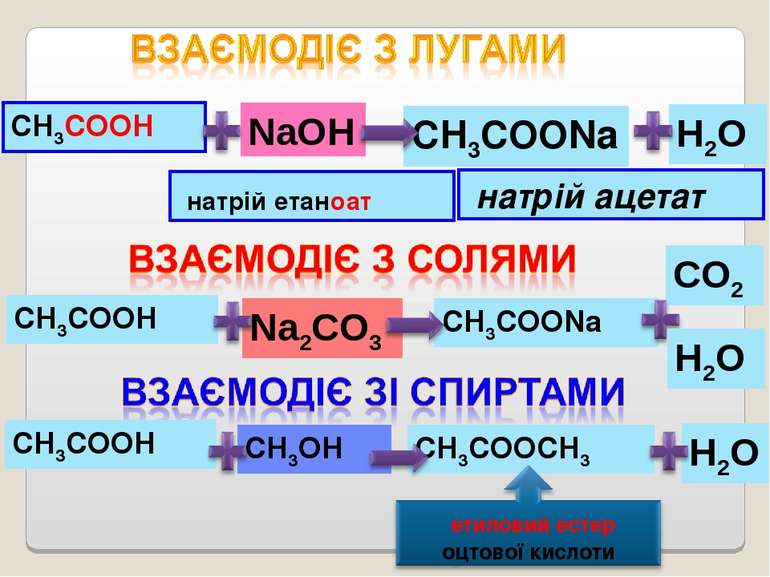
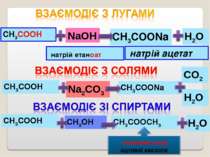
CO2 СН3СООNa Na2CO3 H2O СН3СООН NaOH СН3СООNa натрій етаноат натрій ацетат СН3СООН H2O СН3СООН СН3ОН СН3СООСН3 H2O
Способи добування насичених одноосновних карбонових кислот: а) в промисловості - окиснення алканів - окиснення первинних спиртів - окиснення альдегідів б) в лабораторії - із солей
Мурашина (метанова, форміатна) кислота HCOOH Мурашина кислота має сильні бактерицидні властивості, тому її водні розчини використовують як харчовий консервант, а пари – для дезінфекції бродильних чанів та бджолиних вуликів. Слабкий спиртовий розчин кислоти(мурашиний спирт) використовують в медицині для розтирань.
Мурашина (метанова, форміатна) кислота HCOOH Мурашина кислота також застосовується в шкіряній (дублення шкір) та текстильній промисловості (як протрава при фарбуванні), виробництві деяких полімерів, органічному синтезі.
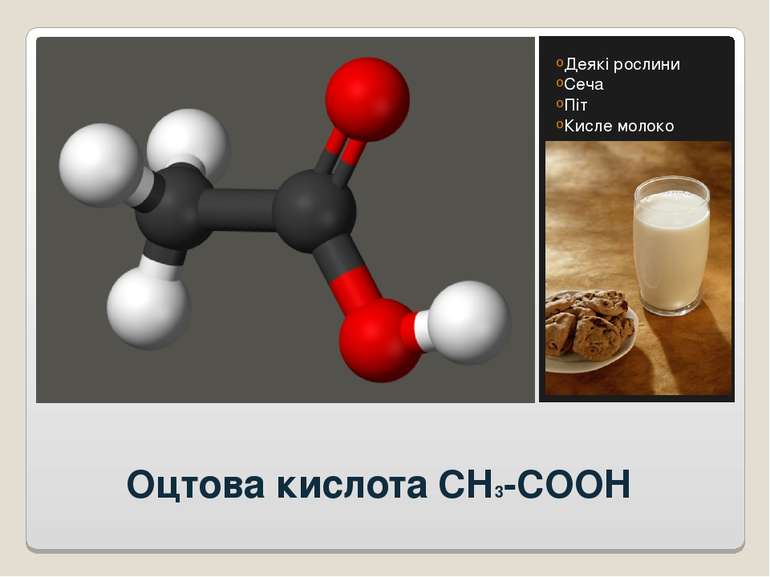
Оцтова (етанова, ацетатна) кислота CH3-COOH Оцтову кислоту використовують в харчовій промисловості (як консервант і як приправу до їжі). У сільському господарстві використовують як консервант, що дозволяє зберігати високу поживність кормів і запобігати гнилісним процесам.
Оцтова (етанова, ацетатна) кислота CH3-COOH Оцтова кислота застосовується для одержання барвників, пластмас, лікарських препаратів (ацетилсаліцилової кислоти), ацетатного шовку, фотоплівки.
Пальмітинова(C15H33-COOH) і стеаринова(C17H35-COOH) кислоти Пальмітинова і стеаринова кислоти використовуються для виготовлення свічок. Розчинні солі цих кислот застосовуються для виробництва мила.
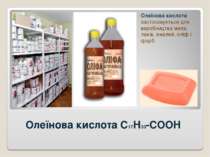
Олеїнова кислота C17H33-COOH Олеїнова кислота застосовується для виробництва мила, лаків, емалей, оліф і фарб.
Яка загальна формула насичених одноосновних карбонових кислот? а) СnН2nСООН; б) CnH2n+1COOH; в) СnН2n-1CООН; г) CnH2n+1CHО.
ДОМАШНЄ ЗАВДАННЯ П.П. Попель, Л. С. Крикля Хімія Підручник 10 клас §18, §19, вправа №130, 131
Схожі презентації
Категорії