Презентація на тему:
Карбонові кислоти
Завантажити презентацію
Карбонові кислоти
Завантажити презентаціюПрезентація по слайдам:
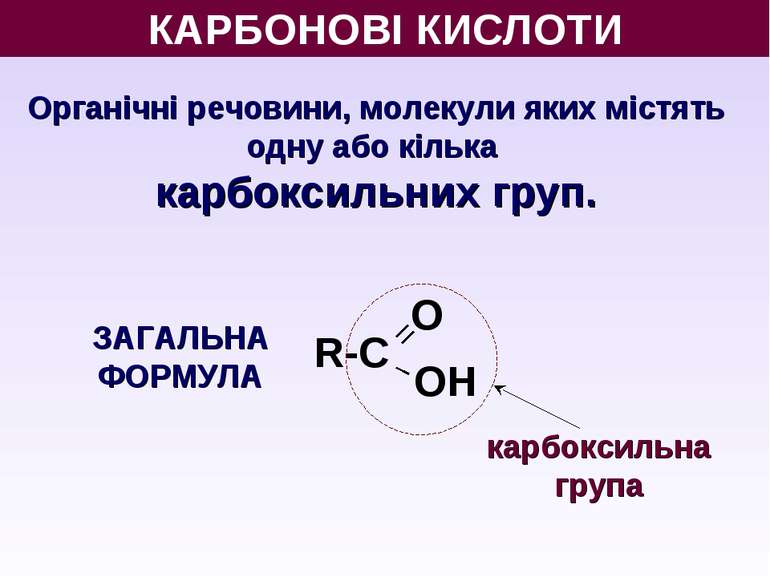
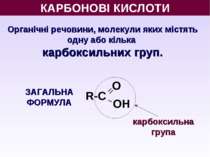
КАРБОНОВІ КИСЛОТИ Органічні речовини, молекули яких містять одну або кілька карбоксильних груп. О ОН R-С карбоксильна група ЗАГАЛЬНА ФОРМУЛА
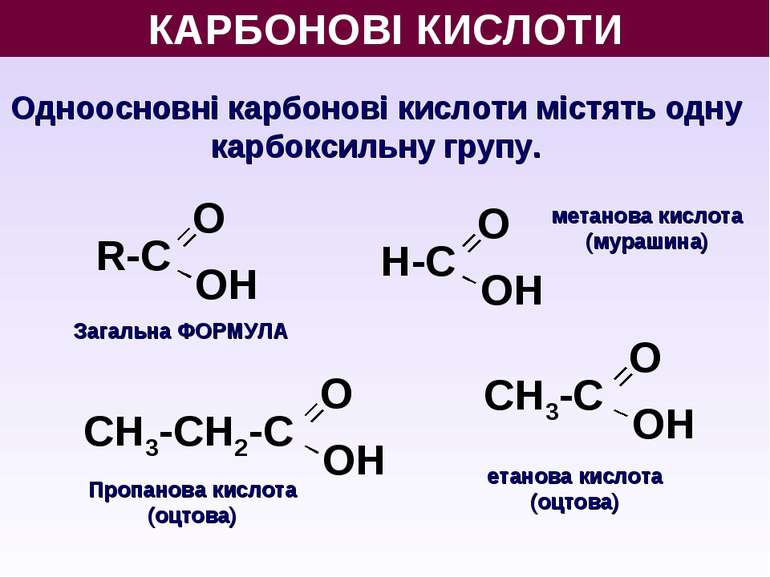
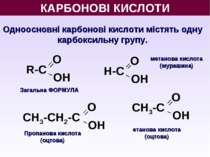
КАРБОНОВІ КИСЛОТИ Одноосновні карбонові кислоти містять одну карбоксильну групу. О ОН R-С О ОН СН3-С О ОН СН3-СН2-С О ОН Н-С Загальна ФОРМУЛА метанова кислота (мурашина) етанова кислота (оцтова) Пропанова кислота (оцтова)
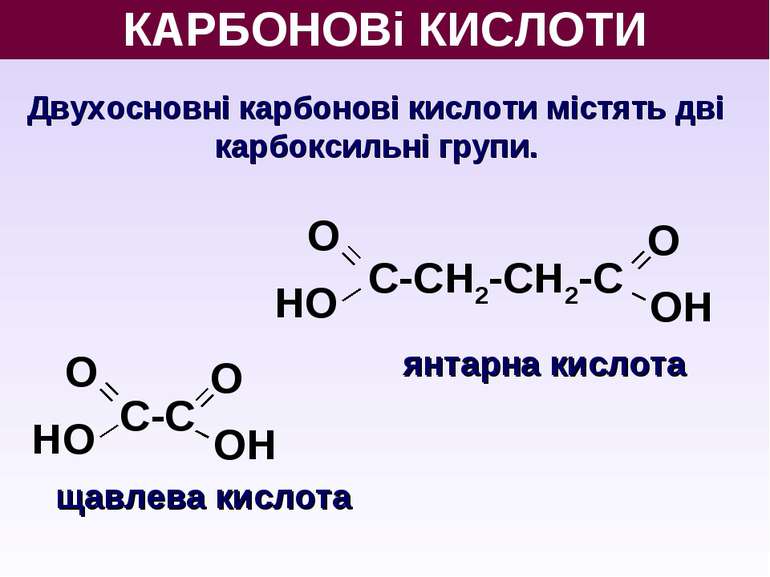
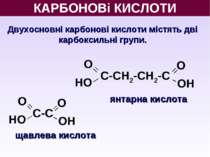
О НО КАРБОНОВі КИСЛОТИ Двухосновні карбонові кислоти містять дві карбоксильні групи. О ОН С-С О ОН С-СН2-СН2-С щавлева кислота янтарна кислота О НО
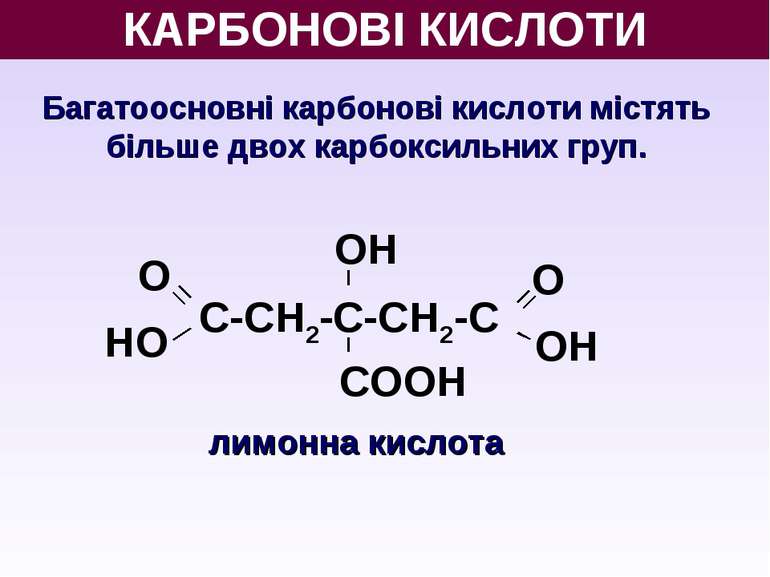
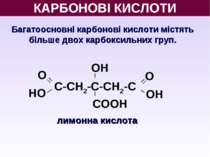
КАРБОНОВІ КИСЛОТИ Багатоосновні карбонові кислоти містять більше двох карбоксильних груп. лимонна кислота
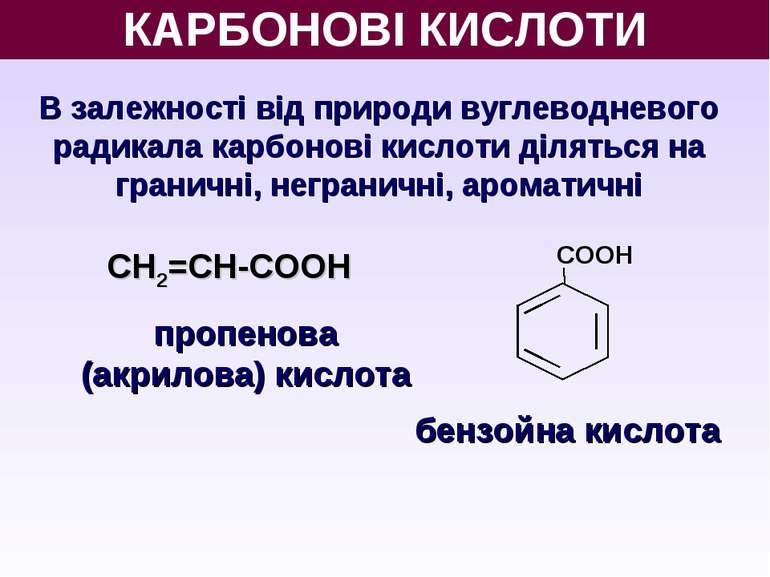
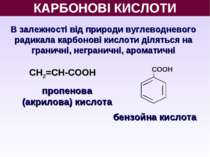
КАРБОНОВІ КИСЛОТИ В залежності від природи вуглеводневого радикала карбонові кислоти діляться на граничні, неграничні, ароматичні пропенова (акрилова) кислота СН2=СН-СООН CООН бензойна кислота
[ O ] ОКИСЛЕННЯ ПЕРВІЧНИХ СПИРТІВ І АЛЬДЕГІДІВ: бутанол СН3-СН2-СН2-СН2-ОН О ОН СН3-СН2-СН2-С бутановаІ кислота [ O ] О ОН СН3-СН2-СН2-С бутановаІ кислота О Н СН3-СН2-СН2-С ОТРИМАННЯ КАРБОНОВИХ КИСЛОТ
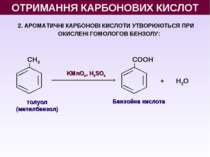
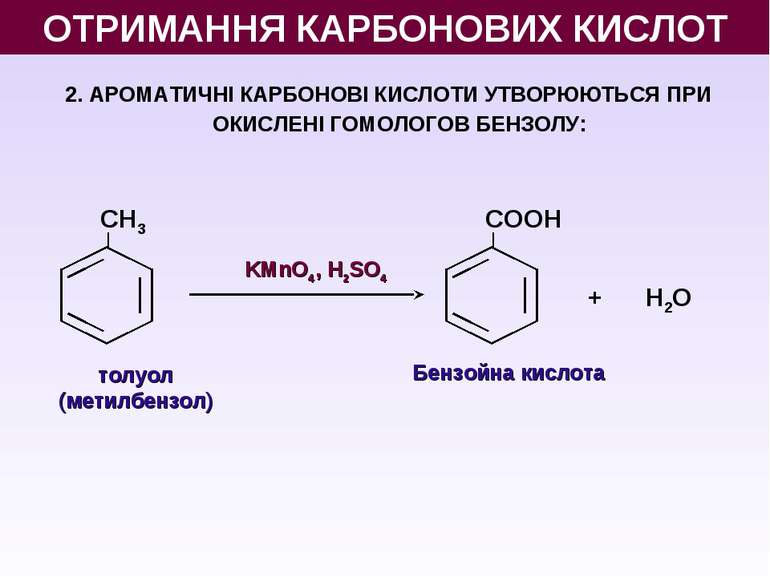
2. АРОМАТИЧНІ КАРБОНОВІ КИСЛОТИ УТВОРЮЮТЬСЯ ПРИ ОКИСЛЕНІ ГОМОЛОГОВ БЕНЗОЛУ: толуол (метилбензол) KMnO4, H2SO4 Бензойна кислота CH3 CООН + H2О ОТРИМАННЯ КАРБОНОВИХ КИСЛОТ
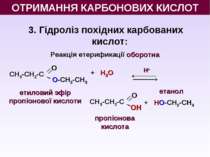
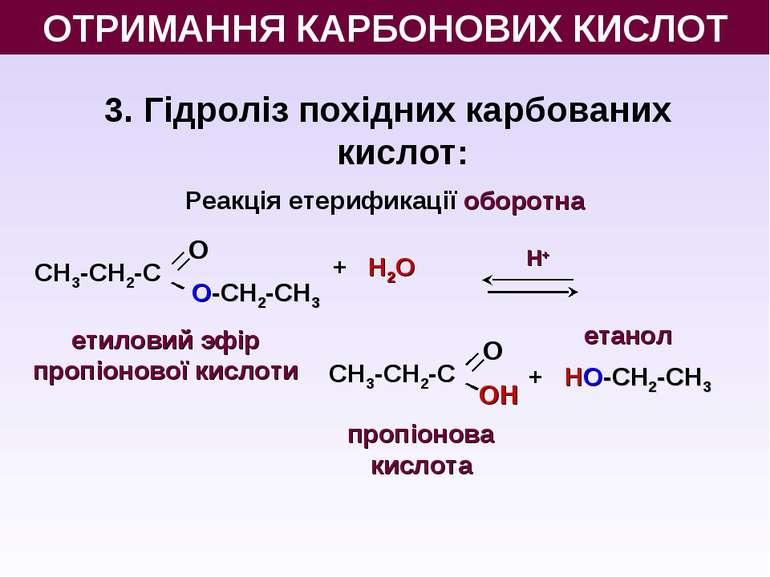
3. Гідроліз похідних карбованих кислот: Реакція етерификації оборотна Н+ + Н2O + НО-СН2-СН3 пропіонова кислота етанол етиловий эфір пропіонової кислоти ОТРИМАННЯ КАРБОНОВИХ КИСЛОТ
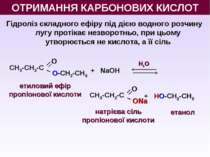
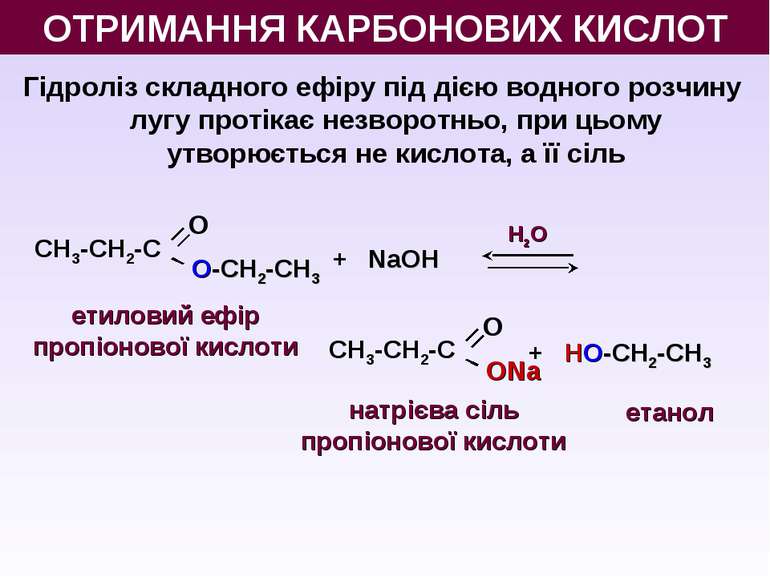
Гідроліз складного ефіру під дією водного розчину лугу протікає незворотньо, при цьому утворюється не кислота, а її сіль H2O + NaOH + НО-СН2-СН3 натрієва сіль пропіонової кислоти етанол етиловий ефір пропіонової кислоти ОТРИМАННЯ КАРБОНОВИХ КИСЛОТ
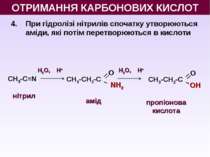
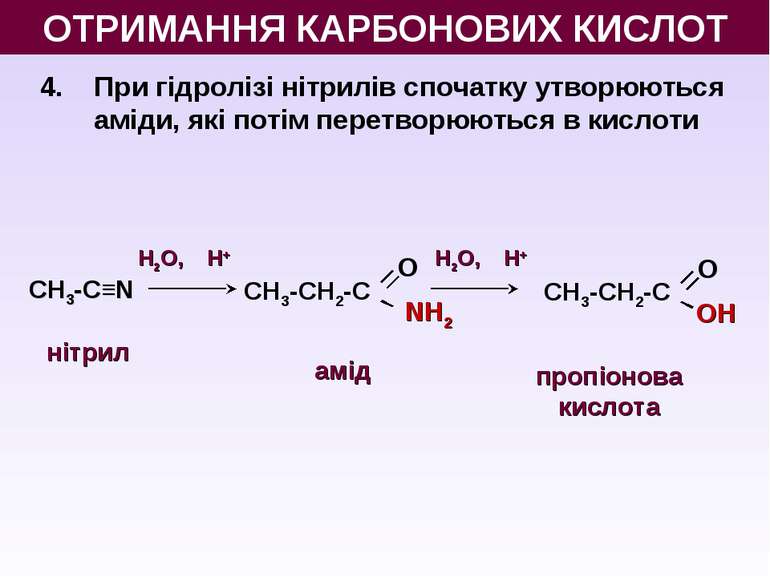
4. При гідролізі нітрилів спочатку утворюються аміди, які потім перетворюються в кислоти СН3-C≡N H2O, Н+ H2O, Н+ нітрил амід пропіонова кислота ОТРИМАННЯ КАРБОНОВИХ КИСЛОТ
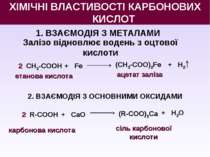
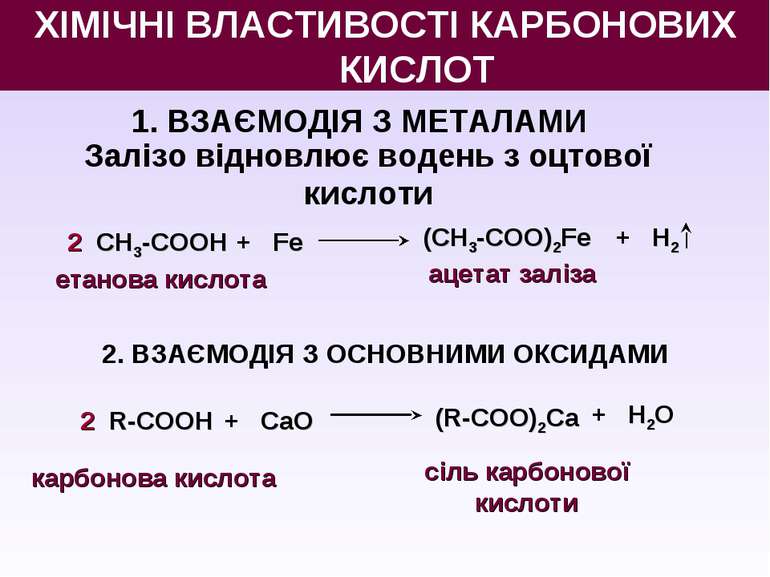
1. ВЗАЄМОДІЯ З МЕТАЛАМИ 2 СН3-СООН + Fe етанова кислота ХІМІЧНІ ВЛАСТИВОСТІ КАРБОНОВИХ КИСЛОТ (СН3-СОО)2Fe + H2 Залізо відновлює водень з оцтової кислоти ацетат заліза 2. ВЗАЄМОДІЯ З ОСНОВНИМИ ОКСИДАМИ 2 R-СООН + CaO (R-СОО)2Ca + H2O карбонова кислота сіль карбонової кислоти
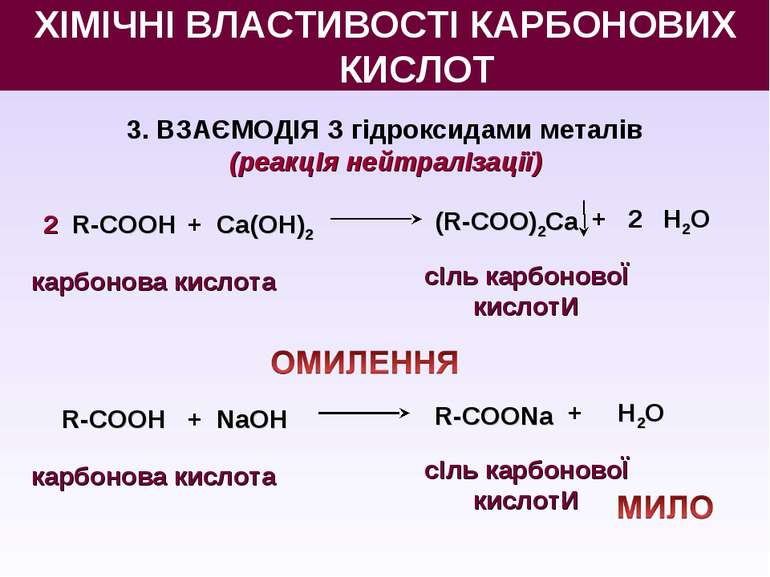
3. ВЗАЄМОДІЯ З гідроксидами металів (реакцІя нейтралІзації) 2 R-СООН + Ca(OН)2 (R-СОО)2Ca + 2 H2O карбонова кислота сІль карбоновоЇ кислотИ R-СООН + NaOН R-СООNa + H2O карбонова кислота сІль карбоновоЇ кислотИ ХІМІЧНІ ВЛАСТИВОСТІ КАРБОНОВИХ КИСЛОТ
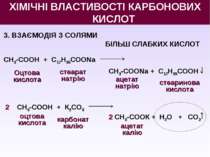
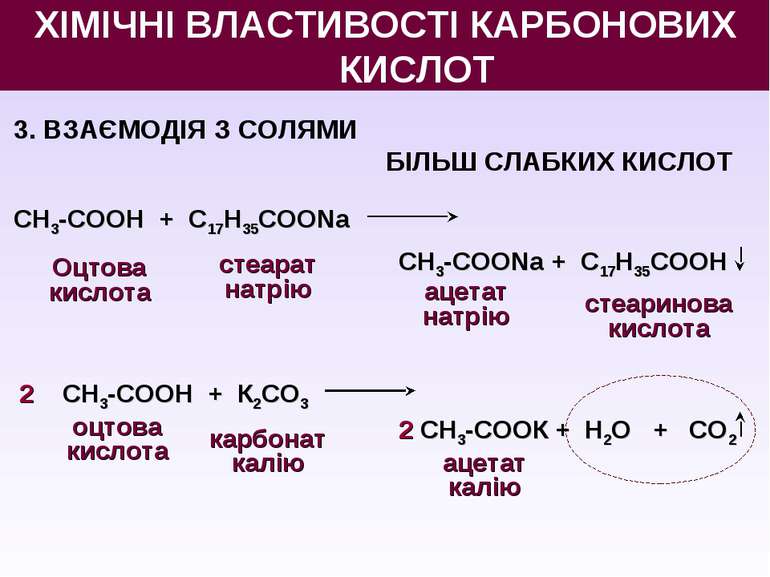
3. ВЗАЄМОДІЯ З СОЛЯМИ БІЛЬШ СЛАБКИХ КИСЛОТ СН3-СООН + С17Н35СООNa Оцтова кислота СН3-СООNa + С17Н35СООН 2 СН3-СООН + К2СО3 2 СН3-СООК + Н2О + СО2 стеарат натрію ацетат натрію стеаринова кислота оцтова кислота карбонат калію ацетат калію ХІМІЧНІ ВЛАСТИВОСТІ КАРБОНОВИХ КИСЛОТ
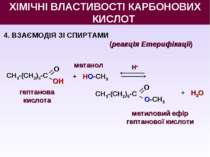
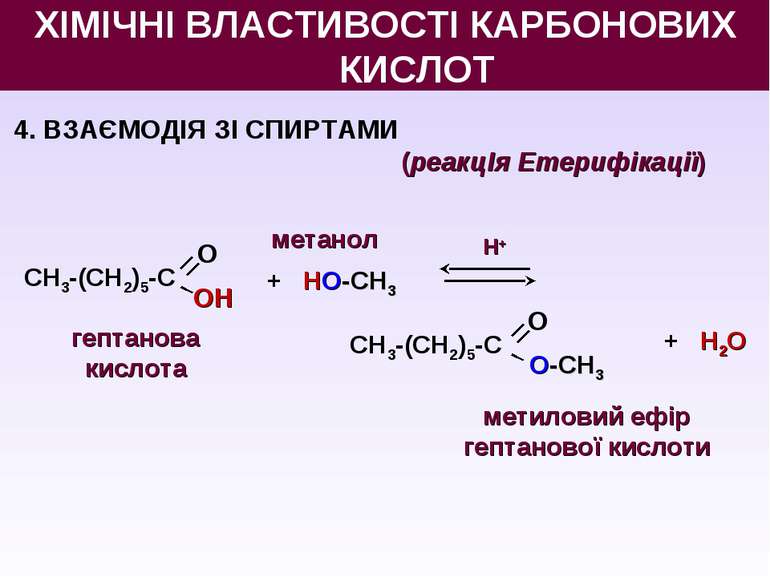
4. ВЗАЄМОДІЯ ЗІ СПИРТАМИ (реакцІя Етерифікації) + НО-СН3 Н+ + Н2O гептанова кислота метанол метиловий ефір гептанової кислоти ХІМІЧНІ ВЛАСТИВОСТІ КАРБОНОВИХ КИСЛОТ
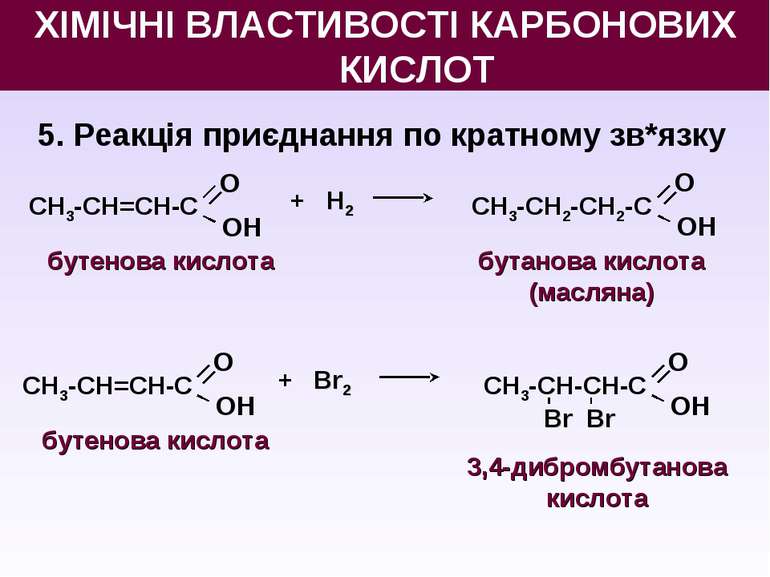
5. Реакція приєднання по кратному зв*язку бутенова кислота О OН СН3-СН=СН-С + H2 О OН СН3-СН2-СН2-С бутанова кислота (масляна) бутенова кислота О OН СН3-СН=СН-С + Br2 О OН СН3-СН-СН-С 3,4-дибромбутанова кислота Br Br ХІМІЧНІ ВЛАСТИВОСТІ КАРБОНОВИХ КИСЛОТ
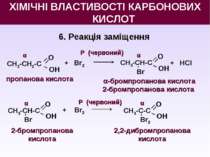
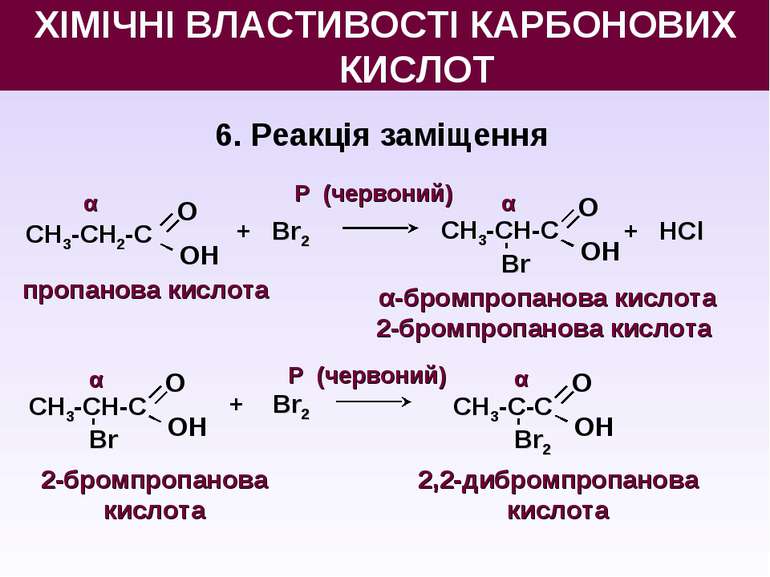
6. Реакція заміщення О OН СН3-СН2-С пропанова кислота + Br2 О OН СН3-СН-С Br + НCl α α О OН СН3-СН-С Br α + Br2 О OН СН3-С-С Br2 α α-бромпропанова кислота 2-бромпропанова кислота 2-бромпропанова кислота 2,2-дибромпропанова кислота Р (червоний) Р (червоний) ХІМІЧНІ ВЛАСТИВОСТІ КАРБОНОВИХ КИСЛОТ
Мурашиная кислота застосовується в медицині, бджільництві, в органічному синтезі, при отриманні розчинників та консервантів; як сильного відновлювача. Вперше була виділена в XVII столітті з червоних лісових мурашок. Міститься також в соку пекучої кропиви. Безводна мурашина кислота - безбарвна рідина з гострим запахом і пекучим смаком, що викликає опіки на шкірі. Застосовується в текстильній промисловості в якості протрави при фарбуванні тканин, для дублення шкір, а також для різних синтезів
Оцтова кислота застосовується в харчовій та хімічній промисловості (виробництво ацетилцелюлози, з якої отримують ацетатне волокно, органічне скло, кіноплівку; для синтезу барвників, медикаментів і складних ефірів). У домашньому господарстві як смакова і консервуюча речовина. Широко поширена в природі - міститься у виділеннях тварин (сечі, жовчі, екскрементах), в рослинах (у зелених листках). Утворюється при бродінні, гнитті, скисании вина, пива, міститься в кислому молоці і сирі.
Схожі презентації
Категорії


![[ O ] ОКИСЛЕННЯ ПЕРВІЧНИХ СПИРТІВ І АЛЬДЕГІДІВ: бутанол СН3-СН2-СН2-СН2-ОН О ... [ O ] ОКИСЛЕННЯ ПЕРВІЧНИХ СПИРТІВ І АЛЬДЕГІДІВ: бутанол СН3-СН2-СН2-СН2-ОН О ...](https://svitppt.com.ua/images/16/15532/770/img6.jpg)



![[ O ] ОКИСЛЕННЯ ПЕРВІЧНИХ СПИРТІВ І АЛЬДЕГІДІВ: бутанол СН3-СН2-СН2-СН2-ОН О ... [ O ] ОКИСЛЕННЯ ПЕРВІЧНИХ СПИРТІВ І АЛЬДЕГІДІВ: бутанол СН3-СН2-СН2-СН2-ОН О ...](https://svitppt.com.ua/images/16/15532/210/img6.jpg)