Презентація на тему:
Оксиген
Завантажити презентацію
Оксиген
Завантажити презентаціюПрезентація по слайдам:
«Оксиген как химический элемент. Кислород как простое вещество. Кислород в природе. Физиологическое действие кислорода. Получение кислорода в лаборатории. Реакция разложения. Понятие о катализаторе. Физические свойства кислорода.» Цель: закрепить понятия об элементах и простых веществах на примере кислорода; ознакомить учащихся с историей открытия кислорода, его распространением в природе и физиологическим действием; сформировать понятие о реакции разложения на примере реакций получения кислорода; выяснить физические свойства кислорода; развивать познавательную компетентность; поликультурную и коммуникативную компетентности. Коррекционная цель: воспитывать самоконтроль за речью, способствовать развитию активной функции памяти.
Расставить коэффициенты в уравнениях P + O2 → P2O5 Fe + Cl2 → Fe Cl3 Fe Cl 2 + Cl2 → Fe Cl3 KClO3 → KCl + O2↑ Fe (OH)3 t Fe2O3 + H2O Al + I2 → Al I3
Оксиген - химический элемент, кислород - простое вещество. Без газа этого на свете Не жили б звери и народ, Его назвать могли б и дети Ведь это - кислород
Кислородная теория горения А история простая... Джозеф Пристли как-то раз, Окись ртути нагревая, Обнаружил странный газ. Газ без цвета, без названья, Ярче в нём горит свеча. А не вреден для дыханья? (Не узнаешь у врача) новый газ из колбы вышел – Никому он не знаком. Этим газом дышат мыши Под стеклянным колпаком. Человек им тоже дышит...
Стал кислород Чуть не всюду начинкой. С кремнием он обернулся песчинкой. В воздух попал кислород Как ни странно, Из голубой глубины океана. И на Земле появились растения. Жизнь появилась: Дыханье, горение... Первые птицы и первые звери, Первые люди, что жили в пещере... Огонь добывали с помощью трения, Хоть и не знали причины горения, Роль кислорода на нашей Земле Понял великий Лавуазье Распространение в природе
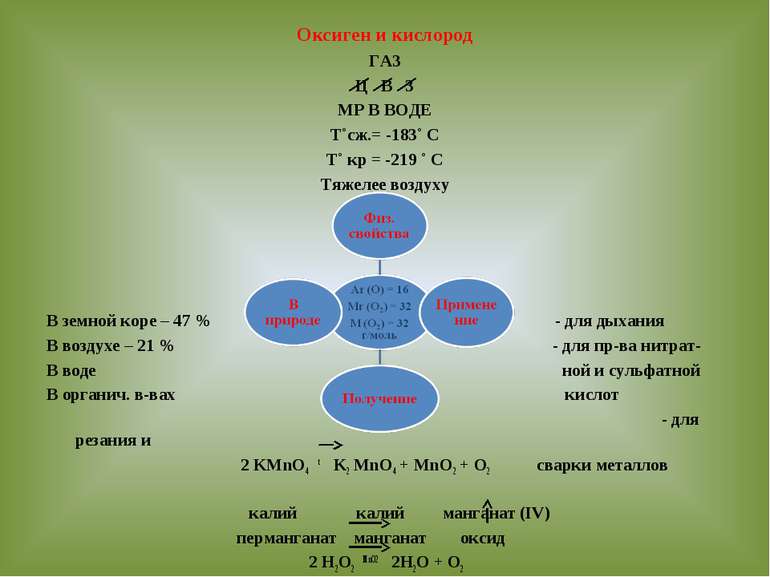
Оксиген и кислород ГАЗ Ц В З МР В ВОДЕ Т˚сж.= -183˚ С Т˚ кр = -219 ˚ С Тяжелее воздуху В земной коре – 47 % - для дыхания В воздухе – 21 % - для пр-ва нитрат- В воде ной и сульфатной В органич. в-вах кислот - для резания и 2 KMnO4 t K2 MnO4 + MnO2 + O2 сварки металлов калий калий манганат (IV) перманганат манганат оксид 2 H2O2 MnO2 2H2O + O2 2KClO3 MnO2 2KCl +3O2
Схожі презентації
Категорії