Презентація на тему:
Фізичні і хімічні властивості білків. Значення білків для людини. Хвороби зв'язані з відсутністю білків. Норми вживання білка
Завантажити презентацію
Фізичні і хімічні властивості білків. Значення білків для людини. Хвороби зв'язані з відсутністю білків. Норми вживання білка
Завантажити презентаціюПрезентація по слайдам:
Михайлюк Галина Анатоліївна вчитель хімії ЗОШ І – ІІІст. смт Раухівка, Березівського району Одеської області
Вивчити будову білкової молекули Утворення зв'язків Фізичні і хімічні властивості Значення для людини Хвороби зв'язані з відсутністю білків Норми вживання білка
Із інформаціоних джерела дізналися: - Білки –високомолекулярні сполуки; - Встановили якісні реакції на білки; - Дослідили роль білків в живій природі; - Значення білків для людини
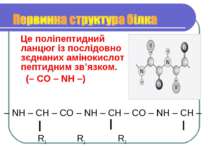
складні високомолекулярні природні органічні речовини, що складаються з амінокислот, сполучених пептидними зв'язками – NH – CH – CO – NH – CH – CO – NH – CH – R1 R2 R3
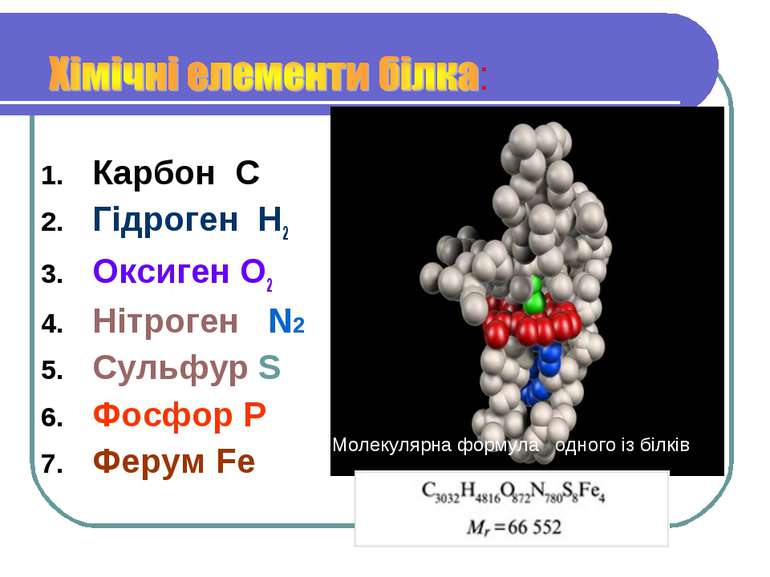
Карбон C Гідроген H2 Оксиген O2 Нітроген N2 Сульфур S Фосфор P Ферум Fe Молекулярна формула одного із білків
В склад білка входить 20 α - амінокислот, але залишки можуть багаторазово повторюватися в дуже різних варіантах тому існує величезна кількість білкових молекул, які мають велике значення в житті організму. Молекула інсуліна
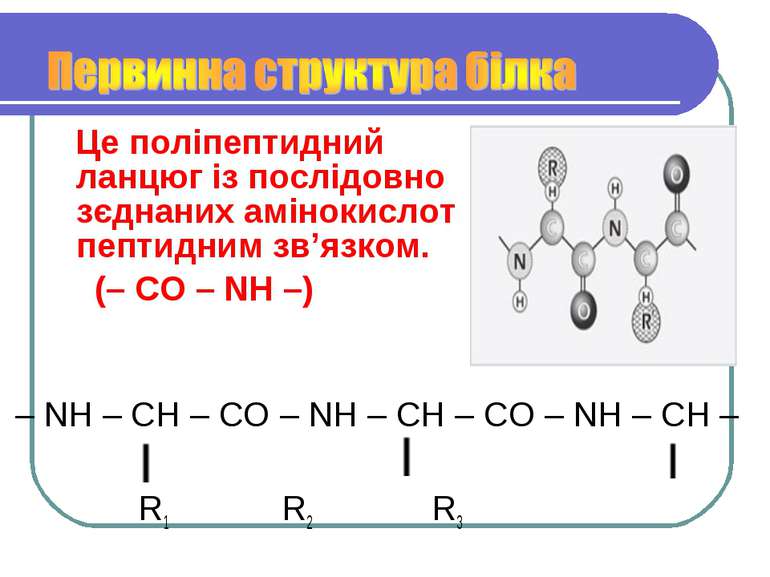
Це поліпептидний ланцюг із послідовно зєднаних амінокислот пептидним зв’язком. (– CO – NH –) – NH – CH – CO – NH – CH – CO – NH – CH – R1 R2 R3
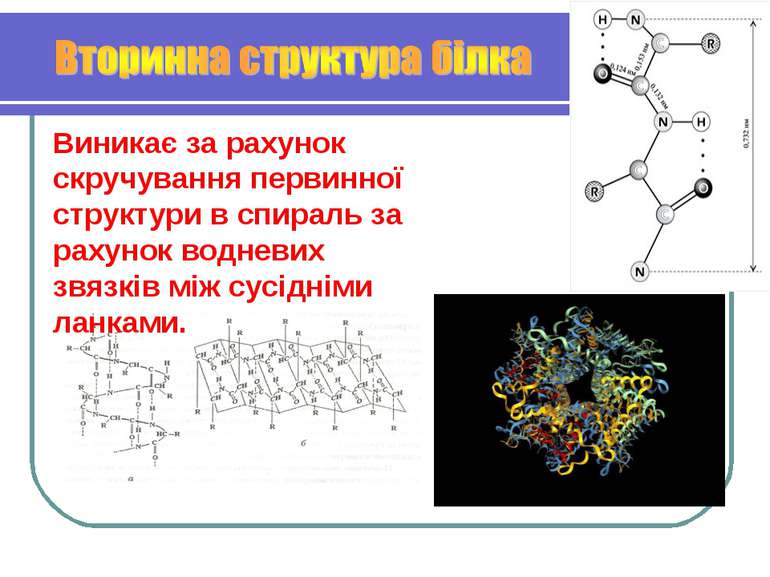
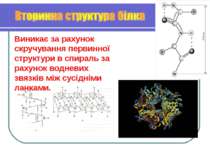
Виникає за рахунок скручування первинної структури в спираль за рахунок водневих звязків між сусідніми ланками.
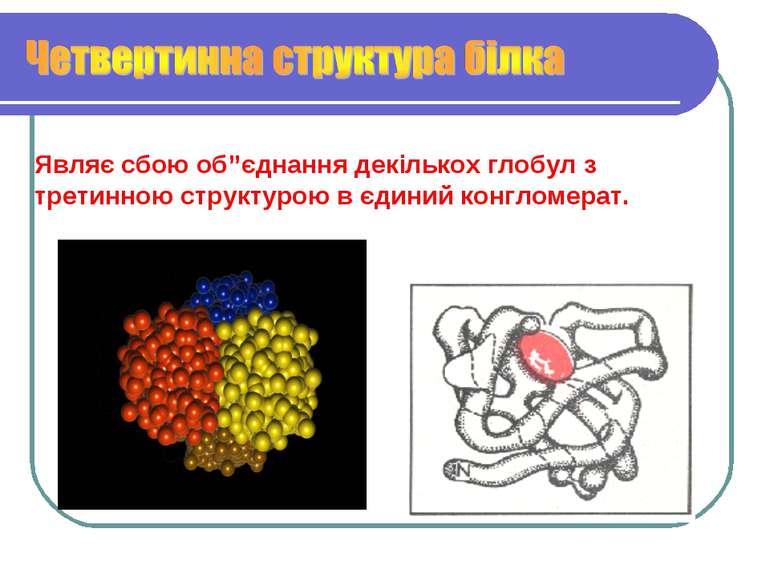
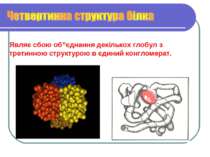
Це глобулярна форма утворена за рахунок гідрофобних зв’язків між радикалами амінокислот із вторинною структурою.
Кольорові (якісні) Денатурація – порушення структури білка Гідроліз – при нагрівані з основами чи кислотами..
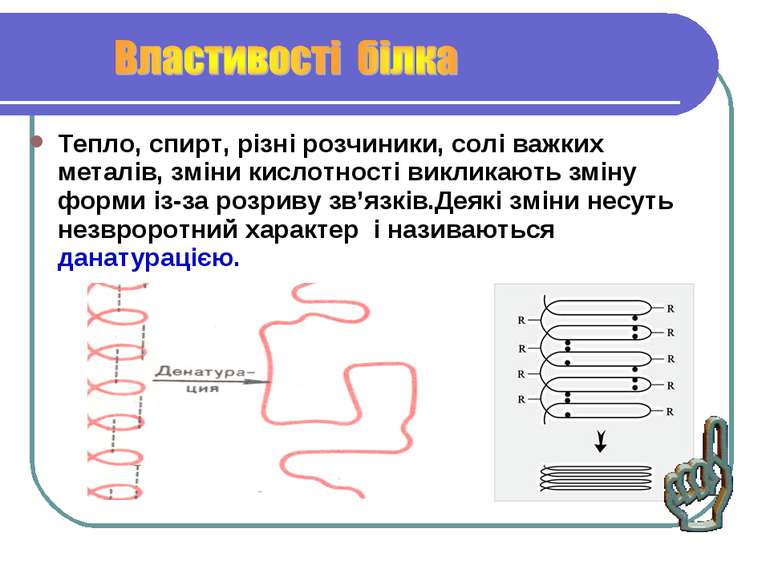
Тепло, спирт, різні розчиники, солі важких металів, зміни кислотності викликають зміну форми із-за розриву зв’язків.Деякі зміни несуть незвроротний характер і називаються данатурацією.
Ксантопротеїнова реакція В пробірку наливаємо 2 мл розчину білка і добавляємо по краплям 0,5 мл концентрованого розчину нітратної кислоти. Обережно нагріваємо пробірку і спостерігаємо зміну кольору. Розчин БіЛКА + HNO3 ? Жовтий колір вказує на присутність білків.
Біуретова реакція В пробірку з 2–3 мл розчину білка добавляємо 2–3 мл 10%-го розчину натрія гідроксиду. До одержаної суміші доливаємо 2–3 мл розчину міді(II) сульфату. Пробірку встряхните Розчин БіЛКА +NaOH + CuSO4 ? Червоно – фіолетове забарвлення вказує на присутність пептидної групи
В пробірку з розчином білка добавляємо плюмбума ацетата і натрію гідроксиду, підігріваємо Розчин білка + СН3СООРb+ NaOH ? Чорний колір вказує на присутність Сульфуру
Захисна Імуноглобуліни (антитіла) Фібриноген, тромбопластин, тромбін (зсідання крові) Транспортна Гемоглобін, гемоціанін, міоглобін Структурна астин (зв'язки) Колаген (хрящі, сухожилки) Олеїн (кістки) Кератини (нігті, пір'я)
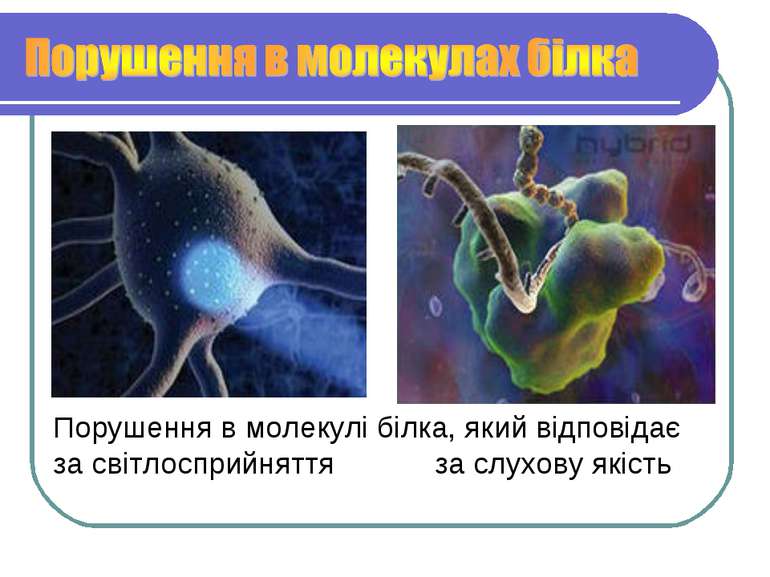
Сигнальна Родопсин (Через білки передаються сигнали і направляються у нервову систему) Скорочувальна (Скоротливі білки, забезпечують рух) Актин і міозин (м'язи) Тубулін (війки, джгутики, мікротрубочки
Запасаюча яєчний альбумін, Казеїн молока Енергетична (Розпадаються з виділенням енергії) 1 г білка утворює 17,2 кДж Регуляторна Гормони (інсулін, гормон росту) Каталітична Ферменти (Прискорюють хімічні реакції в клітині)
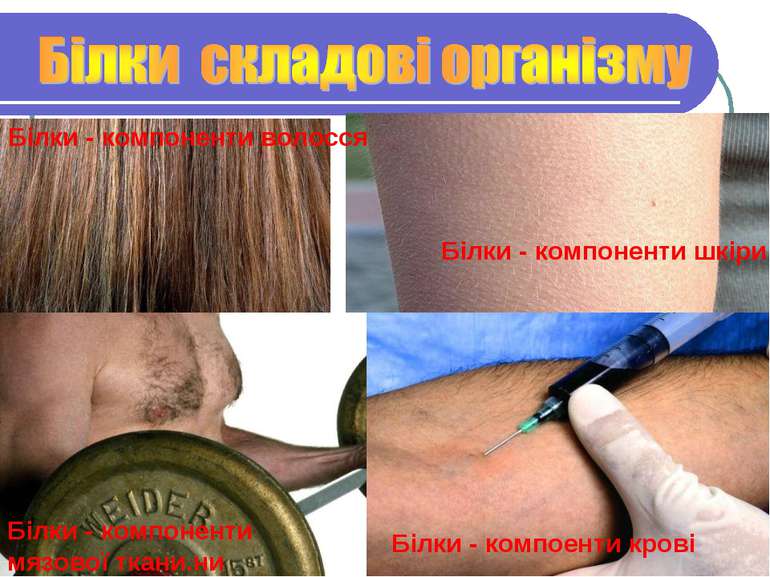
Білки - компоненти волосся Білки - компоненти шкіри Білки - компоненти мязової ткани.ни Білки - компоенти крові
10 днів - 50 % білків печінки і плазми крові 80 днів - 50 % білків людини 158 днів - білок мязів і шкіри людини Життя - 200 разів відновлюється білок організма людини. Вообще говоря, старые клетки на новые заменяются очень часто. Например, красные кровяные клетки ежемесячно полностью обновляются. Клетки, выстилающие стенки кишечника, обновляются еженедельно. Каждый раз, принимая ванну, мы сбрасываем с себя мертвые клетки кожи.
Видатним досягненням органічної хімії став синтез окситоцина. Цей гормон пептидної природи, стимулює виделеня молока молочними залозами, складається із залишків 9 амінокислот. Видатному американському біохіміку Винсенту Дю Виньо, який все своє життя присвятив вивченю гормонів, витамінів і антибіотиків, в 1932 р. вдалось встановити структуру окситоцина, а в 1954 р. здійснив його повний синтез із окремих амінокислот. За це відкриття йому в 1955 г. була присуджена Нобелівська премія
Більш прості пептиди в даний час синтезують хімічним або мікробіологічним шляхом. Наприклад, синтезовано заміна цукру в харчовій промисловості.Він має назву аспартам. На етикетках з дешевими газованими напоями він позначається кодом Е951 (його добавляють також в жуйку). По хімічній будові аспартам являє собою дипептид, утворений аспарагіновою кислотою і метиловим ефіром фенілаланіна
Схожі презентації
Категорії