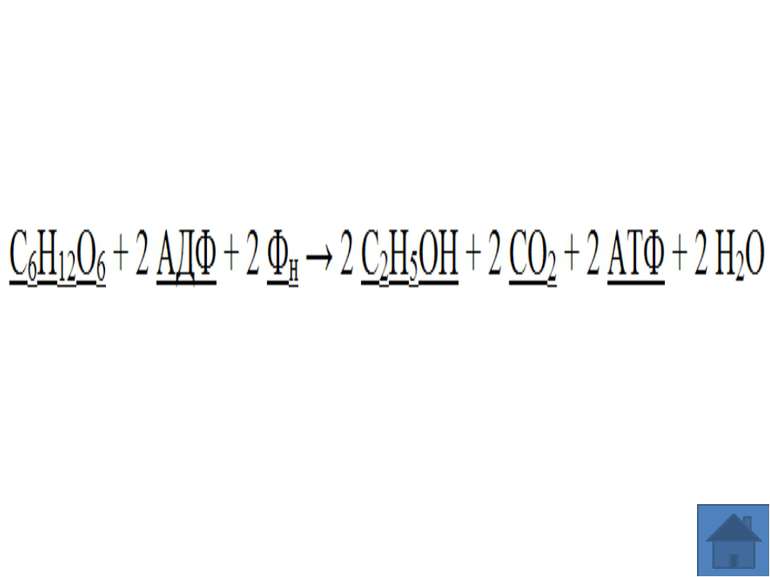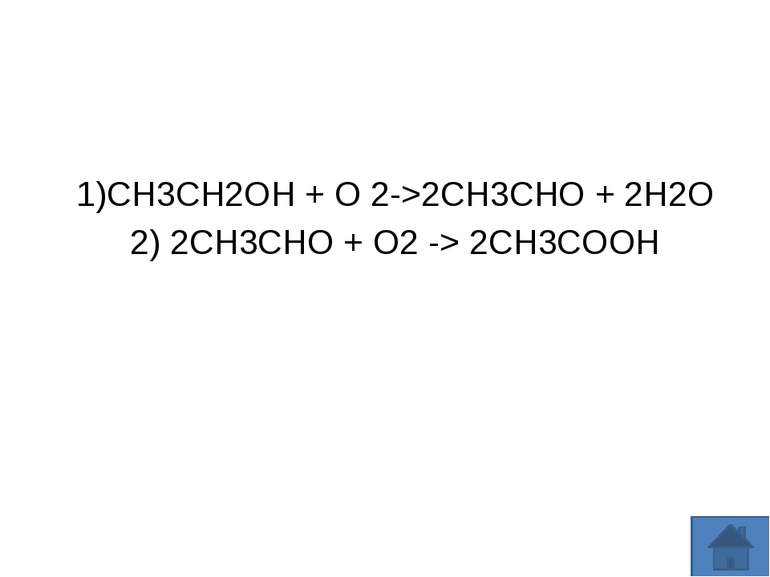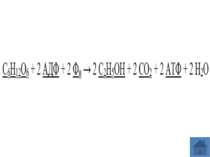Презентація на тему:
Бродіння. Види бродіння
Завантажити презентацію
Бродіння. Види бродіння
Завантажити презентаціюПрезентація по слайдам:
Броді ння, шумува ння — біохімічний процес розкладу вуглеводів, що відбувається під впливом мікроорганізмів або їх ферментів Бродіння (біохімія) (також зброджування, ферментація), - це анаеробний метаболічний розпад молекул (наприклад, глюкози) за допомогою мікроорганізмів. Найчастіше, кажучи про бродіння, мають на увазі перетворення цукру на спирт за допомогою дріжджів, але, наприклад, при виробництві кефіру використовується бродіння за допомогою інших бактерій.
Є такі види броддіння: - Спиртове бродіння - Молочнокисле бродіння - Метанове бродіння Пропіоновокисле бродіння Маслянокисле бродіння Лимоннокисле бродіння Оцтове бродіння
Спиртове бродіння — тип процесу бродіння, під час якого глюкоза перетворюється доетилового спирту та вуглекислого газу. Дозволяє отримати два моль АТФ на моль глюкози в анаеробних умовах. Загальне рівняння спиртового бродіння: C6H12O6 + 2 АДФ + 2 Фн → 2 C2H5OH + 2 CO2 + 2 АТФ + 2 H2O Цей метаболічний шлях характерний для багатьох грибів (дріжджів, дріжджеподібних і деяких цвілевих грибків), водоростей, найпростіших та деяких бактерій. Спиртове бродіння здавна використовується людиною у процесі хлібопекарства (спричиняє «сходження»дріжджового тіста) та виготовлення алкогольних напоїв. Однією із нових галузей застосування цього метаболічного шляху є виробництво етанолу як відновного і відносно недорого біопалива.
Використання спиртового бродіння: Виробництво алкогольних напоїв Хлібопекарство -Виробництво біопалива - Виробництво гліцеролу
Виробництво алкогольних напоїв Спиртове бродіння здавна використовується для виробництва алкогольних напоїв, таких як вино, пиво, ель. Джерелом вуглеводів для цих процесів можуть слугувати різноманітні рослини. Частина з них містять готові до зброджування моно- та олігосахариди: наприклад сахароза і фруктоза у виноградному соці. В такому випадку ферментація може починатись без попередньої обробки. З іншого боку зернові, такі як пшениця, овес, рис тощо та інші продукти, що містять крохмаль, спочатку повинні пройти процес гідролізу полісахаридів. Продуктом гідролізу є сусло, яке вже містить цукри готові до зброджування. Бродіння мусту під час виробництва вина
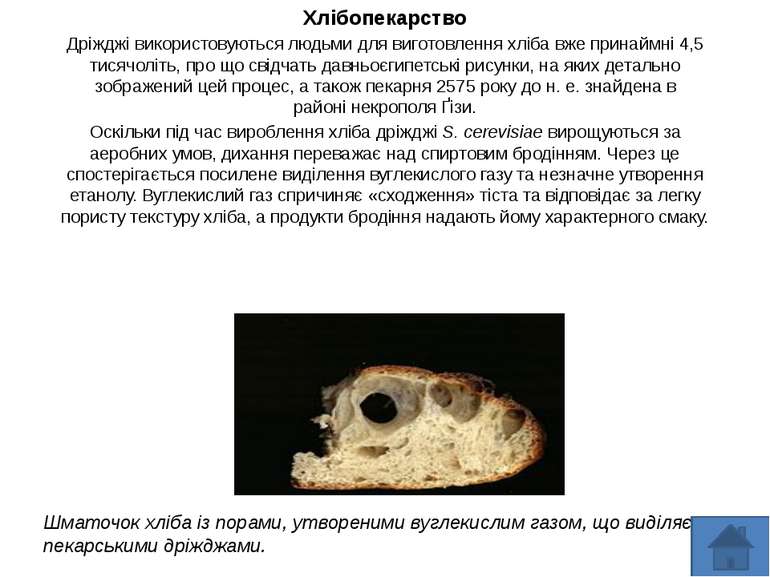
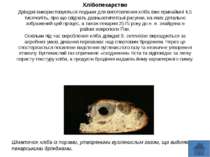
Хлібопекарство Дріжджі використовуються людьми для виготовлення хліба вже принаймні 4,5 тисячоліть, про що свідчать давньоєгипетські рисунки, на яких детально зображений цей процес, а також пекарня 2575 року до н. е. знайдена в районі некрополя Ґізи. Оскільки під час вироблення хліба дріжджі S. cerevisiae вирощуються за аеробних умов, дихання переважає над спиртовим бродінням. Через це спостерігається посилене виділення вуглекислого газу та незначне утворення етанолу. Вуглекислий газ спричиняє «сходження» тіста та відповідає за легку пористу текстуру хліба, а продукти бродіння надають йому характерного смаку.
Виробництво біопалива Етанол, отриманий у процесі спиртового бродіння, може бути використаний як недороге і відновлюване джерело енергії. Як сировину для виробництва етанолового біопалива використовується рослинний матеріал, багатий на сахарозу, крохмаль або целюлозу: кукурудзу, пшеницю, цукровий буряк і тростину, солому, відходи деревообробної промисловості, побутові відходи рослинного походження тощо. Зазвичай сировину хімічно обробляють з метою гідролізу полісахаридів до мономерів, після чого до отриманої маси додають витривалі штами дріжджів.
Виробництво гліцеролу Під час Другої світової війни Німеччина мала велику потребу у гліцеролі, для виготовлення вибухової речовини нітрогліцеролу. Імпорт гліцеролу був обмежений британською морською блокадою, тому здійснювались спроби налагодити власне виробництво. На той час було відомо, що гліцерол у невеликих кількостях утворюється під час спиртового бродіння за участі S. cerevisiae. Німецький вчений Карл Нойберг знайшов спосіб модифікувати процес таким чином, щоб вихід цієї речовини був значно вищим. Для цього він додав у середовище із дріжджами 3,5 % сульфіту натрію при pH 7,0. Бісульфіт іони утворюють комплекс із ацетальдегідом, внаслідок чого останній стає недоступним для відновлення до етанол. Оскільки дріжджі однаково потребують акцептора електронів та водню, вони використовують із цією метою один із проміжних продуктів гліколізу —дигідроксиацетонфосфат, що відновлюється до гліцеролфосфату. Останній перетворюється у гліцерол внаслідокдефосфорилювання. Це відкриття дозволило Німеччині отримувати близько 1000 тон гліцеролу на місяць, завдяки тому, що більшість пивоварень було перетворено на фабрики по виробництву цієї речовини. Після настання миру такий шлях одержання гліцерину не був економічно конкурентоспроможним і тому припинився. Формула гліцеролу
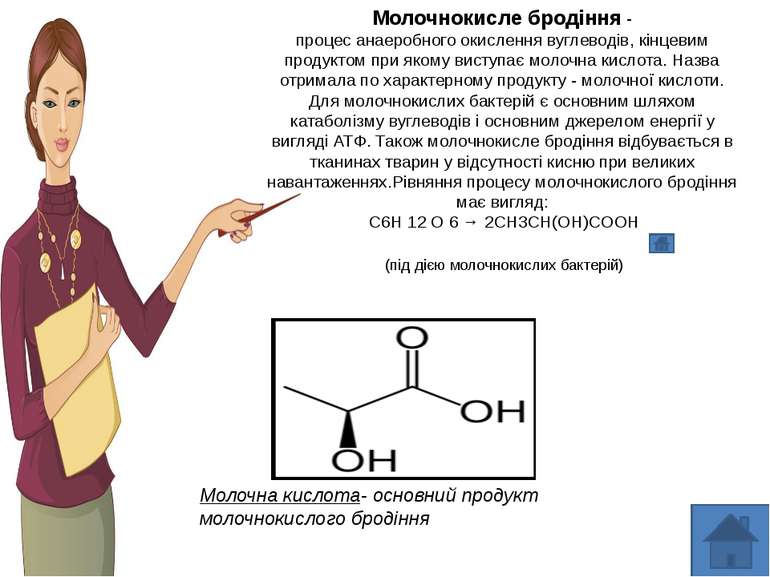
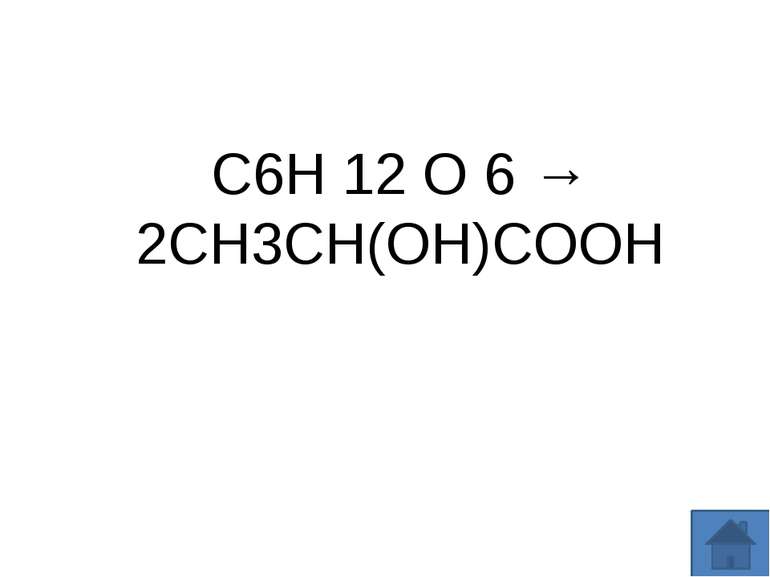
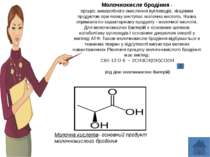
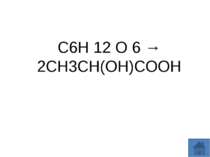
Молочнокисле бродіння - процес анаеробного окислення вуглеводів, кінцевим продуктом при якому виступає молочна кислота. Назва отримала по характерному продукту - молочної кислоти. Для молочнокислих бактерій є основним шляхом катаболізму вуглеводів і основним джерелом енергії у вигляді АТФ. Також молочнокисле бродіння відбувається в тканинах тварин у відсутності кисню при великих навантаженнях.Рівняння процесу молочнокислого бродіння має вигляд: C6H 12 O 6 → 2CH3CH(OH)COOH (під дією молочнокислих бактерій)
Види молочнокислого бродіння: -Гомоферментативне молочнокисле бродіння. -Гетероферментативне молочнокисле бродіння. Значення молочнокислого бродіння для людини
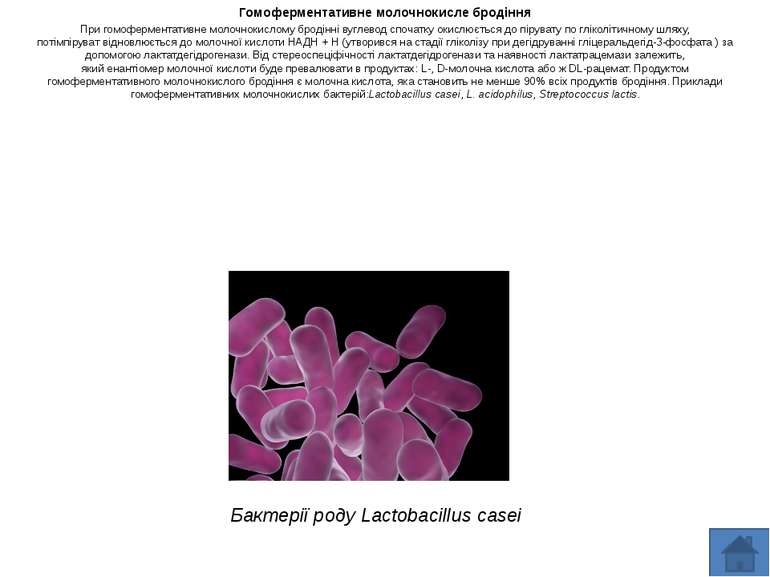
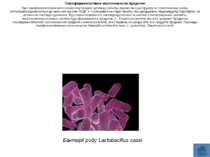
Гомоферментативне молочнокисле бродіння При гомоферментативне молочнокислому бродінні вуглевод спочатку окислюється до пірувату по гліколітичному шляху, потімпіруват відновлюється до молочної кислоти НАДН + Н (утворився на стадії гліколізу при дегідруванні гліцеральдегід-3-фосфата ) за допомогою лактатдегідрогенази. Від стереоспеціфічності лактатдегідрогенази та наявності лактатрацемази залежить, який енантіомер молочної кислоти буде превалювати в продуктах: L-, D-молочна кислота або ж DL-рацемат. Продуктом гомоферментативного молочнокислого бродіння є молочна кислота, яка становить не менше 90% всіх продуктів бродіння. Приклади гомоферментативних молочнокислих бактерій:Lactobacillus casei, L. acidophilus, Streptococcus lactis.
Гетероферментативне молочнокисле бродіння На відміну від гомоферментативного бродіння, деградація глюкози йде по пентозофосфатному шляху, гліцеральдегид-3-фосфат що утворюється з ксилулозо-5-фосфату окислюється до молочної кислоти, а ацетілфосфат відновлюється до етанолу (деякі гетероферментативні молочнокислі бактерії окислюють отриманий етанол частково або повністю до ацетату). Таким чином, при гетероферментативному молочнокислому бродінні утворюється більше продуктів: молочна кислота, оцтова кислота, етанол, двоокис вуглецю. приклади гетероферментативних молочнокислих бактерій: L. fermentum , L. brevis , Leuconostoc mesenteroides , Oenococcus oeni.
Значення молочнокислого бродіння для людини Молочнокисле бродіння використовується для консервації продуктів харчування (за рахунок інгібування росту мікроорганізмів молочною кислотою і зниження рН) з метою тривалого збереження (приклад — квашення овочів, сирокопчення), приготуванні кисломолочних продуктів (кефіру , ряжанки , йогурту, сметани), силосуванні рослинної маси, а також біотехнологічного способу виробництва молочної кислоти.
Мета нове броді ння — метод біотехнології, що полягає ферментаційному перетворюванні біоценозом анаеробних мікроорганізмів більшості органічних полімерних та інших сполук на біометан і вуглекислий газ. Це один з відомих методівочищення стічних вод, обробки осадів первинних відстійників і надлишкового активного мулу очисних споруд каналізації. У біотехнології анаеробного ферментування використовуються герметичні резервуари — метантенки. У результаті життєдіяльності біоценозу метантенка відбувається зниження концентрації органічних речовин і утворення екологічно чистого палива — біогазу. Для отримання біогазу можуть використовуватися відходи сільського господарства, стоки переробних підприємств, що містять цукор, побутові відходи, стічні води міст, спиртних заводів і т.д.
Принцип метанового бродіння Біотехнологія методу включає в себе чотири біохімічні стадії, які, хоча і можуть проводитися в одному резервуарі, виконуються різними типами мікроорганізмів: -Гідроліз за допомогою бактерій складних вхідних полімерних матеріалів на прості розчинні сполуки, доступні інших мікроорганізмам; -ацидогенез, тобто перетворення цукрів та амінокислот на вуглекислий газ, водень, аміак і органічні кислоти -ацетогенез, тобто перетворення органічних кислот на оцтову кислоту, аміак, водень, та вуглекислий газ -метаногенез, тобто перетворення археями-метаногенами цих продуктів на метан і вуглекислий газ. Метанове бродіння ефективніше для перероблення відходів за звичайні аеробні методи. Хоча процес був відомий з середини 20 століття, він отримав значну увагу лише в 21 столітті через збільшення економічної вигоди від нього за рахунок отримання палива.
Переваги анаеробного методу очищення стічних вод Перевагами анаеробного методу є низька енергозатратність (енергоспоживання процесів анаеробного очищення становить ~ 10% від енергоспоживання аеробного очищення), високі навантаження, одержання метану як енергоносія, утворення невеликої кількості надлишкового мулу, невеликі площі для споруд, можливість застосування модулів доочищення, а вартість анаеробного очищення становить суму в 13 разів меншу, ніж аеробного.
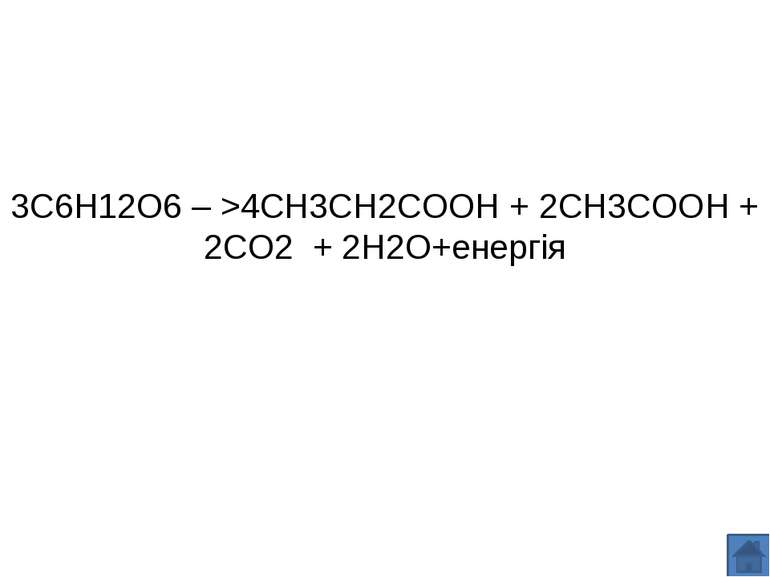
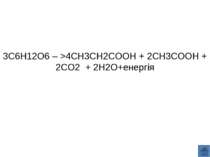
3C6H12O6 – >4CH3CH2COOH + 2CH3COOH + 2CO2 + 2H2O+енергія Пропіоновокисле бродіння — це метаболічний шлях анаеробного перетворення вуглеводів тамолочної кислоти, що здійснюється деякими бактеріями, зокрема представниками родини Propionibacteriaceae, кінцевими продуктами якого є пропіонова та оцтова кислоти та вуглекислий газ. Бактерії, для яких характерне пропіоновокисле бродіння, використовуються у процесі виробництва швейцарських сортів сиру. Виділення кислот і газу цими мікроорганізмами важливе для остаточного формування смаку та утворення «вічок» у цих сирах. Формула пропіонокислого бродіння:
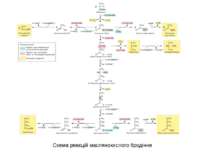
Використання пропіоновокислого бродіння у: -Виробництві сиру -Хлібопеченні -Синтезі вітаміну B12 Схема реакції пропіоновокислого бродіння.
Сировиробництво – найбільш давня біотехнологія, яка використовує біохімічну активність пропионових бактерій. Високі органолептичні властивості мають тверді сичужні під час виготовлення яких використовуються пропіоновокислі бактерії. Загальне правило, що стосується використання цих бактерій в дозріванні сирів, говорить: шкідливий як недолік, і надлишок бактерій. Основна роль пропионовокислих бактерій в дозріванні сирів полягає у використанні лактатів, освічених молочнокислими бактеріями при зброжувані лактози молока,потім лактати перетворюються на пропіонову та оцтову кислоти й CO2. Кислоти забезпечують гострий смак сирів. За рахунок виділення CO2 утворюються очка.
Використання пропіоновокислого бродіння у хлібопеченні Пропіоновокислі бактерії також застосовують у хлібопеченні. Їх поруч із молочнокислими бактеріями і дріжджами вводять у деякі закваски для тіста з метою створення у процесі ферментації, крім молочної і оцтової кислот, ще й пропіонової. При внесенні в тісто такої закваски хліб містить 0,1% оцтової, 0,2% молочної, 0,1%пропіоновї кислоти (відносно борошна). Такої кількості пропіонової кислоти достатньо щоб проявилась фунгіцидна дія, без помітного впливу на смак та запах хліба
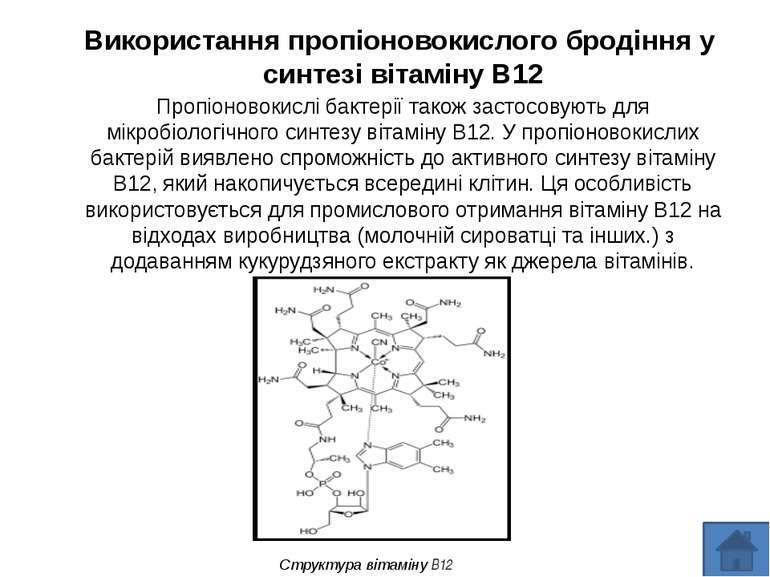
Використання пропіоновокислого бродіння у синтезі вітаміну B12 Пропіоновокислі бактерії також застосовують для мікробіологічного синтезу вітаміну B12. У пропіоновокислих бактерій виявлено спроможність до активного синтезу вітаміну B12, який накопичується всередині клітин. Ця особливість використовується для промислового отримання вітаміну B12 на відходах виробництва (молочній сироватці та інших.) з додаванням кукурудзяного екстракту як джерела вітамінів.
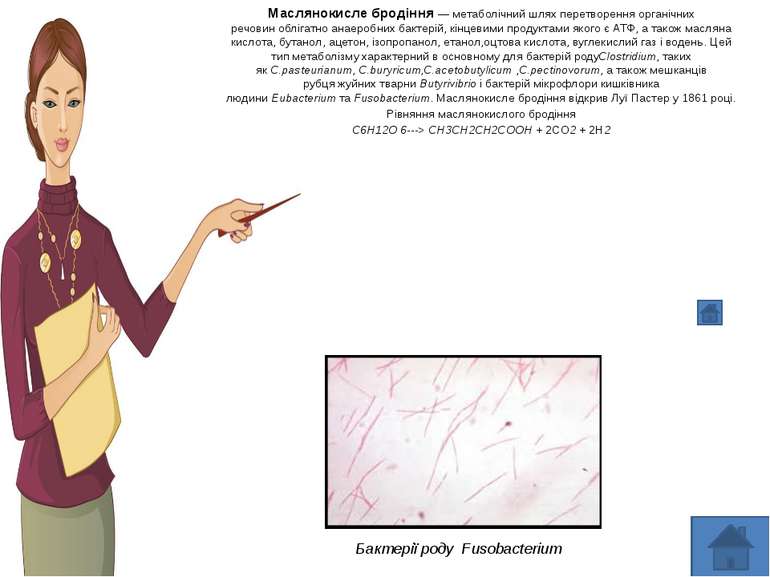
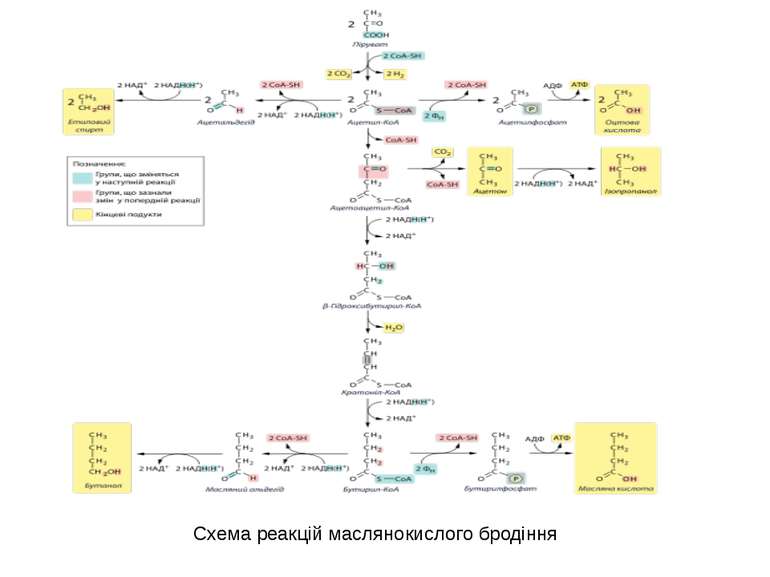
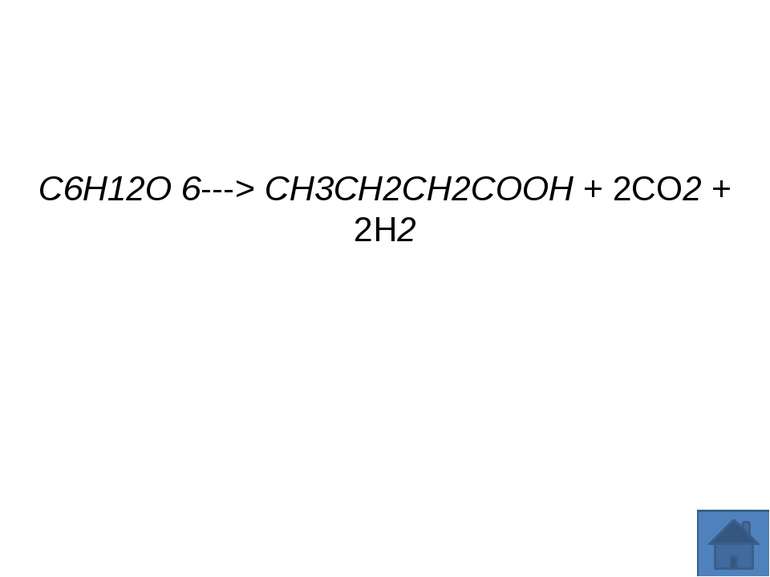
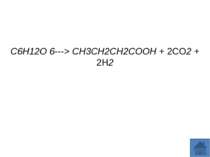
Маслянокисле бродіння — метаболічний шлях перетворення органічних речовин облігатно анаеробних бактерій, кінцевими продуктами якого є АТФ, а також масляна кислота, бутанол, ацетон, ізопропанол, етанол,оцтова кислота, вуглекислий газ і водень. Цей тип метаболізму характерний в основному для бактерій родуClostridium, таких як C.pasteurianum, C.buryricum,C.acetobutylicum ,C.pectinovorum, а також мешканців рубця жуйних тварни Butyrivibrio і бактерій мікрофлори кишківника людини Eubacterium та Fusobacterium. Маслянокисле бродіння відкрив Луї Пастер у 1861 році. Рівняння маслянокислого бродіння C6H12O 6---> CH3CH2CH2COOH + 2CO2 + 2H2
- Історія відкриття маслянокислого бродіння - Реакції маслянокислого бродіння - Використання маслянокислого бродіння у харчовій промисловості -
Історія відкриття маслянокислого бродіння Використання маслянокислого бродіння у промислових масштабах почалось під час Першої світової війни. Британці потребували великої кількості органічних розчинників бутанолу (для виробництва штучної ґуми) та ацетону (як розчинник нітроцелюлози у процесі виготовлення бездимного вибухового пороху кордиту). Ці речовини добували методом піролізу деревини, при чому на виготовлення однієї тонни ацетону потрібно було витрати 80—100 т берези, буку або клену. У 1915 році молодий вчений Хаїм Вейцман розробив метод бродіння за допомогою бакетрії Clostridium acetobutylicum, який дозволяв перетворювати 100 т меляси у 12 т ацетону та 24 т бутанолу. Пізніше він вдосконалив цей метод, знайшовши штам бактерій, що виділяв особливо багато потрібних розчинників. Ацетон та бутанол отримували шляхом малсянокислого бродіння до 1950—1940 років, коли цей метод був замінений дешевшим.
Реакції маслянокислого бродіння Глюкозу та інші гекосози маслянокислі бактерії розкладають по гліколітичному шляху. Піруват, що утворюється декарбоксилюється до ацетил-КоА, цей процес супроводжується виділенням вуглекислого газу та відновленням ферредоксину, який взаємодіє із гідрогеназою, внаслідок чого утворюється водень. Ацетил-КоА є високоенергетичною сполукою, і йогоенергії достатньо для фосфорилювання АДФ, тому у частині цих молекул залишок коферменту А замінюється на фосфатну групу, яка згодом переноситься на АДФ. Ця гілка маслянокислого бродіння енергетично вигідна, оскільки дозволяє отримати 4 моль АТФ на моль глюкози (2 моль в реакціях гліколізу, ще два — під час утворення оцтової кислоти), проте вона має два суттєвих недоліки: по-перше метаболізм глюкози цим шляхом призводить до дуже різкого закислення середовища, внаслідок чого ріст бактерій може пригнічуватись, по-друге, цей шлях не дозволяє клітині окиснити відновлені переносники електронів НАДН, що утворились в ході гліколізу. Якщо внаслідок виділення органічних кислот у процесі маслянокислого бродіння pH опускається нижче 4,4 у бактерій активуються шляхи, кінцевими продуктами яких є етанол, ацетон та бутанол. В кожному із цих шляхів використовується НАДH, проте жоден із них не дає більше двох моль АТФ на моль глюкози.
Використання маслянокислого бродіння у харчовій промисловості У харчовій промисловості маслянокисле бродіння використовується для промислового отримання масляної кислоти яка має неприємний запах прогірклого масла, а її ефіри мають приємний фруктовий аромат і використовуються в кондитерській, безалкогольній, парфумерній промисловості. Ці бактерії можуть бути шкідливими. Вони викликають масову загибель картоплі, бомбаж консервів, прогіркання молока
Лимоннокисле бродіння — окислення вуглеводів, деяких спиртів і органічних кислот до лимонної кислоти плісневими грибами з родів Aspergillus і Penicillum. Окрім лимонної кислоти, при лимоннокислому бродінні утворюються невелика кількість глюконової і щавлевої кислот. Спочатку з вуглеводів гриб утворює піровиноградну кислоту, яка потім перетворюється на щавлевооцетову кислоту; остання за участю ферменту цитратсинтази конденсується з ацетатом за участю кофермента А з утворенням лимонної кислоти. Промислове здобуття лимонної кислоти базується на зброджуванні грибом Aspergillus niger розчину сахарози або меляси. У перерахунку на спожитий цукор утворюється 70—75% лимонної кислоти. Хімізм лимоннокислого бродіння 2C6H12O612+3O2→2C6H8O7+4H2O
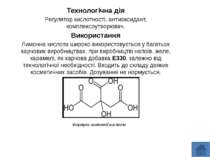
Лимонна кислота Технологічна дія та використання лимонної кислоти Побічна дія лимонної кислоти, ризик для здоровя людини, заходи безпеки.
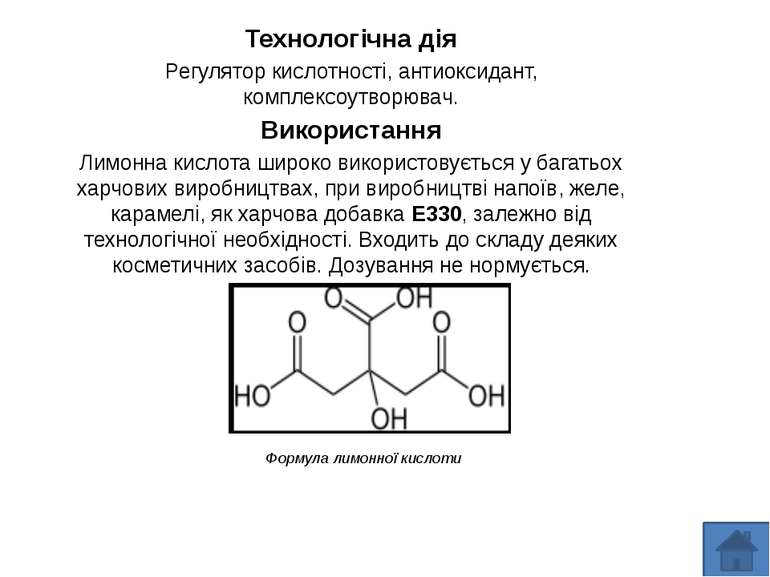
Технологічна дія Регулятор кислотності, антиоксидант, комплексоутворювач. Використання Лимонна кислота широко використовується у багатьох харчових виробництвах, при виробництві напоїв, желе, карамелі, як харчова добавка Е330, залежно від технологічної необхідності. Входить до складу деяких косметичних засобів. Дозування не нормується.
Побічна дія Стимулює розвиток алергічних реакцій, може викликати утворення злоякісних пухлин. Ризик для здоров'я людини Код ризику: R36/37/38, — лимонна кислота подразнює очі, органи дихання та шкіру. Заходи безпеки Якщо лимонна кислота потрапить в очі, їх одразу слід промити великою кількістю води та звернутися до лікаря; з цією речовиною слід працювати в захисних рукавицях, засобах захисту очей та лиця; якщо приміщення недостатньо вентилюється, слід захистити органи дихання респіратором, ефективним для даної речовини.
Оцтовокисле бродіння — це процес окиснення оцтовими бактеріями етилового спирту в оцтову кислоту. Найчастіше оцтовим бродінням уражаються вина. Харчові продукти, після оцтового бродіння мають запах оцтової кислоти, стають мутними і навіть ослизнюються. Оцтове бродіння покладено в основу виробництва оцтової кислоти для побутового споживання. Оцтовокисле бродіння проходить у 2 стадії 1)CH3CH2OH + O 2->2CH3CHO + 2H2O 2) 2CH3CHO + O2 -> 2CH3COOH
О цтова кислота (ацетат), CH3COOH, відома людству з прадавніх часів, знаходиться у низьких коцентраціях в багатьох рослинних та тваринних системах. Оцет, 4 - 12 % розчин оцтової кислоти у воді, як продукт ферментації вина набув широкого використування більш ніж 5000 років тому. Оцтова кислота є прозорою, безбарвною рідиною, що має різкий запах та небезпечну наривну дію. Утворює з металами солі — ацетати. Плавиться за 16,75 °C, кипить за 117,9 °C за нормального тиску. Оцтова кислота — один з базових продуктів промислового органічного синтезу. Більш ніж 65 % світового виробництва оцтової кислоти іде на виготовлення полімерів, похідних целюлози та вінілацетату. Полівінілацетат є основою багатьох ґрунтівних покрить та фарб. З ацетатної целюлози виготовляють ацетатне волокно. Оцтова кислота та її естери важливі промислові розчинники та екстрагенти.
Застосування оцтової кислоти Застосування оцтової кислоти досить різноманітне. У хімічній промисловості з неї виробляють пластичні маси, різні барвники, лікарські речовини, штучне волокно (ацетатний шовк), незаймисту кіноплівку та багато інших речовин. Солі оцтової кислоти – ацетати алюмінію, хрому, феруму – застосовують як протраву при фарбуванні тканин. Оцтова кислота має широке застосування і як розчинник. У харчовій промисловості застосовується як консервувальний засіб та смакова приправа. Застосовується при солянокислотних обробленнях привибійних зон пласта як стабілізатор (з метою стабілізації продуктів реакції) від випадання трудновилучуваних гелеподібних сполук заліза (осаду). Залежно від вмісту заліза в кислотному розчині (від 0,01 до 0,5%) беруть 1-3% О. к. Для приготування робочих розчинів використовують О. к. синтетичну і О. к. лісохімічну технічну очищену. Товарний реагент – це водний розчин О. к. різної концентрації, від якої залежать густина і температура застигання (має складний характер залежності).
Схожі презентації
Категорії