Презентація на тему:
Вчення про антибіотики. Основи раціональної хіміотерапії інфекційних захворювань
Завантажити презентацію
Вчення про антибіотики. Основи раціональної хіміотерапії інфекційних захворювань
Завантажити презентаціюПрезентація по слайдам:
Кафедра медичної біології, мікробіології, вірусології та імунології Вчення про антибіотики. Основи раціональної хіміотерапії інфекційних захворювань Лектор – проф. Климнюк С.І.
План лекції 1. Історія вчення про антибіотики. 2. Класифікації антибіотиків. 3. Методи визначення чутливості бактерій до антибіотиків. 4. Помилки при визначенні АБ-чутливості. 5. Ускладнення антибіотикотерапії. 6. Природа антибіотикорезистентності.
За даними ВООЗ інфекційні захворювання є серйозною загрозою для людства: “Ми знаходимось на порозі глобальної кризи в області інфекційних захворювань. Жодна країна світу не може бути застрахованою від них і не може собі дозволити ігнорувати цю загрозу”.
Згідно статистики ВООЗ, серед інфекційних захворювань, що зареєстровані в світі, наймасовішими були: інфекції, які супроводжуються діареєю,- 4 млрд випадків, малярія - 500 млн, гострі інфекції дихальних шляхів - 395 млн, венеричні захворювання - 330 млн, кір - 42 млн, кашлюк - 40 млн туберкульоз - 1,5 млрд інфікованих ВІЛ-інфіковані – ~ 50 млн осіб
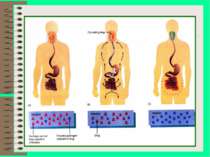
Л. Пастер В основі відкриття лежить явище бактеріального антагонізму. Воно характеризується тим, що один вид мікроорганізмів (бактерії, актиноміцети, гриби, водоростей) здатний пригнічувати або затримувати ріст інших.
З. Ваксман Виділив стрептоміцин у 1944 р. Увів термін “антибіотик” у 1942 р. За його визначенням це хімічні речовини, що утворюються мікробами, і здатні пригнічувати ріст або руйнувати бактерії та інші мікроорганізми.
Сульфонаміди Gerhard Domagk отримує Нобелівську премію з медицини, 1939 р. У 1930-х роках відкрив протимікробний ефект пронтозилу – попередника сульфонамідів
Антибіотики - це хіміотерапевтичні засоби, що утворюються мікроорганізмами або отримані з інших природних джерел, а також їх похідні та синтетичні продукти, що мають здатність вибірково пригнічувати в організмі хворого збудників захворювань.
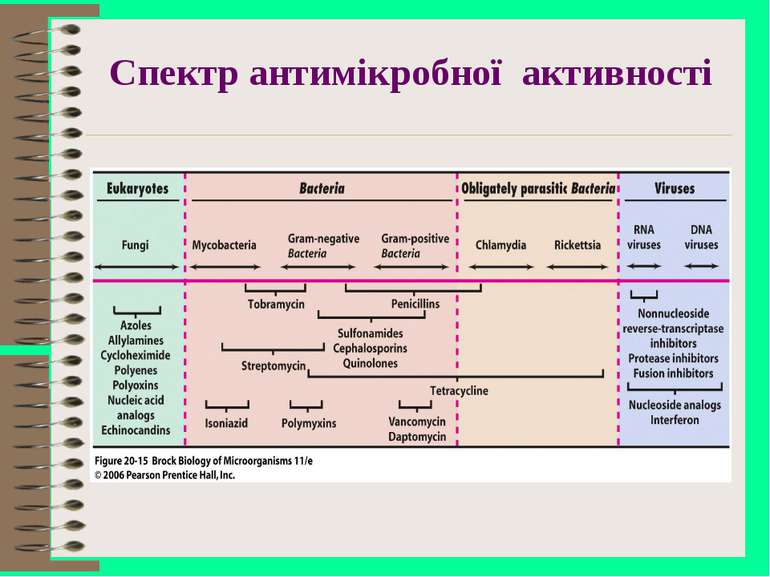
Антибіотики мають характерні особливості, що відрізняють їх від інших продуктів життєдіяльності: висока біологічна активність: пеніцилін вже у концентрації 0,000001 г/мл проявляє чітко виражену бактерицидну дію на бактерії. вибіркова специфічність: антибіотик проявляє активність тільки по відношенню до певних груп організмів, не завдаючи шкоди іншим.
За типом антимікробної дії антибіотики поділяються на: бактерицидні (пеніциліни, стрептоміцин, цефалоспорини, поліміксини); бактеріостатичні (тетрацикліни, левоміцетин, макроліди). Такий поділ антибіотиків має певне значення при виборі тактики лікування. При легкому і середньому ступеню тяжкості й перебігу інфекцій для забезпечення терапевтичного ефекту часто достатньо застосування антибіотиків бактеріостатичного типу, так як вважається, що захисні сили організму довершать розпочату антибіотиками справу.
До препаратів, що використовуються в лікарській практиці, ставляться певні вимоги: висока вибірковість антимікробного ефекту в дозах, нетоксичних для організму; відсутність або повільний розвиток резистентності збудників до препарату під час його застосування; збереження антимікробного ефекту в рідинах організму, ексудатах, тканинах, відсутність або низький рівень зв’язування білками сироватки крові, інактивації тканинними ферментами;
До препаратів, що використовуються в лікарській практиці, ставляться певні вимоги: всмоктування, розподіл і виведення препарату, що забезпечують терапевтичні концентрації в крові, тканинах, рідинах (в тому числі лікворі), які повинні швидко досягаються і підтримуються протягом тривалого періоду; особливого значення набуває створення високих концентрацій препарату в сечі, жовчі, калі, вогнищах ураження; зручна лікарська форма, яка забезпечує максимальний ефект, і залишається стабільною при звичайних умовах зберігання.
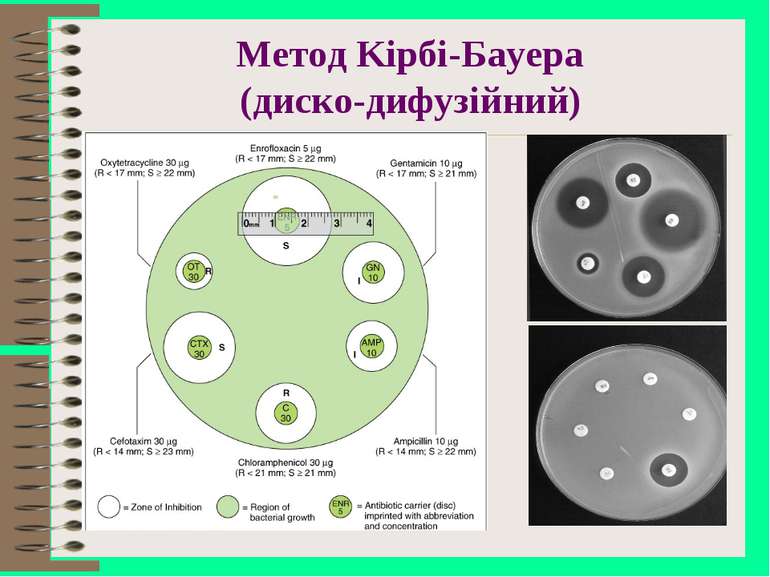
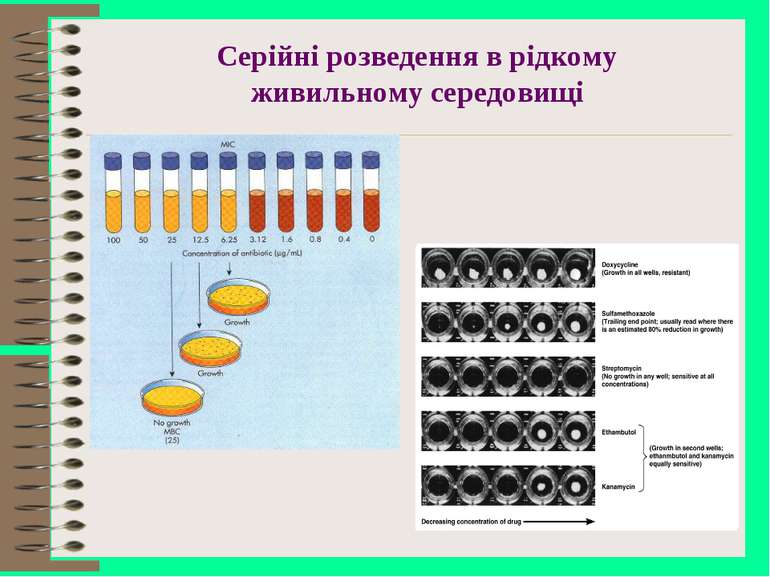
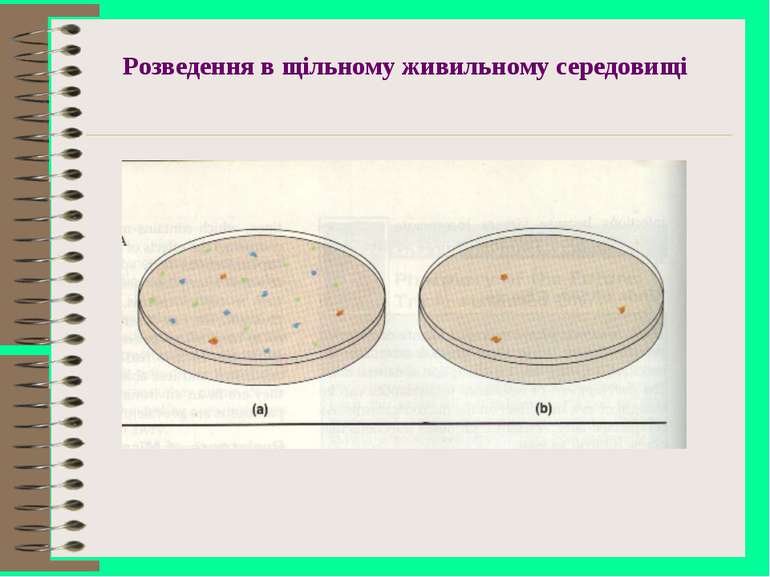
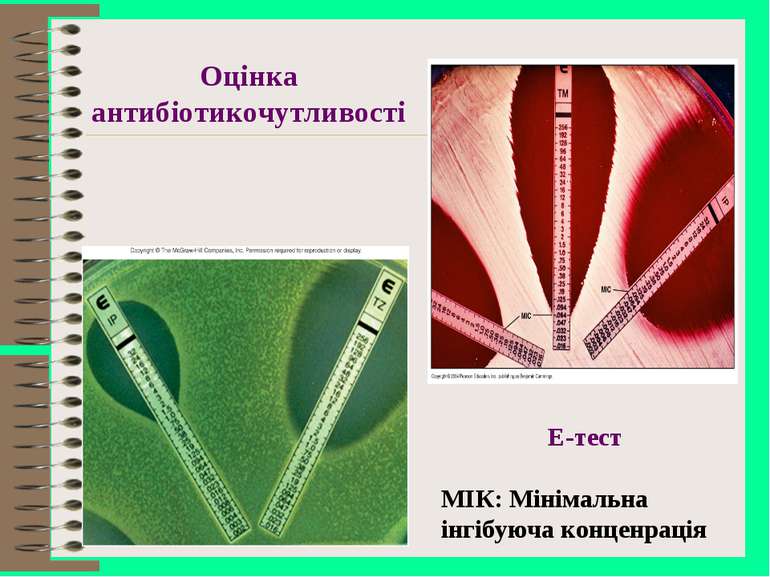
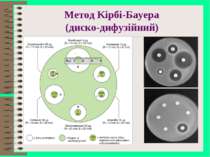
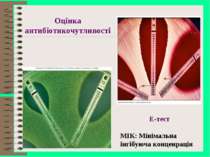
Лабораторні методи вивчення чутливості мікроорганізмів до антибіотиків диско-дифузійний, метод дисків серійних розведень прискорені методи
Живильні середовища для визначення чутливості бактерій до антибіотиків повинні відповідати таким вимогам: бути стандартними та забезпечувати оптимальні умови росту мікроорганізмів; не містити інгібіторів бактеріального росту і великої кількості стиму-ляторів; не мати речовин, що пригнічують активність препаратів.
Прискорені методи визначення чутливості мікроорганізмів до антибіотиків · визначення змін ферментативної активності мікроорганізмів під впливом антибіотиків; · визначення кольору редокс-індикаторів при зміні окисно-відновного потенціалу під час росту бактерій у живильному середовищі; цитологічна оцінка змін морфології бактеріальних клітин під впливом антибіотиків; автоматизоване
Помилки при визначенні антибіотикочутливості: - використання при посіві не чистої культури бактерій, а патологічного матеріалу; - збудники із встановленою антибіотикограмою і чутливі до певних препаратів часто елімінуються з організму в процесі лікування (при змішаній або суперінфекції); - незважаючи на чутливість збудника до антибіотика, терапія неефективна внаслідок їх внутрішньоклітинного розміщення і поганого проникнення препаратів всередину клітини; можливість інактивації антибіотиків ферментними системами організму, зв’язування білками сироватки крові і тканин, некротичними масами; погане проникненням препарату у вогнище інфекції внаслідок недостатнього кровопостачання останнього, утворенням фібринозних скупчень, несприятливі умови всмоктування та дифузії при колапсі, капіляротоксикозі
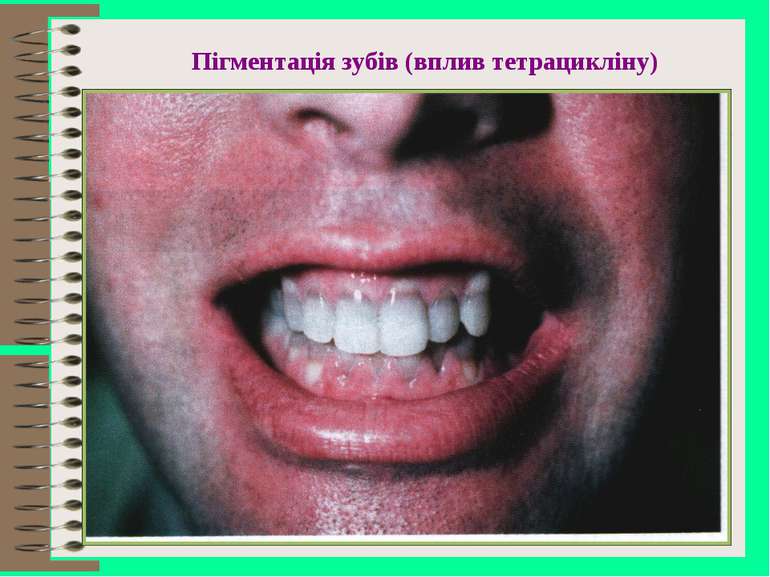
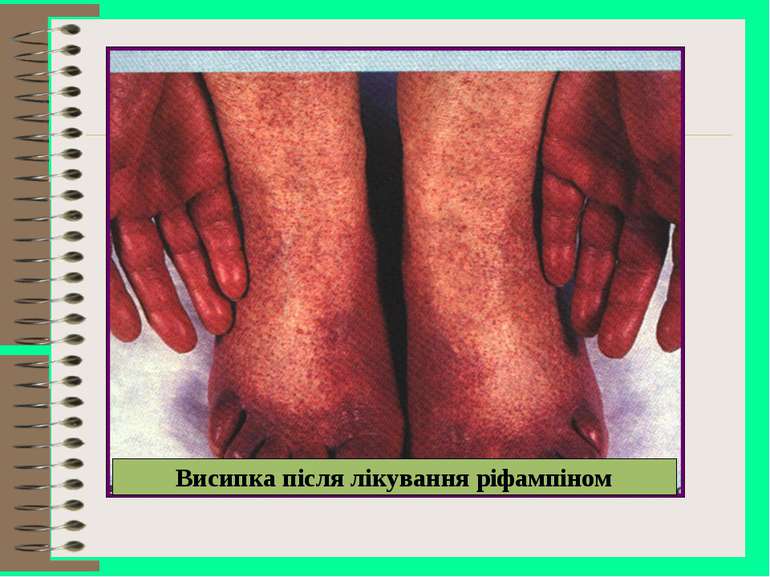
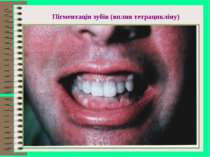
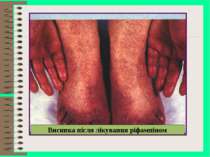
Побічна дія антибіотиків І. Алергічні реакції - небезпечні для життя (анафілактичний шок, ангіоневротичний набряк гортані) - безпечні для життя (шкірний зуд, кропив’янка, висипка, астматичні приступи, набряк Квінке, риніт, глосит, кон’юнктивіт, еозинофілія, фотодерматози від тетрацикліну, грізеофульвіну) ІІ. Токсичні реакції - небезпечні для життя (токсична дія на кров, агранулоцитоз, апластична анемія, ендотоксичний шок – реакція Яриш-Герксгеймера) - безпечні для життя (ураження вестибулярного та слухового апарату від аміноглікозидів, периферичний неврит, нудота, блювота, гіперемія ротоглотки, діарея, гепатотоксичність, нефротоксичність, ембріотоксина дія стрептоміцину, тетрацикліну (пігментація зубів, затримка скелетоутворення)
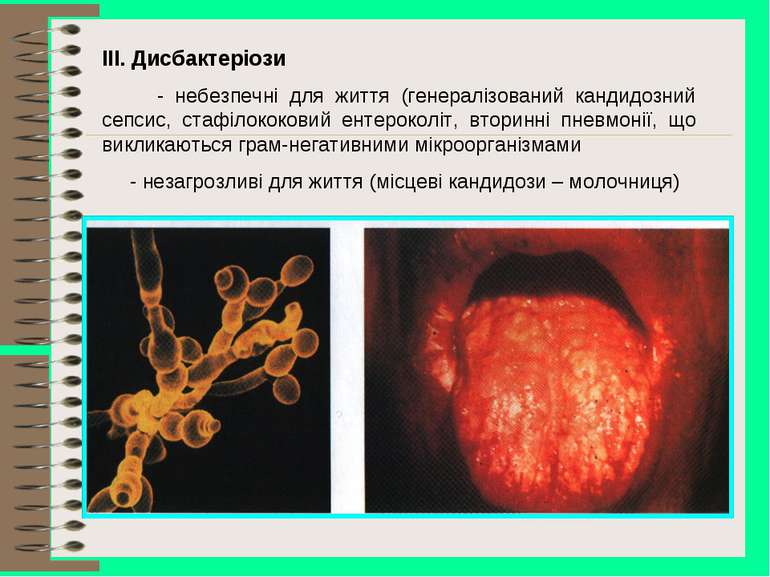
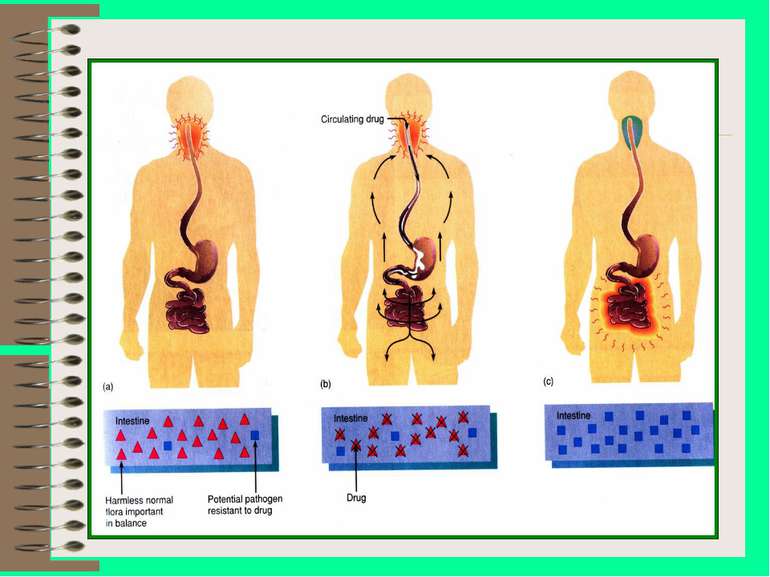
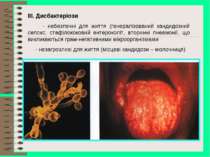
ІІІ. Дисбактеріози - небезпечні для життя (генералізований кандидозний сепсис, стафілококовий ентероколіт, вторинні пневмонії, що викликаються грам-негативними мікроорганізмами - незагрозливі для життя (місцеві кандидози – молочниця)
Резистентність мікроорганізмів до антибакте-ріальних засобів - збереження їх здатності до розмноження в присутності таких концентрацій цих речовин, які створюються при введенні терапевтичних доз. Резистентність бактерій “S” (sensitive) – чутливий до антибіотика мікроб “R” (resistant) – резистентний до антибіотика мікроб
Nota bene: 1929 – Александер Флемінг відкриває перший антибіотик - пеніцилін 1942 – Починається промислове виробництво пеніциліну 1954 – 1 тис. т антибіотиків випускається в США 1960’s – з’являються антибіотикостійкі бактерії внаслідок нераціонального застосування препаратів Сьогодні – 25 тис т антибіотиків виробляється в США щорічно Напевно, немає хіміотерапевтичного препарату, до якого бактерія за певних умов не зможе стати стійкою Александер Флемінг
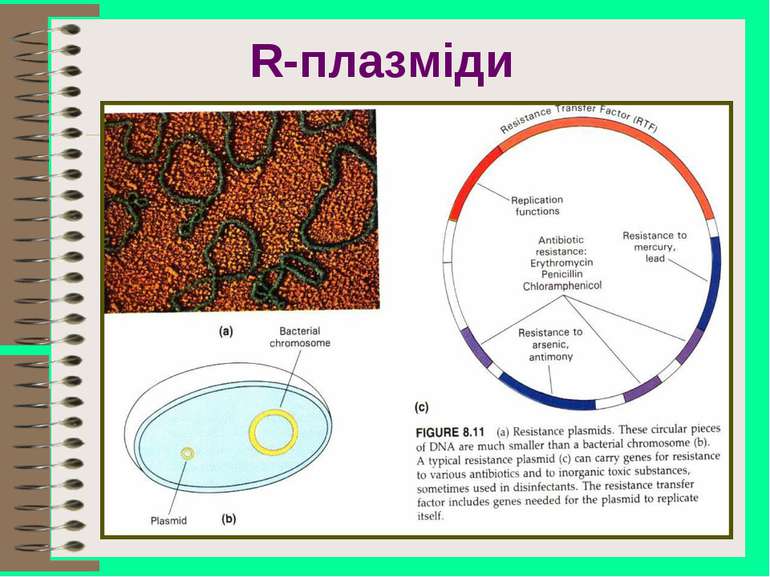
Типи стійкості бактерій до антибіотиків Перший тип - природна стійкість, яка визначається властивостями даного виду або роду мікроорганізмів. Другий тип - набута стійкість: первинна - як результат мутації - виявляється в окремих клітинах популяції через її гетерогенність до початку лікування антибіотиками. вторинна - формується також за рахунок мутацій при контакті бактерій з антибіотиками Набуття чужорідної ДНК: Передача плазмід (кон’югація)і Трасформація Трансдукція Транспозони Клональне поширення
Залежно від швидкості виникнення мутантів набута вторинна стійкість буває двох типів: стрептоміциного - “одноступенева мутація“ - швидко відбувається утворення мутантів з високою стійкістю після одно-двократного контакту мікроба з антибіотиком (стрептоміцин, рифампіцин, новобіоцин) пеніцилінового - “багатоступеневі мутації”- селекція стійких варіантів відбувається повільно (пеніцилін, ванкоміцин, левоміцетин, поліміксин, циклосерин)
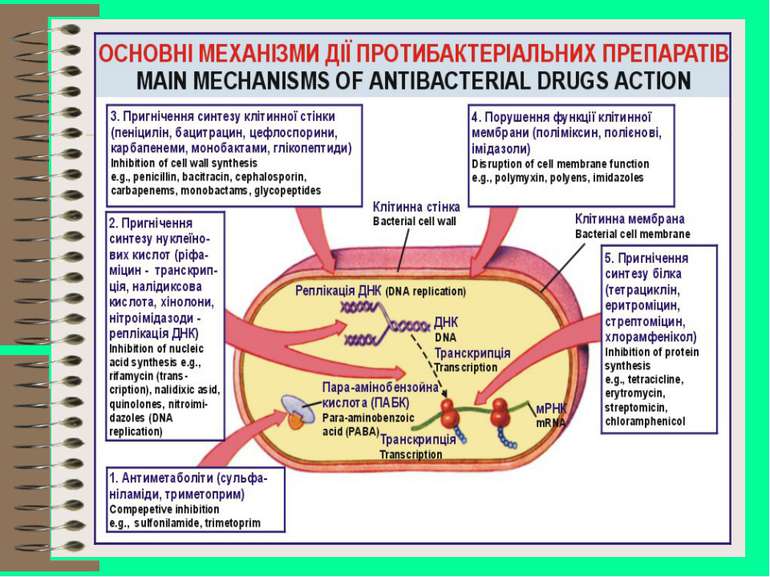
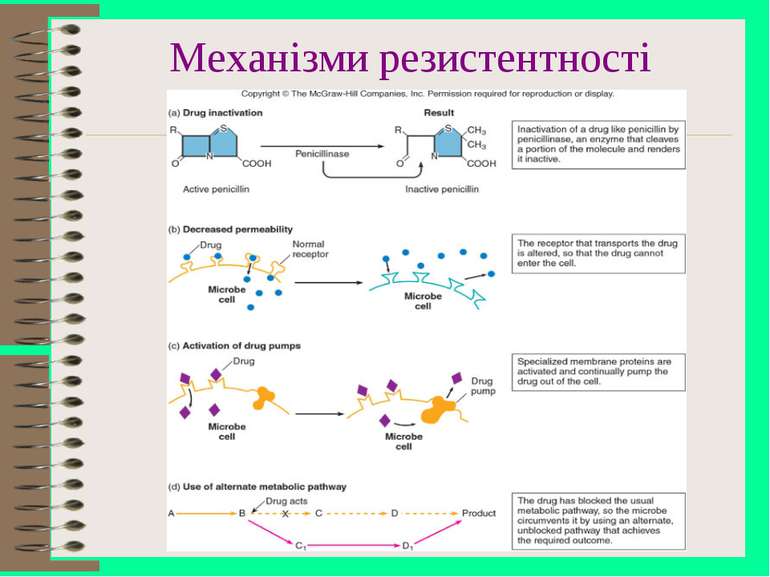
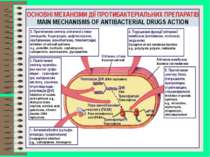
Механізми резистентності Мікроби не мають структур, до яких прикріплюється антибіотик Мікроби не проникливі для антибіотика Мікроби можуть модифікувати антибіотик в неакивну форму (пеніцилінази) Мікроби можуть модифікувати мішень для антибіотика Мікроби можуть формувати резистентність біохімічним шляхом Мікроби можуть виводити антибіотики, які поступають у клітину
Фактор селективного тиску Мутації, що зумовлюють резистентність до антибіотиків, відбуваються нечасто. Але використання антибіотиків забезпечує селективний тиск, що дозволяє врешті мутантам домінувати No antibiotics
Резистентність при реплікації Резистентні бактерії, як правило, мають гени, які роблять антибіотик неефективним Ті мікроби, які вижили, будуть розмножуватись Бактерії мають плазміди, яким вони можуть обмінюватися між собою Бактерії, які до того були чутливими, тепер мають гени резистентності Мертві бактеріальні клітини можуть передавати свою ДНК, яка інтегрується в геном чутливих клітин, і останні стають резистентними (трансформація)
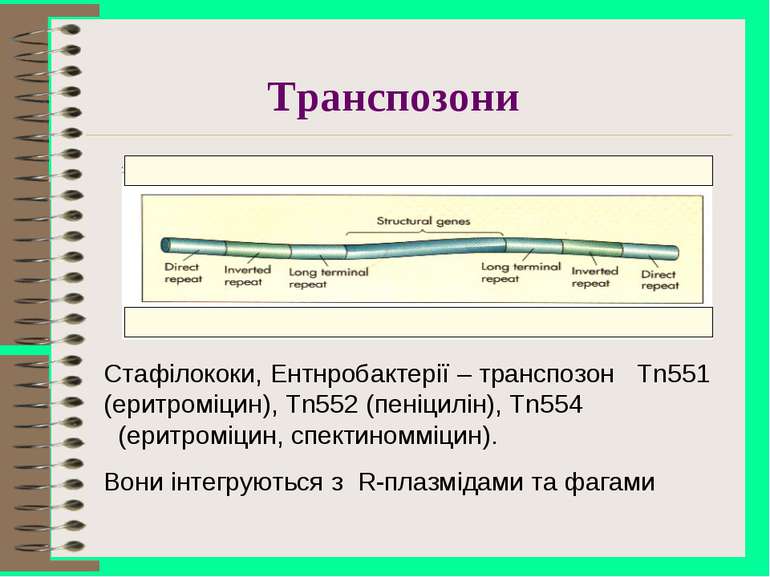
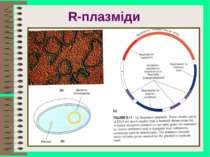
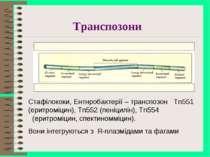
Транспозони Стафілококи, Ентнробактерії – транспозон Tn551 (еритроміцин), Tn552 (пеніцилін), Tn554 (еритроміцин, спектиномміцин). Вони інтегруються з R-плазмідами та фагами
Подолання антибіотикорезистентності Альтернативне використання існуючих антибіотиків: Зменшення періоду використання антибіотика, щоб не сформувалась резистентність Збільшення дози препарату для створення в організмі вищої його концентрації Відмінити антибіотик на певний період часу Зміна антибіотиків у процесі лікування Комбінування антибіотиків при лікуванні
Попередження антибіотикорезистентності Використовувати антибіотик тільки тоді, коли він буде корисним Не застосовувати антибіотики для лікування таких вірусних інфекцій, як загальна простуда, хворе горло або грип НЕ зберігати рецепти на виписані Вам антибіотики Застосовувати антибіотики тільки за призначенням лікаря Не приймати антибіотики, які були виписані іншим особам
Альтернатива антибіотикам Iнгібітори, що будуть нейтралізувати здатність мікроба ставити резистентним Антибіотик буде атакувати іншу мішень, ніж за нормальних умов, що дозволить йому бути ефективнішим Хімічні речовини з антибіотичними властивостями можуть використовуватись для знищення бактерій Зараз антибіотики отримують переважно із мікробів і грибів Бактеріофаги (віруси, що атакують бактерії)
Майбутнє хіміотерапевтичних засобів Антисенсові агенти Комплементарні фрагменти ДНК або пептиди нуклеїнових кислот, що зв’язуються з генами, відповідальними за вірулентність, і попереджують їх транскрипцію
Основні принципи раціональної антибіотикотерапії І. Обгрунтовані показання до призначення антибіотика. ІІ. Вибір найбільш активного і найменш токсичного препарату. Найефективніші при певному виді інфекції, до яких чутлива більшість штамів даного збудника, називаються препаратами першого вибору (першого ряду, першої групи). Альтернативні препарати (другого ряду) призначаються тоді, коли препарати першої групи неефективні або коли штам виділеного збудника найчутливіший саме до них. Препарати резерву використовують лише у крайніх випадках (при неефективності першої і другої груп антибіотиків); як правило, вони викликають багато ускладнень.
ІІІ. Введення оптимальних доз препарату з оптимальною частотою та урахуванням тяжкості інфекційного процесу. ІV. Вибір оптимального способу введення препарату з урахуванням важкості і локалізації інфекційного процесу і особливостей фармакокінетики даного антибіотика. V. Встановлення тривалості курсу антибіотикотерапії. VI. Контроль за виліковуванням. VII. Моніторінг і профілактика негативних побічних реакцій і ускладнень. VIII. Вирішення питання про доцільність комбінованої антибіотикотерапії з урахуванням явищ синергізму та антагонізму між препаратами.
Схожі презентації
Категорії