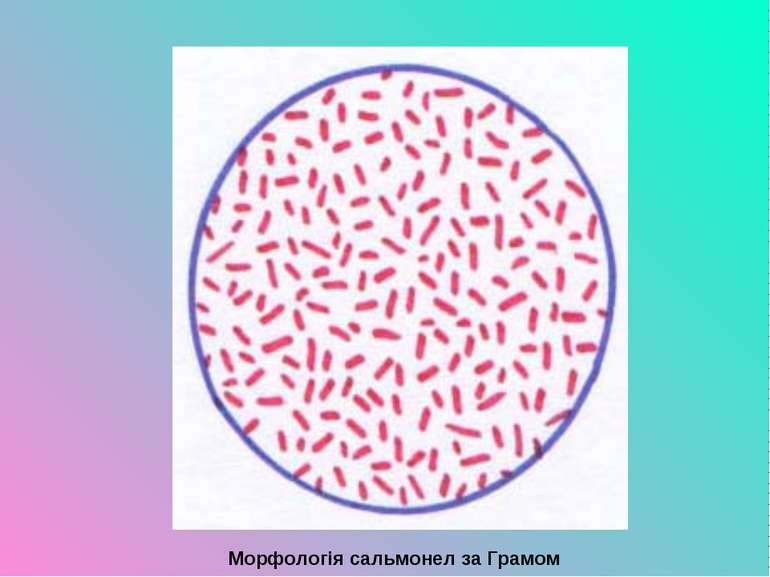
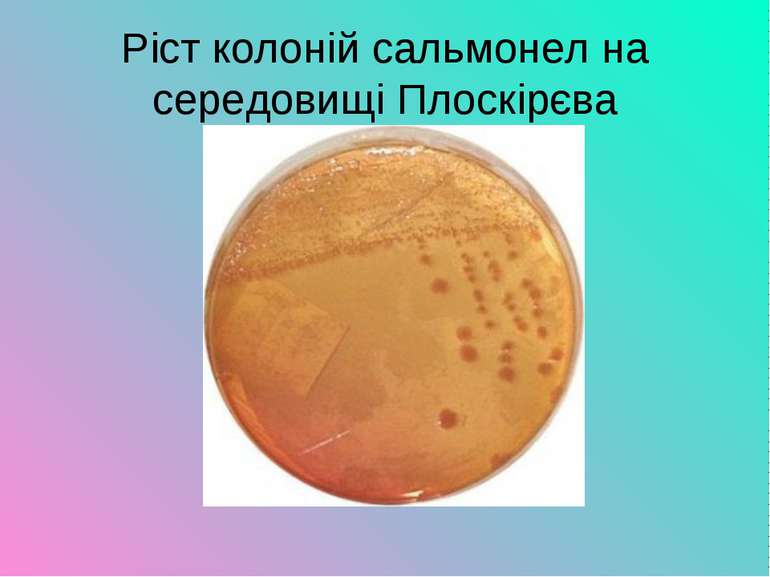
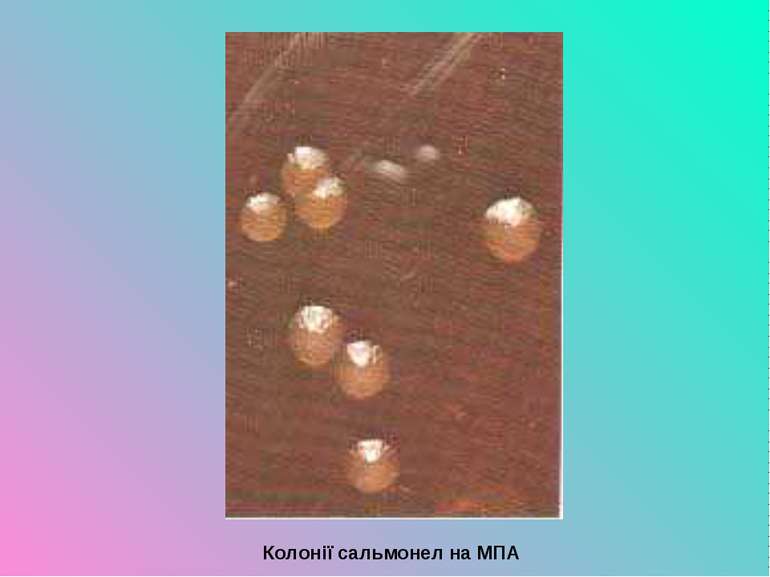
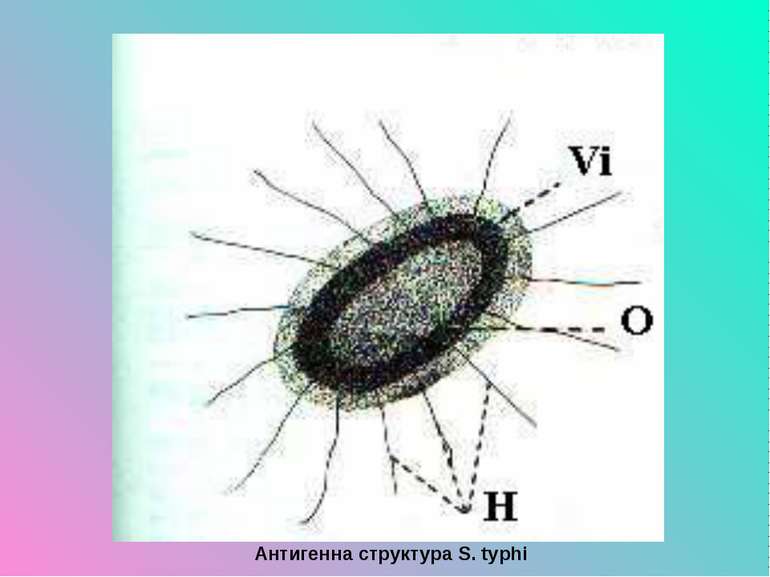
Презентація на тему:
РОДИНА ЕНТЕРОБАКТЕРІЙ
Завантажити презентацію
РОДИНА ЕНТЕРОБАКТЕРІЙ
Завантажити презентаціюПрезентація по слайдам:
План лекції Вступ Загальна характеристика родини Enterobacteriaceae Біологічні властивості і методи лабораторнаої діагностики захворювань, викликаних Е. сoli Збудники сальмонельозів. Захворювання, які вони викликають і методи лабораторної діагностики
Родина Enterobacteriaceae Бактерії родини Enterobacteriaceae включає більш ніж 20 родів, що об′єднують близько 100 видів бактерій. Ушкодження у людини викликають бактерії родів Escherichia, Shigella, Salmonella, Klebsiella, Proteus, Citrobacter, Serracia, Yersinia та багато інших. На даний час великого значення набуває роль умовно-патогенної флори, що часто викликає опортуністичні інфекції, котрі викликають близько 50 % всіх септицемій, до 70 % всіх гастроентеритів, и більш ніж 70 % інфекцій сечовидільних шляхів.
Класифікація родини Enterobacteriaceae Escherichia Shigella Edwardsiella Salmonella Citrobacter Klebsiella Enterobacter Hafnia Serratia Proteus Providencia Morganella Yersinia Erwinia
Ешеріхії (Escherichia) Свою назву бактерії отримали в честь німецького педиатра Теодора Ешеріха, котрий вперше виділив Е.coli з вмісту кишківника дітей. До роду входять рухливі (перитрихи) прямі паличкоподібні бактерії розміром 1,1-1,5 х 2,0-6,0 мкм. В мазках вони розташовуються поодиноко чи парами. У більшості штамів є капсули чи мікрокапсули. Температурний оптимум для росту складає 37 С. Ешеріхії ферментують вуглеводи з утворенням кислоти чи кислоти і газу, оксидазовід′ємні та каталазо позитивні.
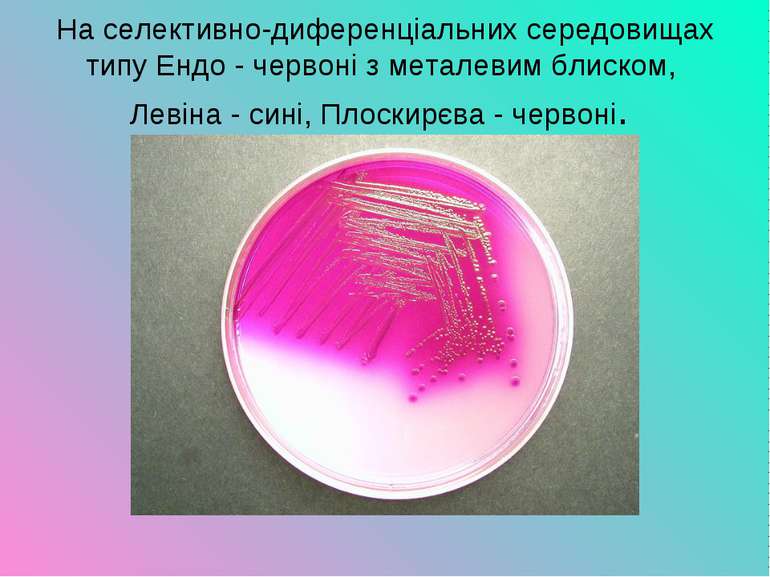
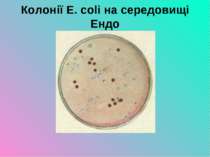
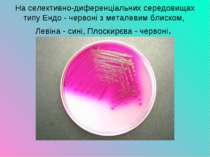
Ферментативні властивості Е. сoli. На середовищах Гіса Е. сoli ферментує вуглеводи з утворенням кислоти і газу. утворювати газ. На селективно-диференціальних середовищах колонії набувають кольору середовища. На агарі Ендо лактозопозитивні ешеріхії утворюють фуксиново-червоні колонії з металевим блиском, лактозонегативні – блідо-рожеві чи безколірні з темним центром. На середовищі Левіна формують темно-фіолетові колонії з металевим блиском, а лактозонегативні – безколірні. На середовищі Плоскірєва - відповідно- рожево-червоні та безколірні. На КА – повний гемоліз.
На селективно-диференціальних середовищах типу Ендо - червоні з металевим блиском, Левіна - сині, Плоскирєва - червоні.
Токсиноутворення Ендотоксини - складні ліпополісахаридні комплекси, які утворюються клітинними стінками бактерій і виділяются при лізісі мікробів. Це термостабільні речовини загальною малекулярною масою від 100000 до 900000. Ліпополісахариди можуть бути екстраговані з бактерій сумішшю фенол-вода. Вони складаються з трьох фрагментів: - комбінації олігосахаридів, які повторюються (маноза-рамноза-галактоза) і є типоспецифічнми гаптенними детермінантами; - N-ацетилглюкозамін, глюкоза, галактоза, гептоза (однакові у всіх грамнегативних бактерій); - основа з гептоз і фосфатних груп, які чергуються, зв язаніз ліпідом. Дія всіх ендотоксинів незалежить від їх походження.
Введення ендотоксину тваринам або людям призводить до розвитку явищ, пов язаних із захватом його ретикулоендотеліальними і ендотеліальними клітинами клітинами, наступної деградації або нейтралізації. В клінічних експериментах відмічено такі найбільш виражені зміни: - гарячка ( через 60-90 хвилин після введення токсину); - лейкопенія (пізніше розвивається лейкоцитоз); - гіпотонія; - порушення кровопостачання органів і ацидоз; - активація С3-фракції та системи комплементу (за рахунок цього прискорюється продукція анафілотоксинів, хемотаксис, пошкодження мембран); - дисемінована внутрішньосудинна коагуляція (активація ХІІ фактора - фактора Хагемана) - приклеювання тромбоцитів до ендотелія судин і закупорка дрібних кровоносних судин, що в свою чергу спричиняє розвиток ішемічного та геморагічного некрозу в різних органах; - смерть (через виражений розлад функцій органів, шок, ДВК.
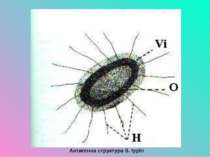
Антигенна структура Е. сoli Оскільки морфологічних відмінностей між патогенними і непатогенними кишковими паличками немає, їх диференціація базується на відмінностях Аг-структури. У Е. сoli виділяють ліпополісахаридні (О-), джгутикові білкові (Н-), капсульні полісахаридні (К) Аг, що позначаються арабськими цифрами. На практиці використовують співвідношення О:Н (виділено 173 О- і 56 Н-сероварів). За К-Аг бактрії розділяють на три групи (L, B, і A), за їх структурою виділяють 80 сероварів.
Антигенна структура Е. сoli Крім цих антигенів описано антигени R, M, f+, , та інші. Структурно ці антигени розміщені неоднозначно: О-атигенний комплекс - в оболонці; рибосомні - в середині цитоплазми; f+ - фімбріальні; К - в оболонці або за її межами; , - подібні до еритроцитарних антигенів.
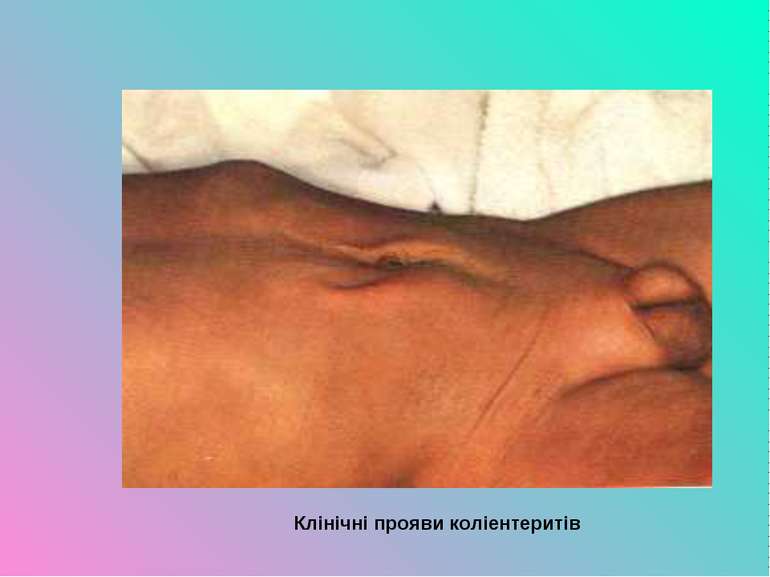
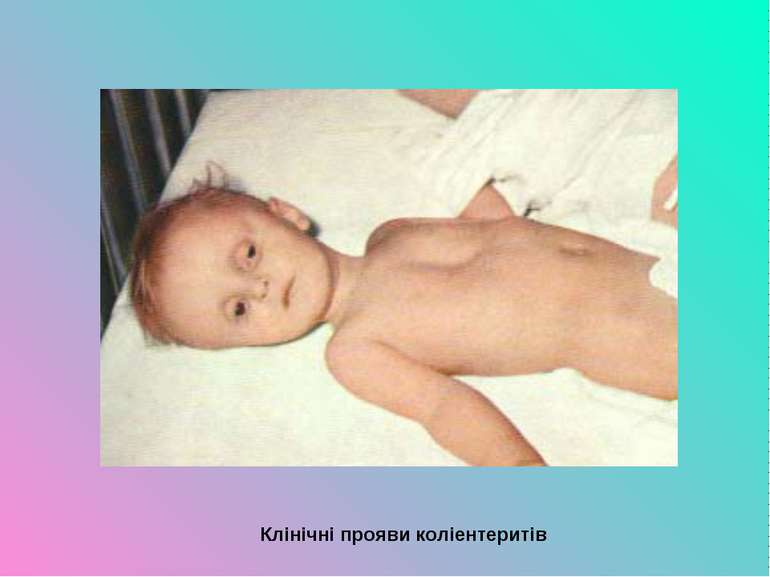
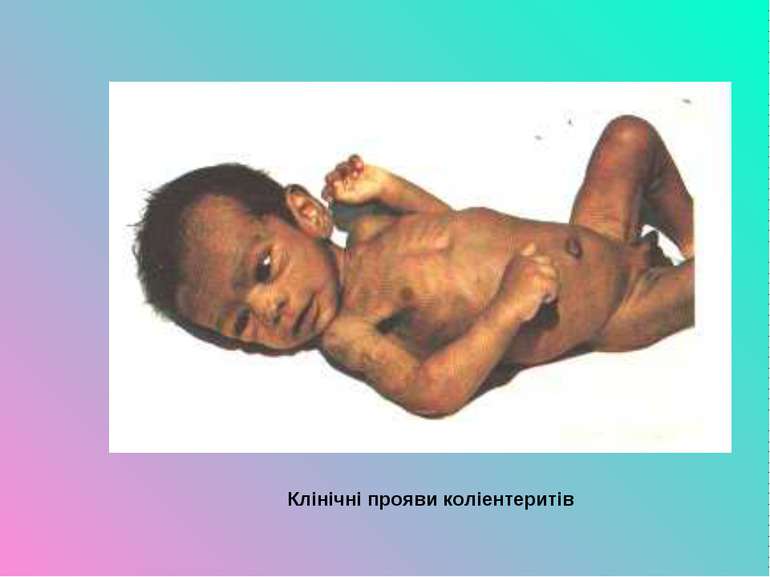
Патогенез уражень та клінічні прояви. У людини кишкова паличка викликає кишкові інфекції, ураження сечовидільних шляхів, бактеріємію, менінгіт, респіраторні інфекції. Кишкові інфекції поділяють на 5 типів: ентеротоксигенні (ЕТКП), ентеропатогенні (ЕПКП), ентерогеморагічні (ЕГКП), ентероінвазивні (ЕІКП) та ентероадгезивні (ЕАКП). Основний шлях передачі ешеріхій, що викликають діарею – фекально-оральний. Найбільш часто людина інфікується при вживанні контамінованої їжі, води та при контакті з тваринами.
Ентеротоксигенні ешеріхії викликають холероподібні захворювання (серовари О6,О 8,О11,О15,О25, О27,О115, О126, О148), ентеропатогенні – класичні коліентерити (О26,О55,О125,О127,О142), ентероінвазивні – дизентерієподібні ураження (О28,О29,О143,О144), ентерогеморагічні – діареї з виділенням крові (О26,О111,О157). Ентероадгезивні кишкові палички вивчені ще недостатньо
Ураження Серогрупи О-антиген, Н-антинген, К-антинген Кишечник Ентеротоксигенні(ЕТКП)06, 08, 011, 015, 020, 025, 027, 063, 078, 080, 085, 0114, 0115, 0126, 0128, 0139, 0148, 0153, 0159, 0166, 0167Н4, Н7, Н9, Н11, Н12, Н19, Н20, Н21, Н28, Н40 Ентеропатогенні(ЕПКП)018, 026, 044, 055, 086, 011, 0112, 0114, 0119, 0125, 0127, 0128, 0142, 0158Н2, Н6, Н7, Н11, Н12, Н14, Н18 Ентероінвазивні(ЕІКП) 028, 029, 0112, 0115, 0124, 0135, 0136, 0143, 0144, 0152, 0164, 0167 Ентерогеморагічні(ЕГКП)028, 029, 0112, 0115, 0124, 0135, 0136, 0143, 0144, 0152, 0164, 0167026, 0111, 0157 Н6, Н7, Н8, Н11 Сечовивідні шляхи01, 02, 04, 06, 07, 08, 09, 011, 018, 022, 025, 062, 075К1, К2, К5, К12, К13 Бактеріємія01, 02, 04, 06, 07, 08, 09, 011, 018, 022, 025, 075К1, К2, К5, К12, К15, К23 Менінгіти01, 06, 07, 016, 018, 083К1
Діареєгенні E. coli Фактори вірулентності Ентеротоксигенні E. coli Термолабільний токсин (LT) Термостабільний токсин (ST) Колонізуючий фактор (фімбрії). Ентерогеморагічні E. coli Шигаподібний токсин І, ІІ (SLT-I, SLТ-II) Колонізуючий фактор (фімбрії) Ентероінвазивні E. coli Шигаподібний токсин І, ІІ (SLT-I, SLТ-II) Здатність проникати в епітеліальні клітини Ентеропатогенні E. coli Адгезивний фактор до епітеліальних клітин E. coli, що спричиняють ураження сечовивідної системи P- фімбрії E. coli, що спричиняють менінгіти K-1 капсули
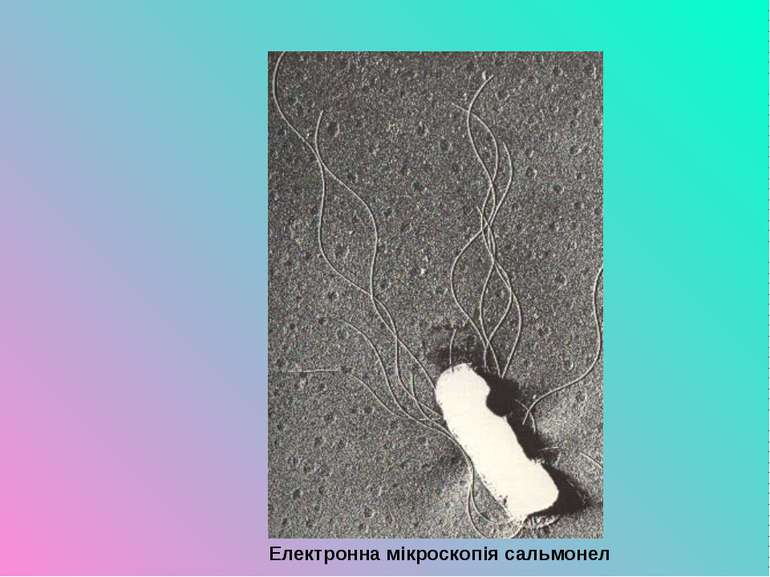
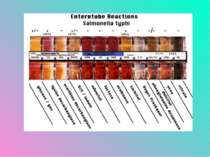
Збудники сальмонельозів (гастроентероколітів) За морфологічними і культуральними властивостями сальмонели подібні до ешеріхій, черевнотифозних і паратифозних бактерій. Вони відрізняються за деякими біохімічними ознаками, але диференціюють їх за антигенною структурою в реакції аглютинації. Крім того, більшість сальмонел патогенні для білих мишей. Збудники сальмонельозів виділяють ентеротоксини і мають ендотоксини, які зумовлюють клінічну симптоматику захворювань і явища інтоксикації організму хворої людини.
Родову назву для цих бактерій дали на честь Д. Сальмона, який описав одного із збудників. Найчастіше захворювання викликають Salmonella typhimurium, S. enteritidis, S. heidelberg, S. anatum, S. haifa, S. derby, S. cholerae suis та ін. Усього ж відомо понад 2200 сероварів сальмонел, які відрізняються за О- і Н-антигенами. Більшість сальмонел патогенні як для людини, так і для різних тварин і птахів. Вийнятком є сальмонели черевного тифу і паратифів, які патогенні лише для людини і викликають зовсім інші клінічні форми захворювань.
Класифікація сальмонел Рід Salmonella Види: Salmonella choleraesuis Salmonella bongory Підвиди Salmonella choleraesuis S. choleraesuis S. salamae S. arizonae S. diarizonae S. houtenae S. indica
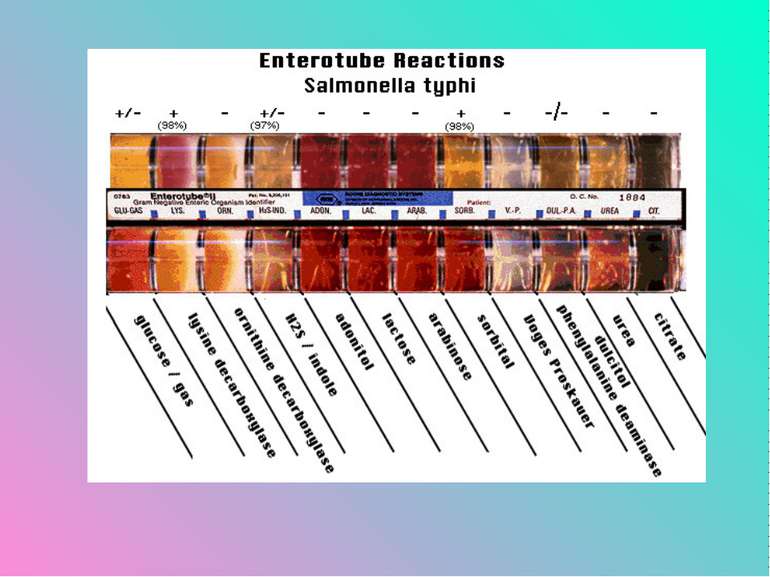
Лабораторна діагностика. Матеріалом для дослідження є випорожнення, блювотні маси, промивні води шлунка, кров, сеча. Одночасно проводять дослідження залишків їжі як можливих факторів передачі збудників. Матеріали треба забирати до початку лікування. Посіви роблять на середовища Ендо, Плоскирєва, вісмут-сульфіт агар, виділяють чисті культури, які ідентифікують у реакції аглютинації груповими і монорецепторними сироватками. Доцільно поставити біологічну пробу на мишах не тільки з виділеними культурами, а й з рештками підозрілої їжі. Для ретроспективної діагностики використовують реакцію аглютинації і РНГА з еритроцитарними діагностикумами. Діагностичне значення має наростання титру антитіл у динаміці при використанні парних сироваток. При осередкових спалахах захворювань як експрес-метод застосовують реакцію імунофлуоресценції.
Збудники черевного тифу і паратифів Збудник черевного тифу Salmonella typhi відкрив К. Еберт у 1880 році, у чистій культурі його виділив Г. Гаффкі в 1884 році. Г. Шотмюллер описав збудника паратифу B (S. schottmuelleri), А. Бріон і Х. Кайзер - паратифу А (S. paratyphi A), а Л. Гіршфельд - паратифу С (S. paratyphi C).
Антигенна структура сальмонел Антигенна структура сальмонел складна. У них розрізняють О- та Н-антигени. В залежності від О-антигену, який позначається арабськими цифрами, сальмонели поділяють а сеологічні групи. Специфічність О-антигену зумовлена полісахаридними ланцюгами: 9 (група D) - поліозид (дідезоксигексоза) тівелози, 4 (група В) - абеквоза, 2 (група А) - паратоза.
Н-антигени існують в 2 фазах - 1-ій і 2-ій, відповідно специфічній та неспецифічній. Н-антигени 1-ої фази позначаються прописними літерами латинського алфавіту, 2-ої фази - арабськими цифрами абро прописними латинськими літерами з арабськими цифрами.Сальмонели, у яких Н-антиген представлено двома фазами, називають двофазними, а одією фазою - монофазними. Одним з компонентів О-антигену є Vi-антиген, антиген групи К-антигенів. Проте він не є прямим антигеном вірулентності, може бути й у інших сальмонел, ешерихій, цітробактера. Виявлено ще М-антиген - слизовий - у S. schottm lleri, S. cholerae-suis, Т-антиген (transient).
Фази патогенезу черевного тифу 1. дигестивна 2. інвазії 3. бактеріємії 4. паренхіматозної дифузії 5. алергічно-видільна 6. реконвалесценції
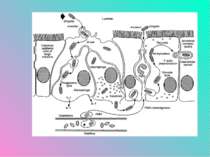
Патогенез захворювань Збудники проникають в організм через рот. Разом із зараженою водою, їжею він попадає в шлунково-кишковий тракт. Внаслідок тривалого філогенетичного розвитку вони виробили тропізм до епітеліальних клітин слизової тонкої кишки, отже, бактерії фіксуються до них, потім проникають в середину клітини і розмножуються в слизовій оболонці, особливо в її лімфоїдній тканині, що ї вихідними етапом формування тифо-паратифозної інфекції (солітарні фолікули, пейерові бляшки, можливо, наіть і мигдалики). Це відбувається недивлячись на на перший потужний фізіологічний бар єр - кислий вміст шлункового соку, наявність місцевого імунітету у вгляді IgA, колонізаційну резистентність слизової, яка забезпечується нормальною мікрофлорою кишечника. На цьому завершується дигестивна та інвазійна фази патогенезу хвороби (інкубаційний період).
Розмноження збудника в лімфатичсних утвореннях супроводжується запальною реакцією з гіперплазією клітин ретикулоендотелію і утворенням специфічних черевнотифозних гранульом. Розвиваються лімфаденіт і лімфангіт. Особливо інтенсивно збудник розмножується в лімфатичних вузлах брижі, бар єрна функція яких внаслідок запалення порушується, і черевнотифозні палички поступають в кров - розвивається фаза бактеріємії. Її розвиток знаменує закінчення інкубаційного періоду і початок клінічних проявів хвороби. Частина циркулюючих мікробів при цьому гине через бактерицидні властивості сироватки крові. При цьому вивільняється ендотоксин. Клінічно це проявляється пропасницею, затьмарення свідомості, апатією, в ялістю (м ялістю), безсонням, маренням, зниженням або втратою апетиту, брадикардією, гіпотензією та іншими симптомами. Таким чином, циркуляція великої кількості ендотоксина і продуктів тканинного розпаду викликають стан глибокої інтоксикації, яку називають “status typhosus”.
У цій фазі спостерігаються значні зміни імунологічной реактивності організму: в крові знаходять підвищення титрів аглютининів, пропердину, комплементзв`язуючих антитіл, бактеріолізинів. Проте на фоні зростаючої імунологічної реактивності циркулюючі в крові мікроби розносяться по всім тканинам, локалізуючись переважно в органах багатих на лімфоїдні та ретикулоендотеліальні клітини - лімфатичних вузлах, селезінці, печінці, легенях, кістковому мозку. З одного боку це захисний механізм, так як сприяє локалізації збудника ( перетворює генералізовану інфекцію в локалізовану), з іншого - виникають вогнищеві ураження у вигляді холециститу, пієліту, бронхопневмоній, менінгіту. Ця фаза називається фазою паренхіматозної дифузії.
В подальшому проходить очищення організму від інфекційного агенту. Мікроби з організму виділяються через шлунково-кишковий тракт (жовчно-печінкову систему), нирки, травні залози кишечнику (ліберкюнові залози), а також через потові, слинні, молочні (у жінок, які годують) залози. Основна маса збудників виділяється з випорожненнями, частина знову попадає в лімфатичні фолікули, які раніше були сенсибілізовані бактеріальними антигенами. При цьому розвивається запально-некротична реакція з утворенням виразок (за типом феномену Артюса-Сахарова) - утворення імунних комплексів. Утворення розеол при ЧТ також в значній мірі зумовлюється алергічним компонентом. Ця фаза дістала назву: видільно-алергічна. В заключній фазі - реконвалесценції - спостерігається остаточне вивільнення організму від збудника, максимальне напруження специфічних механізмів захисту (імунітет) і неспецифічної резистентності організму.
Лабораторна діагностика Основа діагностики - виділення збудників і виявлення антитіл. У перші дні захворювання і пізніше, поки є гарячка, застосовують метод гемокультури. Для її виділення сіють 10 мл крові в середовище Рапопорт або жовчний бульйон у співвідношенні 1:10. Посіви інкубують при 37 °С, роблять пересів на середовище Ендо. Типові колонії відсівають на скошений агар Олькеницького. Виділену чисту культуру ідентифікують за ферментативними властивостями та реакцією аглютинації із специфічними сироватками. Метод гемокультури є раннім і достовірним методом діагностики. Він має абсолютне діагностичне значення.
Серологічне дослідження проводиться як для діагностики захворювання так і для встановлення бактеріоносійства. З діагностичною метою ставлять розгорнуту об′ємну реакцію Відаля (з О- і Н-діагностикумами) і РНГА з О- і Vi- еритроцитарними діагностикумами. РНГА є більш надійною і специфічною. Останнім часом широко використовують метод ІФА. Метод урино- і копрокультури переважно застосовують для діагностики бактеріоносійства у реконвалесцентів.
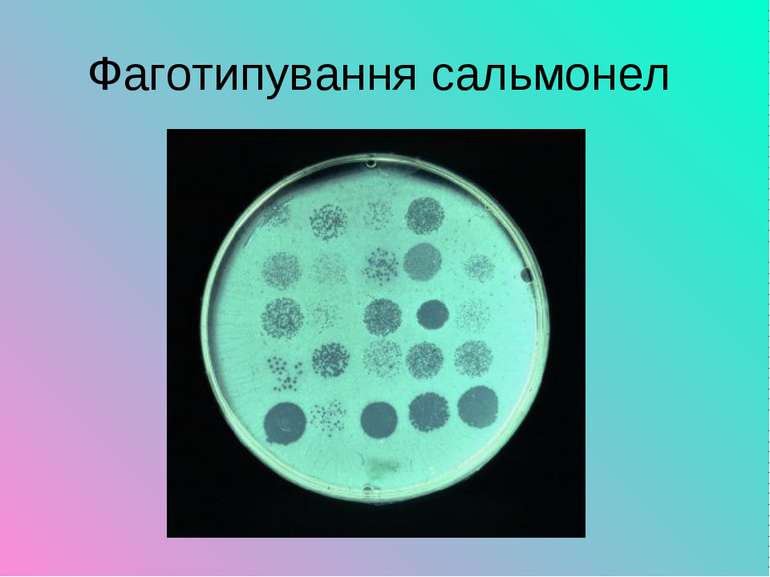
Профілактика черевного тифу і паратифів Крім неспецифічної профілактики існує специфічна профілактика. З цією метою використовується хімічна сорбована тифо-паратифозна В вакцина; ТАВТ - тифо-паратифозна В і правцева вакцина; черевнотифозна спиртова вакцина, збагачена Vi- антигеном; полівалентний черевнотифозний сухий бактеріофаг (вкритий твердою оболонкою). Хімічна вакцина забезпечує захист від захворювання протягом 10 міс. у 53-78 % щеплених осіб.
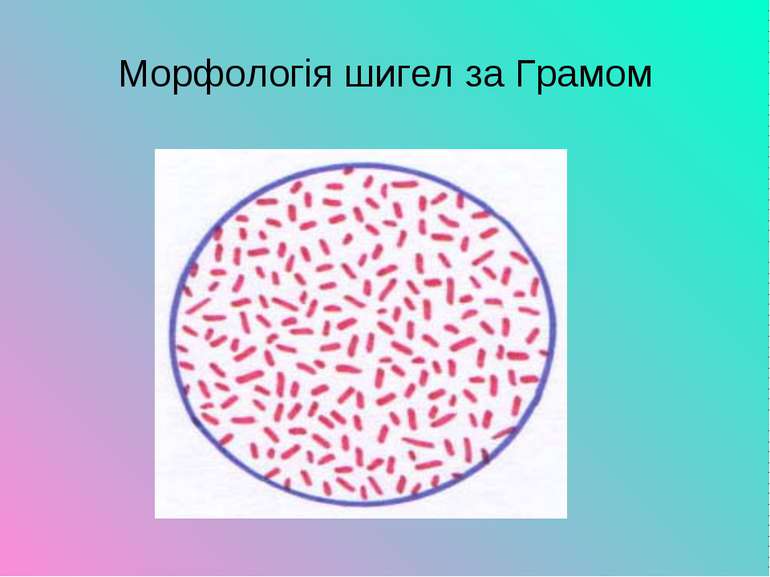
Шигели (Shigella) Бактерії отримали назву на честь японського бактеріолога Кийосі Шига, котрий вперше описав збудника бактеріальної дизентерії (шигельозу). У відповідності до антигенної структури О-Аг і біохімічних властивостей відомо 39 сероварів шигел, які розділяють на 4 види: Shigella dysenteriae (серогрупа А), Shigella flexneri (серогрупа В), Shigella boydii (серогрупа С) та Shigella sonnei (серогрупа D). Рід утворюють прямі нерухомі палички, хеморганотрофи, оксидазонегативні, каталазопозитивні. Оптимальна t для культивування складає 37 С.
Класифікація шигел Підгрупи Види і серотипи Підсеротипи A. Манітнегативні S.Dysenteria 1-12 B. Манітпозитивні S. flexneri 1, 2, 3, 4, 5, 6, X variant Y variant 1a, 1b, 2a, 2b, 3a, 3b, 4a, 4b C. Манітпозитивні S. Boydii, 1-18 D. Ферментують маніт і повільно сахарозу і лактозу S. sonnei
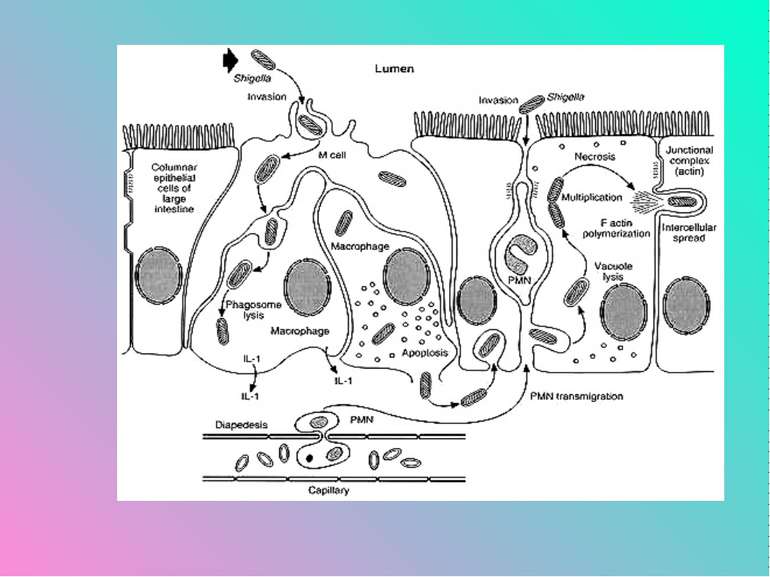
Патогенез захворювання Найважливішою здатністю шигел, що обумовлює їх патогенність – здатність проникати в епітелій слизової оболонки товстої кишки і розмножуватися в ньому. Також вона обумовлена факторами адгезії, інвазії, і стійкістю до дії захисних механізмів, а також здатністю до токсиноутворення. Гени, що кодують комплекс вірулентності розташовані у хромосомі і плазмідах.
Мікробіологічна діагностика Матеріалом для досліджень є випорожнення. Метою дослідження є визначення біохімічних ознак і антигенної структури збудника. Сіють матеріал на середовище Ендо і Плоскірєва або на рідкі живильні середовища накопичення. Після виділення чистих культур визначають їх видову належність. Визначення антигенної структури проводять за здатністю моно- і полівалентних антисироваток аглютинувати бактерії. Для виявлення Аг шигел в крові, сечі і випорожненнях використовують РЗК, ІФА, реакцію коаглютинації.
Особливості забору матеріалу при підозрі на дизентерію Бактеріологічне дослідження по можливості потрібно починати до початку етіотропної терапії, забір проводять натщесерце; Посуд для матеріалу ошпарюють кип′ятком і ні в якому разі не обробляють дезрозчинами; Досліджуваний матеріал швидко висівають на середовище збагачення та паралельно на селективний агар.
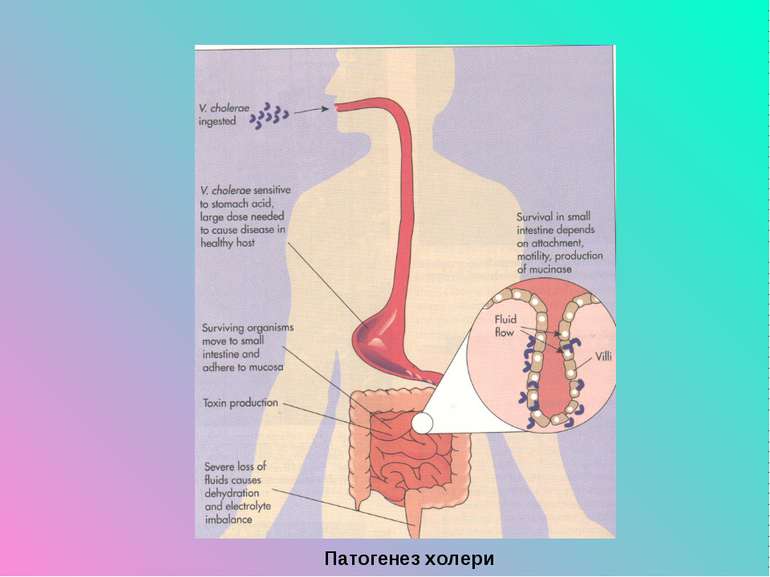
Збудник холери (Vibrio cholerae) Холера - гостра, карантинна, особливо небезпечна інфекційна хвороба з фекально-оральним механізмом передачі, характеризується рясним поносом, блюванням, сильною інтоксикацією та зневодненням організму. Холерний вібріон вперше описав італійський вчений Ф. Пачіні в 1854 р., детально вивчив його властивості і виділив у чистій культурі Р. Кох у 1883 р., Ф. Готшліх у 1906 р. виділив з кишечника прочанина вібріон Ель-Тор, який відрізняється від холерного гемолітичними властивостями й також спричиняє холеру.
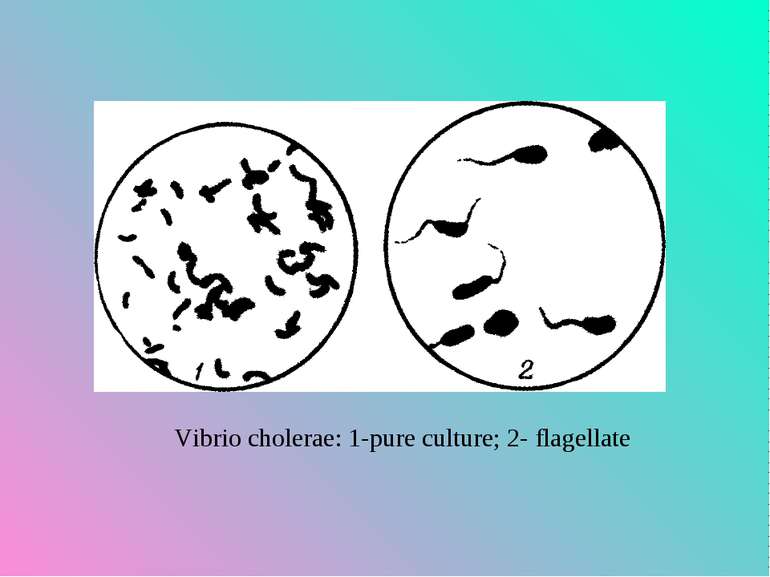
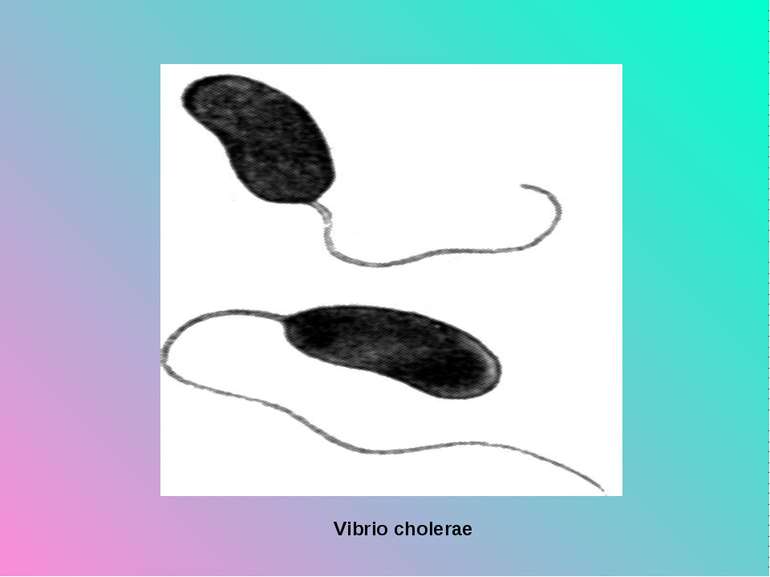
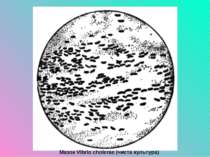
Морфологія і фізіологія. V. cholerae, V. eltor мають форму зігнутих (нагадують кому) або прямих поліморфних паличок довжиною 1,5-3 мкм, шириною 0,3-0,6 мкм, спор і капсул не утворюють, мають один, полярно розташований джгутик (монотрих), завдяки якому дуже активно рухаються. У мазках з чистих культур розташовуються поодинці, а в свіжих препаратах із фекалій хворого мають вигляд табунців рибок.
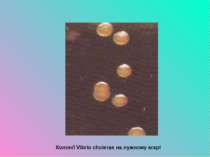
Культуральні властивості Холерні вібріони - факультативні анаероби, легко культивуються в аеробних умовах при 37 °С. До живильних середовищ невибагливі, але вимагають лужної реакції (рН 8,5-9,5). Дуже добре й швидко ростуть у 1 % лужній пептонній воді (ПВ), випереджаючи ріст інших бактерій. Вже через 5-6 год на її поверхні виникає ніжна плівка блакитного кольору. На лужному МПА через 10-12 год утворюють середніх розмірів гладенькі круглі прозорі колонії з блакитним відтінком і чітко окресленим краєм.
Антигенна будова Холерні вібріони мають термостабільні специфічні О-антигени і термолабільні джгутикові Н-антигени. За О-антигеном всі вібріони поділені на багато серогруп О1, О2, О3... О80. Холерний вібріон відноситься до 01 серогрупи. У свою чергу 01-антиген складається з окремих антигенних фракцій А, В, С. Різні комбінації їх властиві трьом сероварам: Oгава (АВ), Інаба (АС) і Гікошима (АВС). Усі три серовари аглютинуються 01 сироваткою. V. eltor належить до серогрупи О1. Крім того, є ще серогрупи RO та О139.
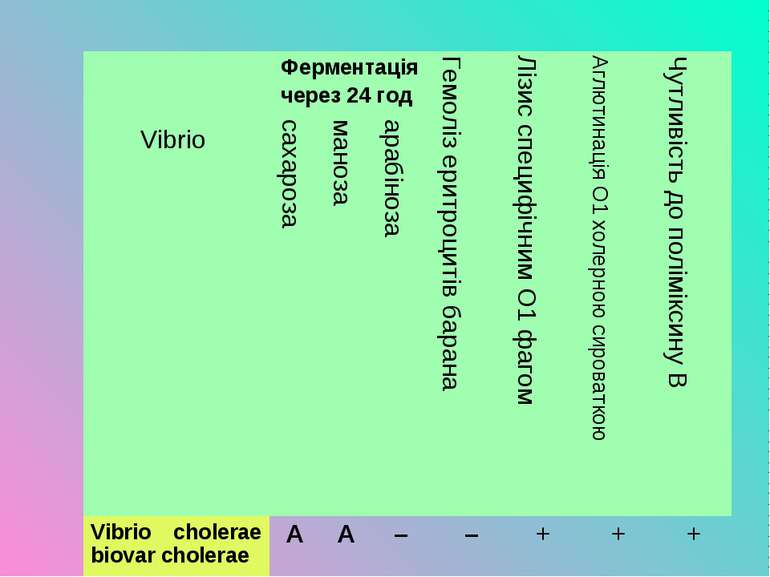
Vibrio Ферментація через 24 год Гемоліз еритроцитів барана Лізис специфічним О1 фагом Аглютинація О1 холерною сироваткою Чутливість до поліміксину В сахароза маноза арабіноза Vibrio cholerae biovar cholerae A A – – + + + Vibrio cholerae biovar El Tor A A – + + + – Vibrio cholerae biovar Proteus A A – + – – – Vibrio cholerae biovar albensis А – – – – – –
Токсиноутворення Холерні вібріони виділяють два типи токсинів: 1) білковий екзотоксин (холероген), який діє на ентероцити тонкого кишечника, спричиняючи ентерит з водянистими випорожненнями і зневоднення організму; 2) ендотоксин - ліпополісахаридний комплекс, який звільняється тільки при руйнуванні вібріонів, він також бере участь у механізмі розвитку хвороби. Токсигенні штами О1, О139 мають ген холерного токсину (vct+) і викликають холеру, схильну до широкого епідемічного розповсюдження.
Лабораторна діагностика Основним і вирішальним у лабораторній діагностиці холери є бактеріологічне дослідження. Від хворих беруть випорожнення, блювотні маси, кусочки забрудненої білизни, від трупів - відрізки тонкого кишечника й жовчний міхур. Досліджують також харчові продукти, воду, мул, риб, жаб та ін. Широко практикують ректальний забір. Стерильні ватний тампон або алюмінієву петлю вводять у пряму кишку на глибину 5-10 см, забирають вміст і вносять у флакон (пробірку) з 1 % лужною ПВ.
Мікробіологічні дослідження проводять цілодобово. Відповідно до інструкції МОЗ України від 30.05.1997 р. вони включають декілька етапів. 1-й етап - матеріал засівають у 10-50 мл 1 % ПВ; застосовують також експрес-методи: імунофлуоресцентний і РНГА. 2-й етап - висів з 1-го середовища збагачення на ЛМПА (лужний МПА) або селективні середовища і в 5 мл 2-го середовища збагачення. Пересіви в рідкі й на щільні середовища проводять з поверхні ПВ великою бактеріологічною петлею діаметром 5 мм. 3-й етап - висів з 2-го середовища збагачення на ЛМПА (або селективні середовища) через 5-6 год вирощування. 4-й етап - проводять відбір підозрілих колоній зі щільних середовищ через 16-24 год інкубації. 5-й етап - ідентифікація. 6-й етап - враховують результати ідентифікації й видають остаточну відповідь про виділення культури холерного вібріона відповідної серогрупи: О1, RO (Інаба, Огава, Гікошима) або О139 із зазначенням гемолітичної активності, чутливості до антибіотиків.
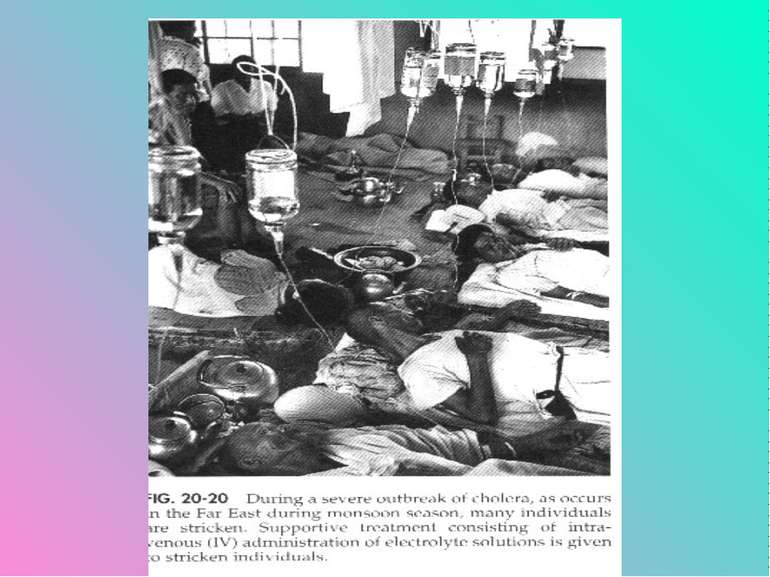
Профілактика і лікування Основним у профілактиці холери є раннє виявлення хворих і вібріоносіїв, їх госпіталізація, виявлення й обсервація всіх контактованих осіб. Необхідно провести профілактичну й заключну дезинфекцію в осередку захворювання. Важливе значення мають карантинні заходи, включаючи охорону державних кордонів від заносу інфекції. Локалізацію й ліквідацію вогнища холери проводять надзвичайні протиепідемічні комісії області, міста, району. Особи, які були у тісному контакті з хворими на холеру, підлягають екстренній профілактиці тетрацикліном. З цією метою їм дають по 0,3 г препарату 3 рази на день протягом 4 діб. Проводиться також широка санітарно-освітня робота серед населення. Специфічна профілактика не проводиться, оскільки всі три типи вакцин (жива, вбита, холероген-анатоксин) виявилися малоефективними. Лікують хворих еритроміцином, тетрацикліном, метацикліном, доксацикліном або левоміцетином протягом не менше 5 днів.
Схожі презентації
Категорії