Презентація на тему:
"Уксусная кислота"
Завантажити презентацію
"Уксусная кислота"
Завантажити презентаціюПрезентація по слайдам:
Презентация на тему : «Уксусная кислота» Выполнила: ученица 11-Б класса Зануда Т.А Проверила: учитель химии Тисленко Л.А
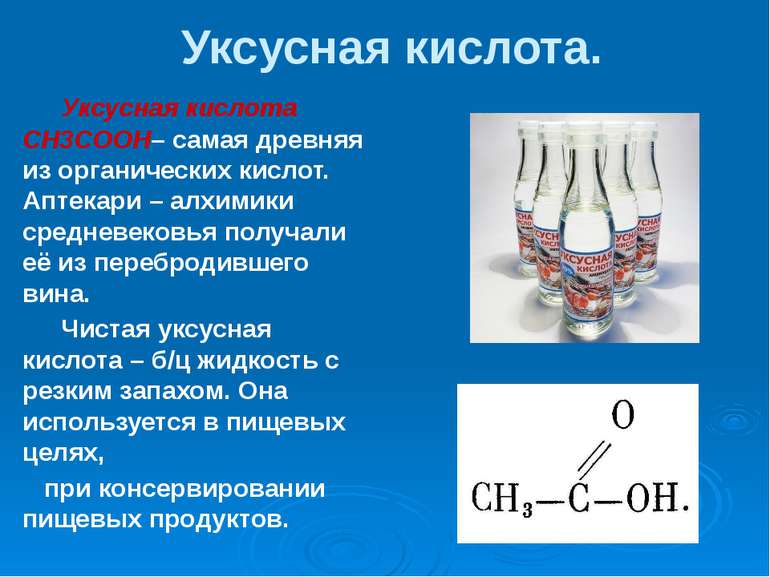
Уксусная кислота. Уксусная кислота СН3СООН– самая древняя из органических кислот. Аптекари – алхимики средневековья получали её из перебродившего вина. Чистая уксусная кислота – б/ц жидкость с резким запахом. Она используется в пищевых целях, при консервировании пищевых продуктов.
История открытия кислоты Уксусная кислота известна с древнейших времен, так как образуется при скисании вин (винный уксус). Водный разбавленный раствор этого вещества называется уксусом. Слово «уксус» происходит от греческого слова «oxys», означающего «кислый». В древности уксус был единственной пищевой кислотой, получаемой при скисании виноградного вина, и это объясняет, что его название древними греками отождествлялось с самим представлением о кислом, кислоте. В России уксус называли «кислой влажностью» или «древесной кислотой». Это связано с получением уксусной кислоты при сухой перегонке древесины лиственных пород, прежде всего березы. Получение уксуса при сухой перегонке древесины описано в сочинениях Иоганна Глаубера и Роберта Бойля
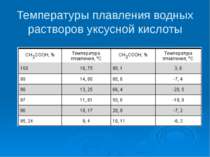
Характеристика Уксусная кислота принадлежит к слабым кислотам. Она во всех отношениях смешивается с водой, спиртом, эфиром, бензолом и нерастворима в сероуглероде. При разбавлении уксусной кислоты водой происходит сокращение объёма раствора.
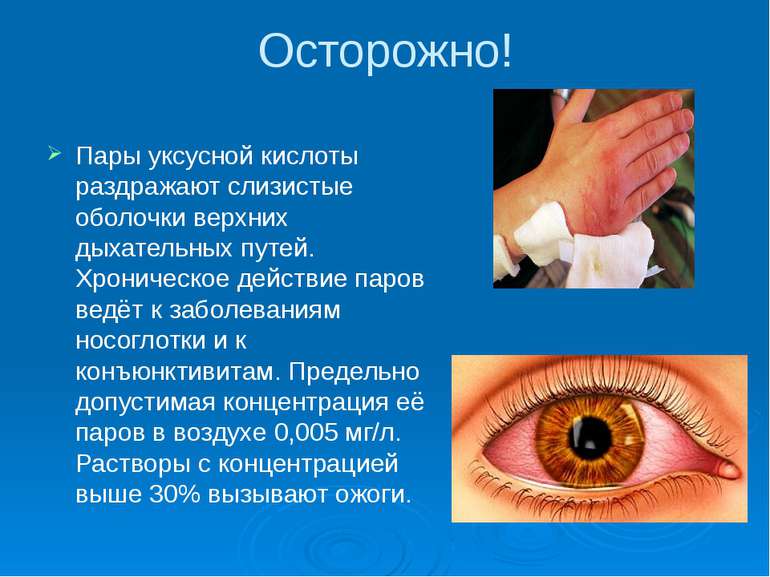
Осторожно! Пары уксусной кислоты раздражают слизистые оболочки верхних дыхательных путей. Хроническое действие паров ведёт к заболеваниям носоглотки и к конъюнктивитам. Предельно допустимая концентрация её паров в воздухе 0,005 мг/л. Растворы с концентрацией выше 30% вызывают ожоги.
Химические свойства С сильными металлами Mg + 2CH3COOH → (CH3COO)2Mg + H2 С солями CH3COOH + NaHCO3 = CH3COONa + H2O + CO2 Диссоциация СН3СООН → Н+ + СН3СООˉ Реакция нейтрализации CH3COOH + NaOH --> CH3COONa + H2О
Гидрирование С2H2+2H20=CH3COOH+H2↑ Окисление С оксидами CH3COOH+MgO=(CH3COO)2+2H2O Реакция этерификации CH3COOH+C2H5OH=CH3COOC2H5+H2O
Физические свойства Уксусная кислота представляет собой бесцветную жидкость с характерным резким запахом и кислым вкусом. Гигроскопична. Неограниченно растворима в воде. Смешивается со многими растворителями; в уксусной кислоте хорошо растворимы неорганические соединения и газы, такие как HF, HCl, HBr, HI и другие. Агрегатное состояние Жидкое Цвет Бесцветная прозрачная жидкость Запах Резкий уксусный Растворимость в воде Хорошая Температура кипения 1180С Температура плавления 170С
Применение уксусной кислоты Значительные количества уксусной кислоты идут на производство ацетона, ацетилцеллюлозы, синтетических красителей, используются при крашении и печатании тканей и в пищевой промышленности. Основные соли уксусной кислоты Al, Fe, Cr и другие служат протравами при крашении; они обеспечивают прочную связь красителя с текстильным волокном.
Их широко применяют как растворители (особенно этилацетат) для нитроцеллюлозных лаков, глифталевых и полиэфирных смол, в производстве киноплёнки и целлулоида, а также в пищевой промышленности и парфюмерии. В производстве полимеров значительную роль играют искусственные волокна, лаки и клеи на основе винилацетата.
Схожі презентації
Категорії