Презентація на тему:
Саліцилова кислота
Завантажити презентацію
Саліцилова кислота
Завантажити презентаціюПрезентація по слайдам:
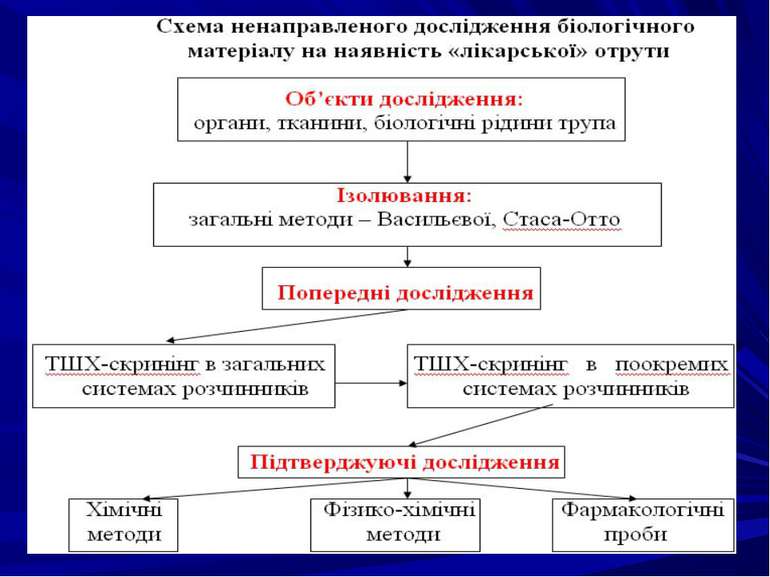
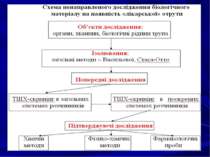
Принципова схема ідентифікації та кількісного визначення речовин, які ізолюються екстракцією полярними розчинниками. Хіміко-токсикологічний аналіз „лікарських” отрут кислого, нейтрального і слабоосновного характеру Доц. Михалків М.М. Лекція № 7
План. Принципова схема аналізу ”лікарських” отрут. ТШХ-скринінг ”лікарських” отрут. Хімічні методи дослідження ”лікарських” отрут. Фізико-хімічні методи ідентифікації отрут. Фармакологічні проби ”лікарських” отрут. Кількісне визначення ”лікарських” отрут. Застосування, токсикологічна характеристика, методи виділення з біологічного матеріалу і методи аналізу похідних саліцилової кислоти. Застосування, токсикологічна характеристика, методи виділення з біологічного матеріалу і методи аналізу похідних барбітурової кислоти. Застосування, токсикологічна характеристика, методи виділення з біологічного матеріалу і методи аналізу похідних піразолону.
1. Принципова схема аналізу “лікарських” отрут. Вибір методів дослідження лікарських отрут Судово-хімічне дослідження біологічного матеріалу Етапи Хіміко-токсикологічне дослідження біологічних рідин живої людини Паперова хроматографія Розділення ТШХ ТШХ Газо-рідинна хроматографія Екстракція ВЕРХ Хімічні методи Виявлення Фізико-хімічні методи Фізико-хімічні методи Імунохімічні методи Фармакологічні проби на тваринах Фізико-хімічні методи Кількісне визначення Фізико-хімічні методи Імунохімічні методи
2. ТШХ-скринінг “лікарських” отрут Переваги методу ТШХ: - розділення препаратів та їх метаболітів; - очистка від домішок; - ідентифікація групи препаратів або індивідуальної речовини; - кількісна оцінка аналізованого препарату. Негативний результат попереднього дослідження навіть на першій стадії скринінгу свідчить про відсутність токсичних доз лікарських препаратів в екстрактах із біологічного матеріалу.
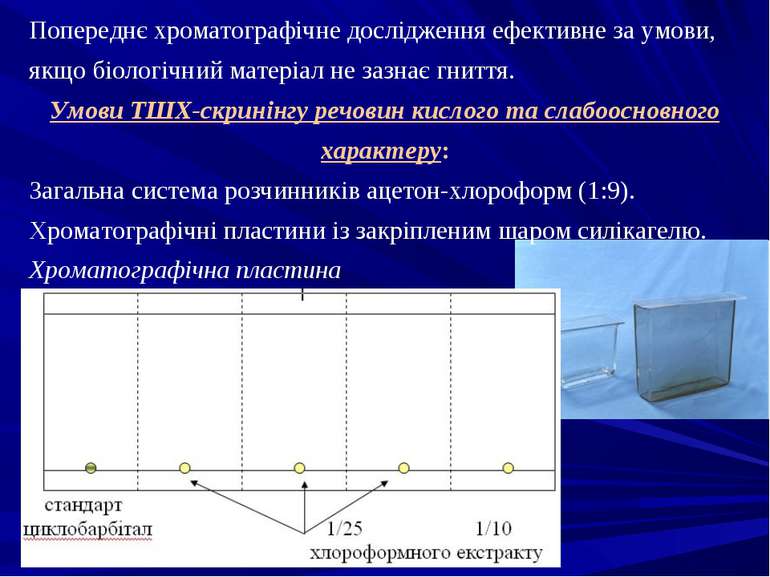
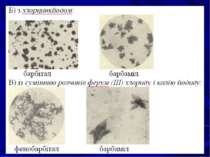
Попереднє хроматографічне дослідження ефективне за умови, якщо біологічний матеріал не зазнає гниття. Умови ТШХ-скринінгу речовин кислого та слабоосновного характеру: Загальна система розчинників ацетон-хлороформ (1:9). Хроматографічні пластини із закріпленим шаром силікагелю. Хроматографічна пластина
Елюенти: - з хроматографічної зони 1 метанол; - з хроматографічних зон 2 та 3 ацетон. Окремі системи розчинників: - похідні піразолону, алкалоїди (зона 1): ацетон-циклогексан (5:1), сорбент - оксид алюмінію; - барбітурати, похідні 1,4-бензодіазепіну (зона 2): хлороформ-бутанол-25%-вий розчин аміаку (70:40:5), сорбент - силікагель КСК, забуферений розчином борної кислоти; - похідні 1,4-бензодіазепіну (зона 3): етилацетат-бензол-етанол-25%-вий розчин аміаку (90:15:5:2,5), сорбент - силікагель КСК.
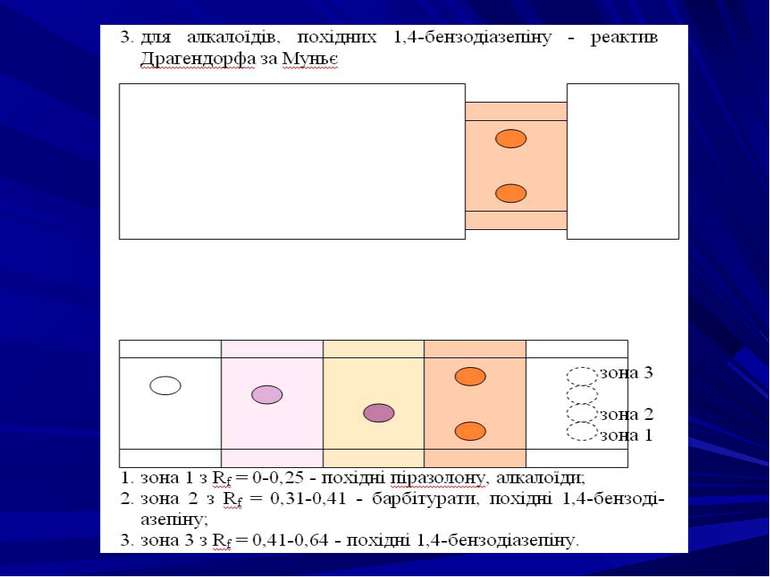
Умови ТШХ-скринінгу речовин основного та слабоосновного характеру: Загальна система розчинників хлороформ-діоксан-ацетон-25%-вий розчин аміаку (45:47,5:5:2,5). Хроматографічні пластини із закріпленим шаром силікагелю. Стандарт етаперазин. Проявники: - для похідних фенотіазину - 10%-вий розчин H2SO4 в етанолі; - для похідних фенотіазину, піразолону - 5 або 10%-вий розчин FеСl3; - для алкалоїдів, похідних 1,4-бензодіазепіну, п-амінобензойної кис лоти - реактив Драгендорфа за Муньє.
Хроматографічні зони: зона 1 з Rf = 0,12-0,36 — алкалоїди; зона 2 з Rf=0,50-0,58 — похідні піразолону, пурину, фенотіазину; зона 3 з Rf = 0,63-0,83 — похідні 1,4-бензодіазепіну, фенотіазину, п-амінобензойної кислоти; зона 4 з Rf = 0,67-0,98 — алкалоїди, похідні 1,4-бензодіазепіну, фенотіазину.
Елюенти: - зона 1: суміш метанол-діетиламін (9:1); зони 2-4: суміш метанол-25%-вий розчин аміаку (9:1). Окремі системи розчинників: алкалоїди (зона 1): хлороформ-діетиламін (9:1), сорбент - силікагель КСК; пурини, похідні піразолону, фенотіазину (зона 2): хлороформ - етанол (5:1), сорбент - алюміній оксид; похідні 1,4-бензодіазепіну, фенотіазину, п-амінобензойної кислоти (зона 3): хлороформ-етанол (20:1), сорбент - алюміній оксид; алкалоїди, похідні 1,4-бензодіазепіну, фенотіазину (зона 4): циклогексан-ацетон (5:1), сорбент - оксид алюмінію.
3. ХІМІЧНІ МЕТОДИ ДОСЛІДЖЕННЯ “ЛІКАРСЬКИХ” ОТРУТ КОЛЬОРОВІ РЕАКЦІЇ Процеси, які лежать в основі: віднімання води (за допомогою концентрованої H2SO4); окислення препаратів (К2Сr2O7 у присутності концентрованої H2SО4); одночасне окислення і віднімання води; конденсація з альдегідами в присутності речовин, які поглинають воду. Умови: високий ступінь чистоти хлороформних витяжок.
Переваги: можливість виключення окремих “лікарських” отрут та їх груп; можливість встановити наявність окремих отрут і навіть груп отрут (реактив Маркі орієнтує на пошук алкалоїдів – похідних ізохіноліну); Недоліки: неспецифічність, невисока чутливість, нестійкість отриманого забарвлення.
РЕАКЦІЇ ОСАДЖЕННЯ Процеси, які лежать в основі: - утворення солей, важкорозчинних у водному середовищі: при взаємодії алкалоїдів з фосфомолібдатною кислотою (реактив Зонненшейна); з фосфовольфрамовою кислотою (реактив Шейблера); пікриновою кислотою, таніном та ін.; - утворення комплексів з важкими металами, майже не розчинних у водному середовищі (при взаємодії алкалоїдів з реактивами Драгендорфа, Марме, Майєра).
Переваги: висока чутливість (найбільшою чутливістю характеризуються фосфомолібдатна, фосфовольфрамова кис лоти та реактив Драгендорфа, найменшою - танін); Недолік: неспецифічність. Хіміко-токсикологічне значення осадових реакцій з реактивами групового осадження алкалоїдів має негативний результат.
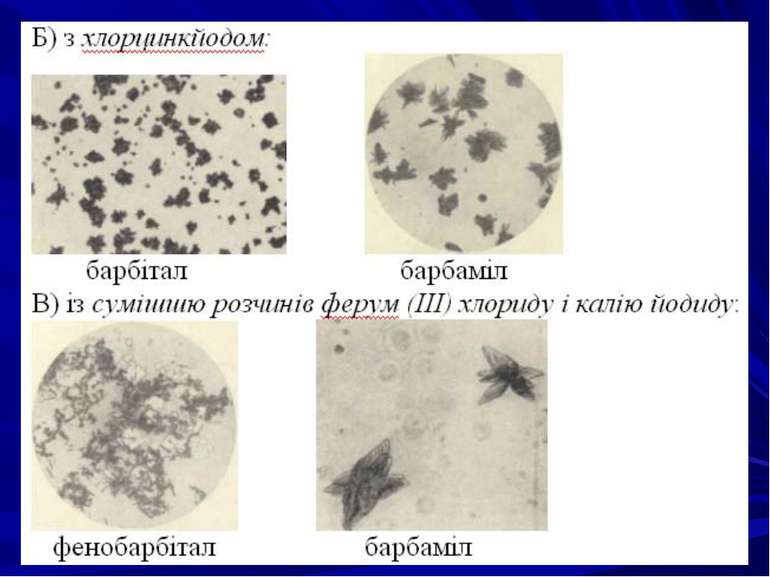
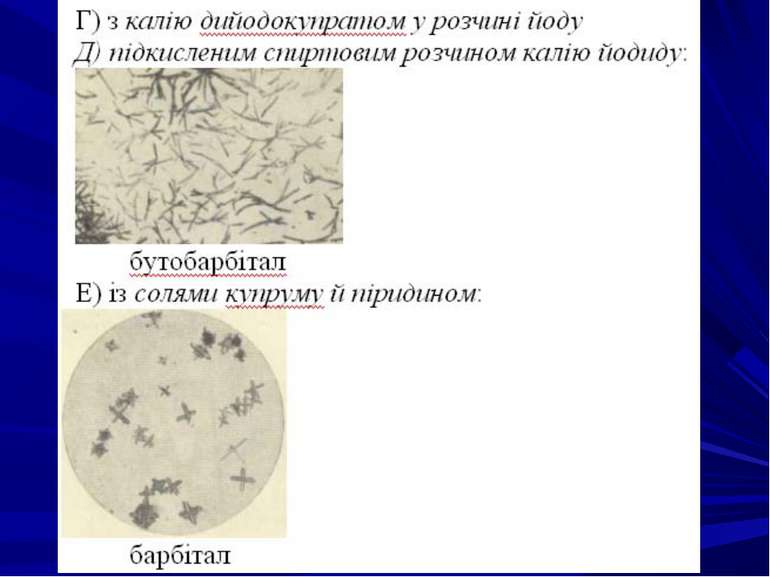
МІКРОКРИСТАЛОСКОПІЧНІ РЕАКЦІЇ Переваги: реакції високочутливі й специфічні щодо умов лабораторії, в якій проводяться дослідження. Недоліки: форма кристалів, які утворюються, залежить від багатьох факторів (концентрації досліджуваної речовини, концентрація реактиву, співвідношення об’ємів розчинів досліджуваної речовини та реактиву, температури, рН середовища, наявності домішок, поліморфізм кристалів).
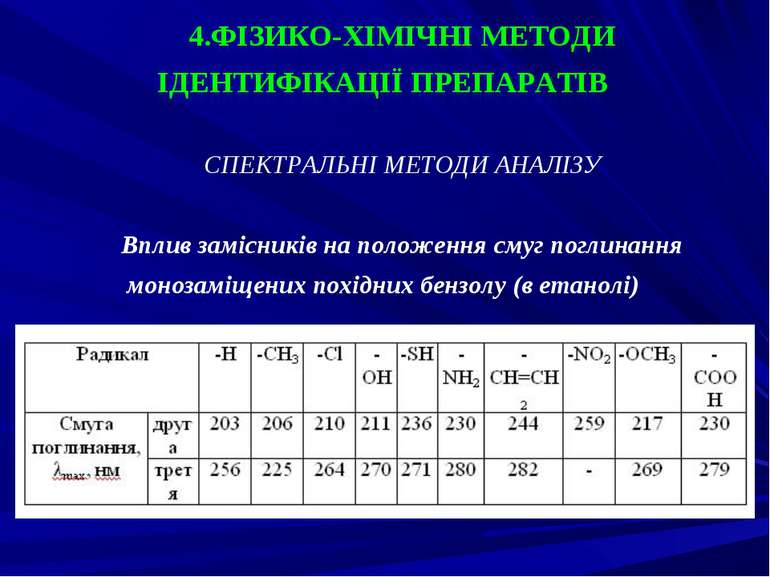
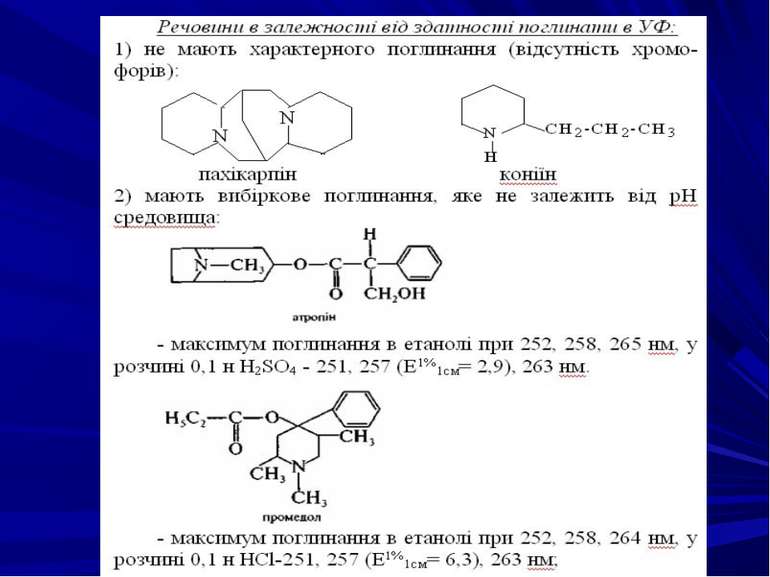
ФІЗИКО-ХІМІЧНІ МЕТОДИ ІДЕНТИФІКАЦІЇ ПРЕПАРАТІВ СПЕКТРАЛЬНІ МЕТОДИ АНАЛІЗУ Вплив замісників на положення смуг поглинання монозаміщених похідних бензолу (в етанолі)
Метод УФ-спектрофометрії чутливий для проведення кількісного визначення, досить точний, але вимагає ретельного очищення аналізованих речовин від супутніх домішок. ХРОМАТОГРАФІЧНІ МЕТОДИ АНАЛІЗУ Ідентифікація “лікарських” отрут методами ГРХ і ВЕРХ проводиться за параметрами утримування.
6. КІЛЬКІСНЕ ВИЗНАЧЕННЯ “ЛІКАРСЬКИХ” ОТРУТ У хіміко-токсикологічному аналізі для кількісного визначення токсичних речовин, виділених з біологічного матеріалу та інших об’єктів, застосовуються: чутливі фотоколориметричні, спектро фотометричні, газохроматографічні і деякі інші методи.
Причини заниження результатів кількісного аналізу: Токсичні речовини в організмі значною мірою піддаються метаболізму, нерівномірно розподіляються в органах і тканинах. В одних органах ці речовини знаходяться в більших кількостях, ніж в інших, а в деяких можуть бути відсутні. Тому результати хіміко-токсикологічного аналізу залежать від правильного вибору органів і тканин, що направляються на дослідження. Отруйні речовини в організмі зв’язуються з білковими та іншими сполуками. Кількість речовин, що переходять у витяжки з біологічного матеріалу, залежить від методу, який застосовується при виділенні токсичних речовин. Кількість токсичних речовин, виділених з біологічного матеріалу, залежить також від ступеня гнилісного розкладу досліджуваних об’єктів та ряду інших чинників.
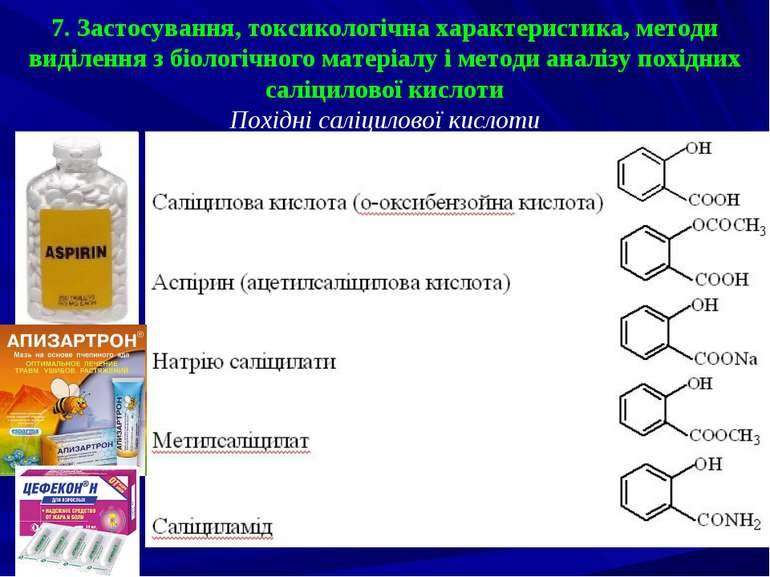
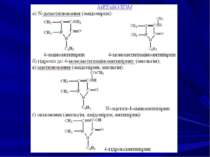
7. Застосування, токсикологічна характеристика, методи виділення з біологічного матеріалу і методи аналізу похідних саліцилової кислоти Похідні саліцилової кислоти
Токсична дія При вживанні лікувальних доз саліцилатів можливі побічні явища: шум у вухах, ослаблення слуху, набряки, печія, блювання. Токсичні дози призводять до загострення бронхіальної астми, появи алергічних реакцій, зменшення синтезу захисного слизу в шлунку й утворення численних виразок слизової оболонки. При порушеннях згортання крові, особливо при гемофілії, саліцилати сприяють розвитку кровотечі. При підвищенні доз з’являються нервово-психічні порушення, які виражаються в дискоординації мови, занепокоєнні, судомах, порушенні дихання, що призводить до летального наслідку. Летальна доза саліцилатів: 2-4 г - для дітей, близько 20 г - для дорослих.
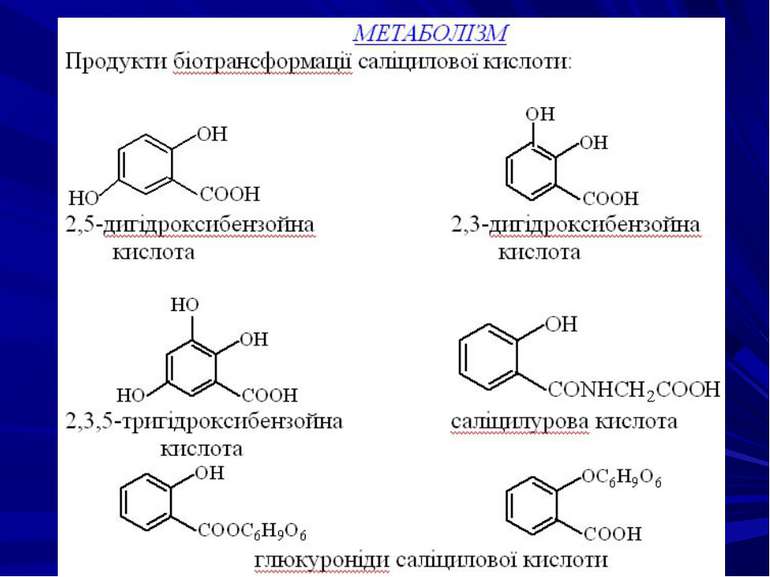
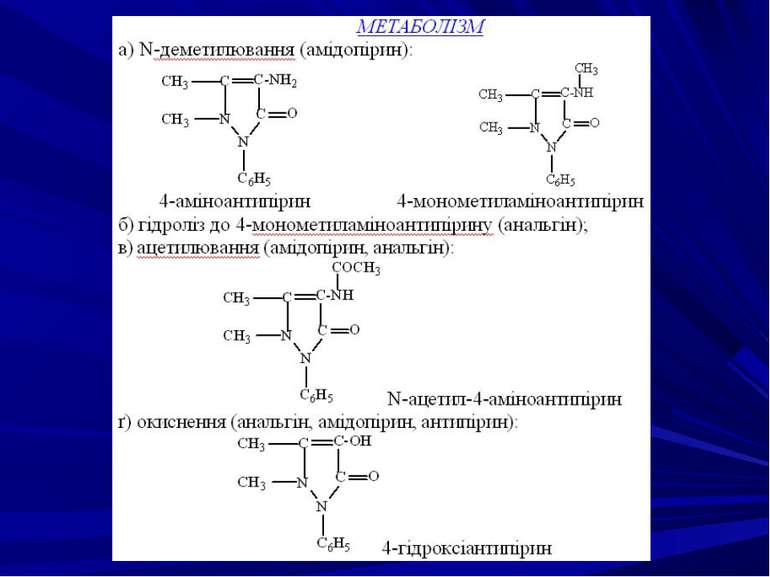
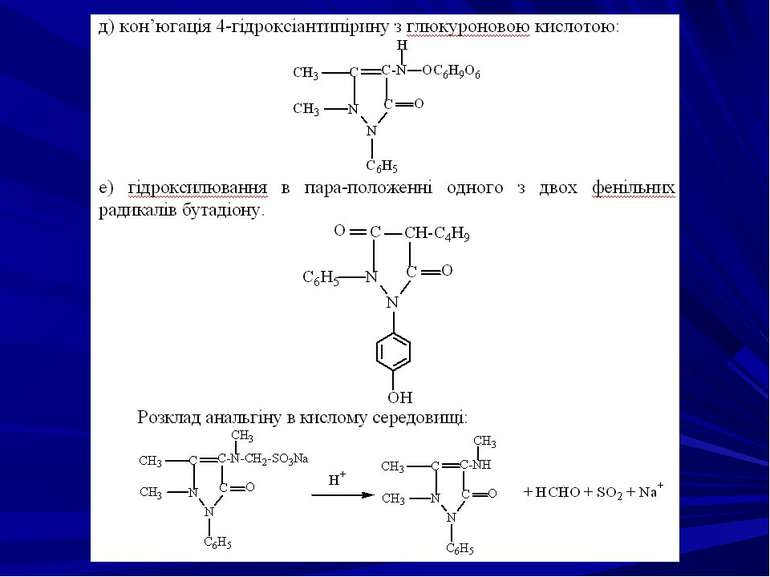
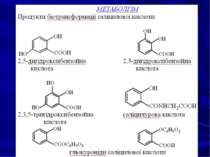
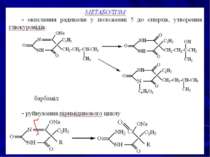
Поведінка в організмі При пероральному вживанні саліцилова кислота швидко всмоктується в шлунку, велика її частина зв’язується з білками плазми, виділяється нирками в незміненому вигляді або у вигляді метаболітів. Ефіри саліцилової кислоти частково піддаються гідролізу в тонкому кишечнику. Саліцилова кислота та її похідні метаболізуються в печінці в таких напрямках: гідроліз; окислення, гідроксилювання; утворення кон’югатів з глюкуроновою кислотою і гліцином. Саліциламід переважно виводиться з організму в незміненому вигляді.
Направлений хіміко-токсикологічний аналіз похідних саліцилової кислоти Дослідження на наявність саліцилової кислоти в біологічних об’єктах проводиться за спеціальним завданням або в разі навідних вказівок у матеріалах справи, а також за появи на склі після видалення хлороформу характерного залишку у вигляді голок. Об’єкти дослідження - шлунок, кишечник, печінка, нирки, кров, сеча, продукти харчування.
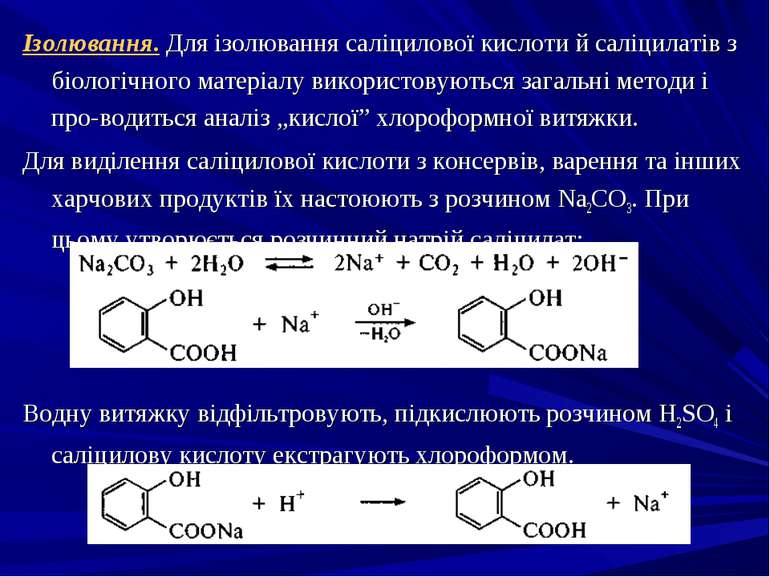
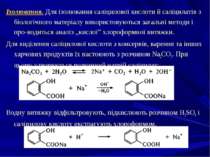
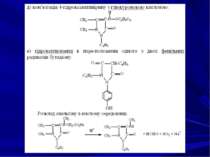
Ізолювання. Для ізолювання саліцилової кислоти й саліцилатів з біологічного матеріалу використовуються загальні методи і про водиться аналіз „кислої” хлороформної витяжки. Для виділення саліцилової кислоти з консервів, варення та інших харчових продуктів їх настоюють з розчином Na2CO3. При цьому утворюється розчинний натрій саліцилат: Водну витяжку відфільтровують, підкислюють розчином H2SO4 і саліцилову кислоту екстрагують хлороформом.
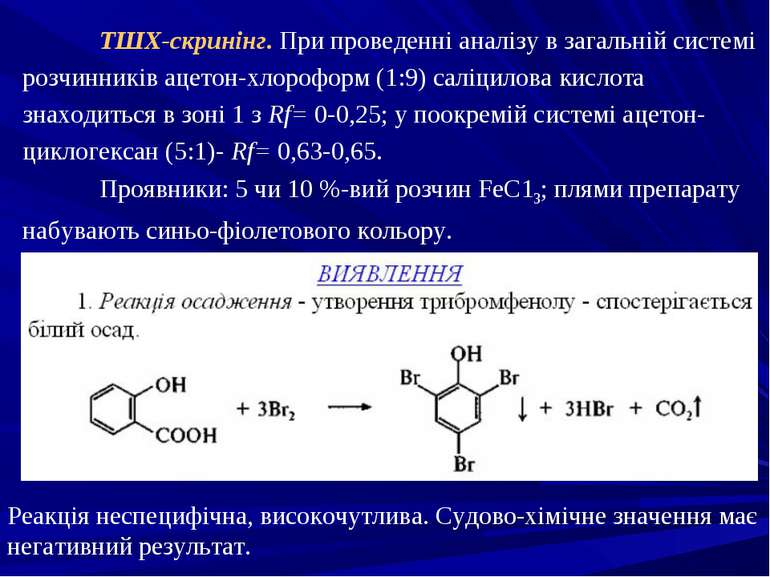
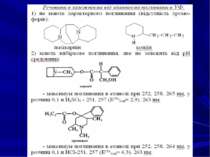
ТШХ-скринінг. При проведенні аналізу в загальній системі розчинників ацетон-хлороформ (1:9) саліцилова кислота знаходиться в зоні 1 з Rf= 0-0,25; у поокремій системі ацетон-циклогексан (5:1)- Rf= 0,63-0,65. Проявники: 5 чи 10 %-вий розчин FеС13; плями препарату набувають синьо-фіолетового кольору. Реакція неспецифічна, високочутлива. Судово-хімічне значення має негативний результат.
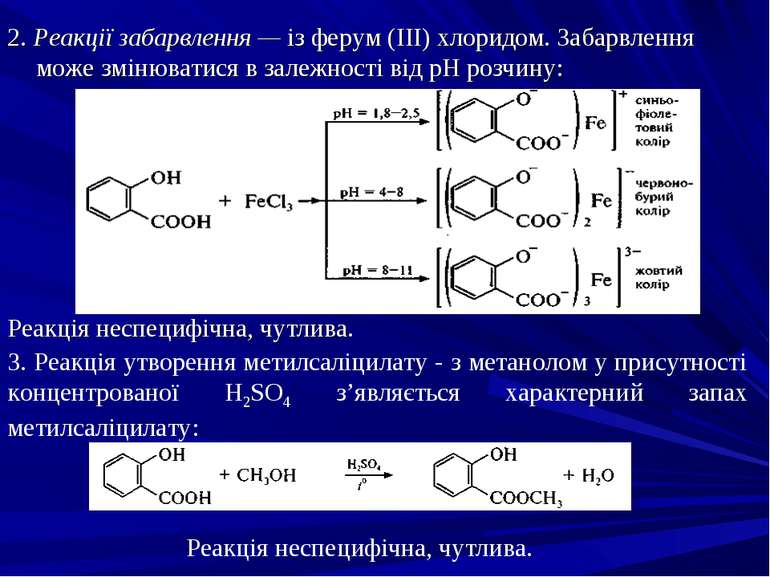
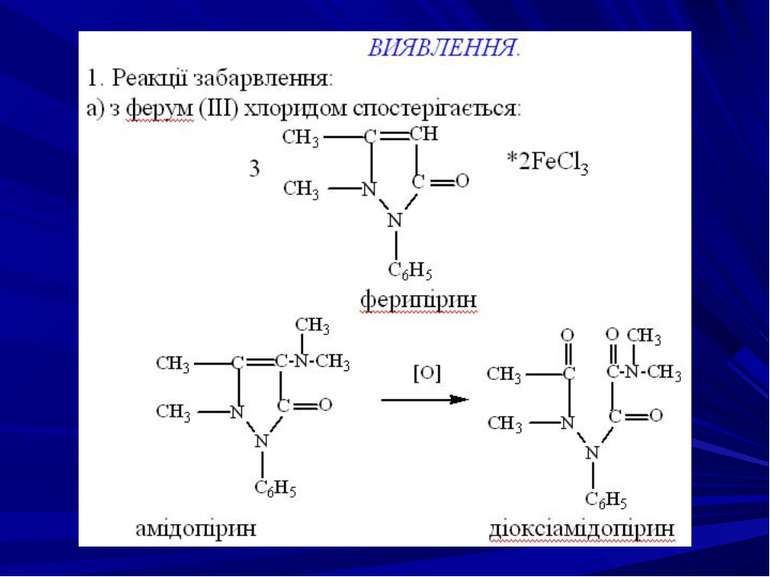
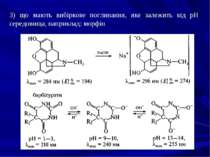
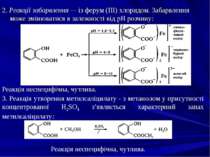
2. Реакції забарвлення — із ферум (III) хлоридом. Забарвлення може змінюватися в залежності від рН розчину: Реакція неспецифічна, чутлива. 3. Реакція утворення метилсаліцилату - з метанолом у присутності концентрованої H2SO4 з’являється характерний запах метилсаліцилату: Реакція неспецифічна, чутлива.
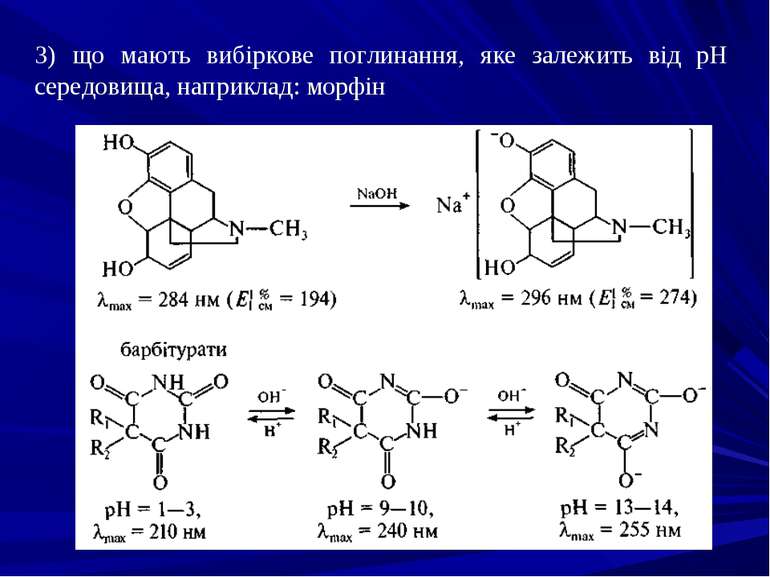
4. Виявлення саліцилової кислоти за УФ-спектрами: а) у 0,5 моль/л розчині NaOH - max = 300 нм; б) у 0,05 моль/л розчині H2SО4 - max = 302 нм. 5. Ідентифікація хроматографічними методами: ГРХ; ВЕРХ; ТШХ. Кількісний аналіз: при дослідженні біологічного об’єкта і харчових продуктів – спектральними методами (УФ-спектрофотометрія, фотоколориметрія, екстракційна фотометрія), хроматографічними методами (ГРХ; ВЕРХ; ТШХ); при дослідженні лікарських препаратів – об’ємними методами (нейтралізація, броматометрія).
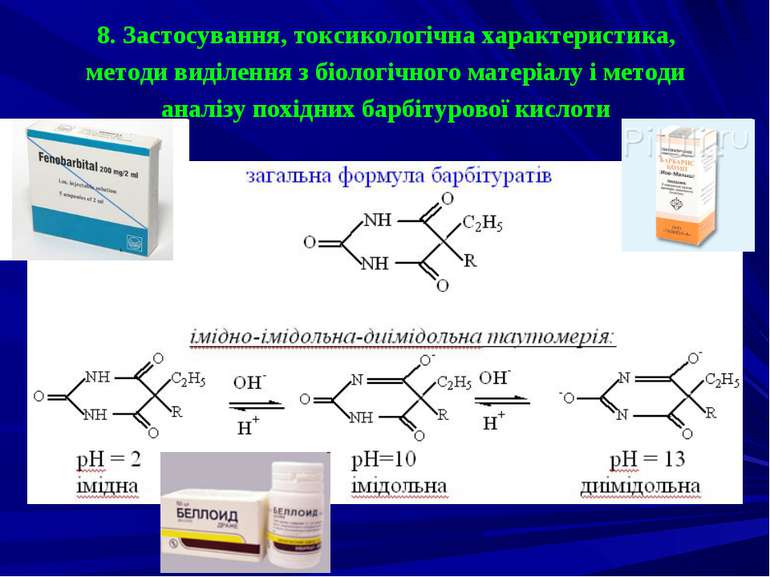
8. Застосування, токсикологічна характеристика, методи виділення з біологічного матеріалу і методи аналізу похідних барбітурової кислоти
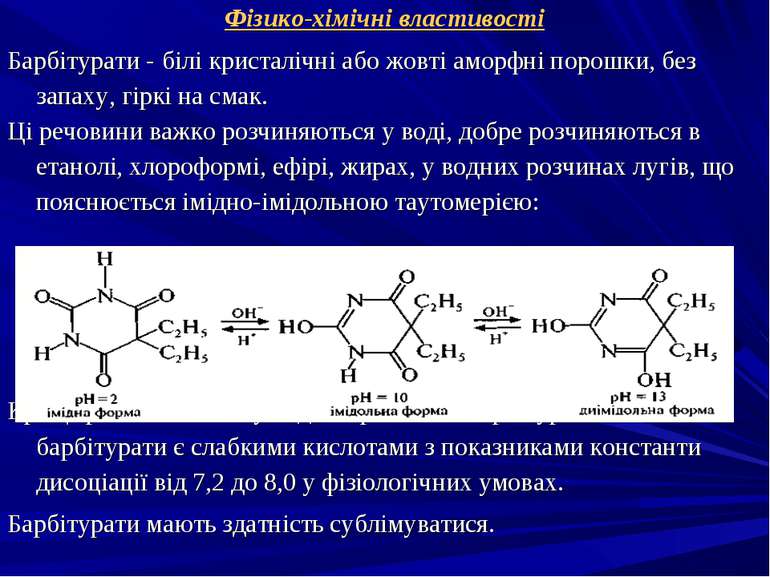
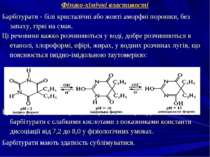
Фізико-хімічні властивості Барбітурати - білі кристалічні або жовті аморфні порошки, без запаху, гіркі на смак. Ці речовини важко розчиняються у воді, добре розчиняються в етанолі, хлороформі, ефірі, жирах, у водних розчинах лугів, що пояснюється імідно-імідольною таутомерією: Краще розчинюються у воді натрієві солі барбітуратів. Усі барбітурати є слабкими кислотами з показниками константи дисоціації від 7,2 до 8,0 у фізіологічних умовах. Барбітурати мають здатність сублімуватися.
Токсична дія Тривале вживання терапевтичних доз барбітуратів призводить до кумуляції їх в організмі. При отруєнні легкого ступеня барбітуратами відзначаються загальмований стан (поведінка млява, хода невпевнена), зниження частоти дихання. Спостерігаються розлади мови й зору, підвищена пітливість. При важких отруєннях барбітуратами настає стан наркозу, що швидко переходить у важку кому, при цьому відзначаються порушення дихання, неврологічні розлади, зниження сухожильних рефлексів та реакції зіниць на світло. Смерть настає через набряк легень і параліч дихання.
Деякі речовини (наркотики, алкоголь, транквілізатори) підсилюють токсичну дію барбітуратів. Особлива небезпека пов’язана з депресивною дією на дихальний центр препаратів опію, алкоголю, окису вуглецю. Смертельні дози: одномоментний прийом близько 10 терапевтичних разових доз кожного з препаратів або їх суміші: для барбіталу – 3-4, фенобарбіталу - 1,4-2, барбамілу – 4-6, натрію етаміналу - 1 г.
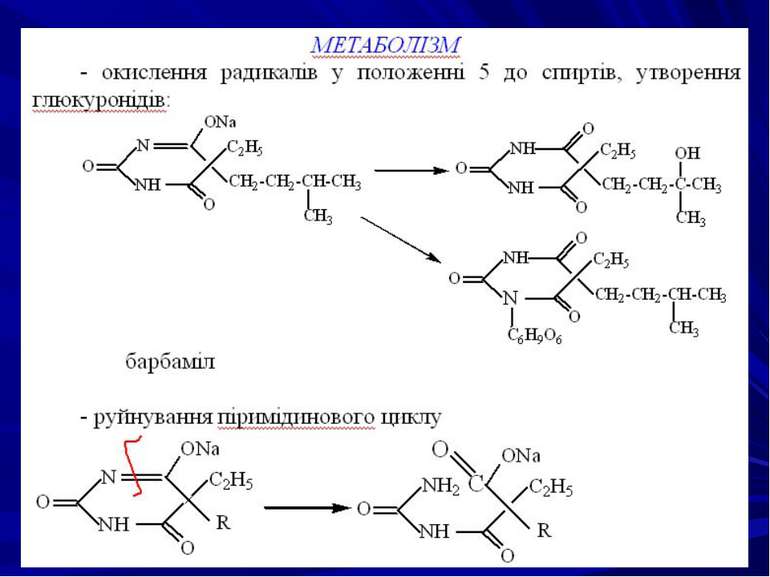
Поведінка в організмі Барбітурати швидко всмоктуються в шлунку. З організму виводяться із сечею в незміненому вигляді або у вигляді метаболітів. Сила і тривалість дії барбітуратів залежать від їх метаболізму. Барбітурати розподіляються в усіх тканинах та біологічних рідинах організму, але їх концентрація може бути різною у залежності від жиророзчинності, зв’язку з білками, ступеня іонізації молекул, інтенсивності кровообігу в тка нинах та ін.
Направлений хіміко-токсикологічний аналіз похідних барбітурової кислоти Об’єкти дослідження. Печінка, нирки, мозок, селезінка, вміст шлунка, кров, сеча. Ізолювання. При направленому дослідженні на барбітурати використовуються поокремі методи ізолювання - екстракція водним розчином натрій гідроксиду (метод Валова) і екстракція водою, підкисленою сульфатною кислотою (метод В. І. Попової).
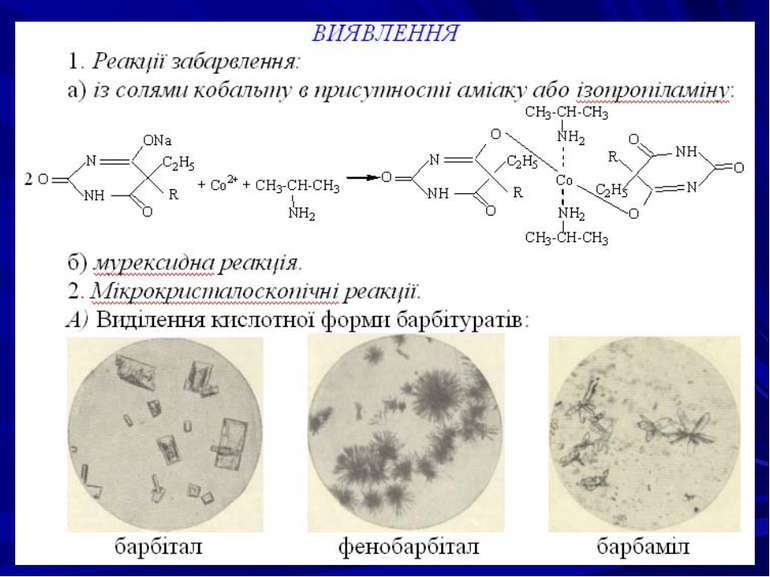
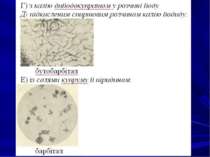
ТШХ-скринінг. При проведенні аналізу в загальній системі розчинників ацетон-хлороформ (1:9) барбітурати знаходяться в другій зоні зі значеннями величини Rf= 0,31-0,41. Як проявник барбітуратів використовують 5%-вий розчин меркурій сульфату і 0,1 %-вий розчин дифенілкарбазону в хлороформі. За наявності барбітуратів з’являються плями, забарвлені в синьо-фіолетовий або червоно-фіолетовий колір. Потім препарати елююють із шару сорбенту ацетоном і елюати досліджують у поокремій системі хлороформ-н-бутанол-25 %-вий розчин аміаку (70:40:5), сорбент - силікагель КСК, забуферений 0,1 н розчином борної кислоти. Ідентифікація індивідуальних барбітуратів проводиться в присутності “свідків”.
3. Фізико-хімічні методи ідентифікації: виявлення за УФ- та ІЧ-спектрами; методи ТШХ, ГРХ, ВЕРХ. Кількісне визначення барбітуратів при хіміко-токсикологічному аналізі Проводиться фізико-хімічними методами: спектральними (УФ-спектрофотометрія, фотоколориметрія, диференційна спектрофотометрія, екстракційна фотометрія); хроматографічними (тонкошарова хроматографія, газо-рідинна і рідинна хроматографії). Найбільш перспективним із перелічених методів є диференційна спектрофотометрія.
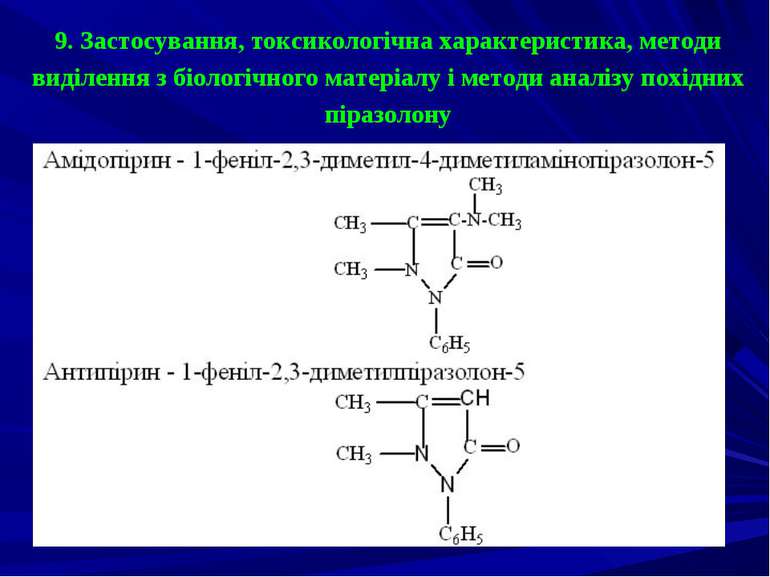
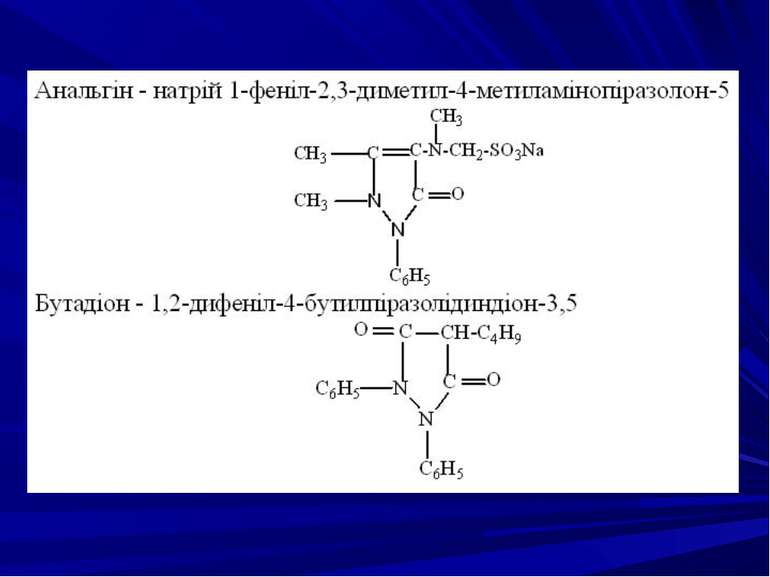
9. Застосування, токсикологічна характеристика, методи виділення з біологічного матеріалу і методи аналізу похідних піразолону
Токсична дія Інтоксикація препаратами обумовлена передозуванням, підвищеною чутливістю до зазначених препаратів, неправильним їх зберіганням. При тривалому вживанні препаратів виникає небезпека хронічного отруєння. Анальгін при повторному впливі на організм викликає ознаки анемії, має нефротоксичну й у меншій мірі - гепатотоксичну дії. Летальна доза похідних піразолону 5-15 г.
Направлений хіміко-токсикологічний аналіз похідних піразолону Об’єкти дослідження. Шлунок, кишечник, печінка, нирки, кров, сеча. Ізолювання. Проводиться загальними методами (Стаса-Отто або О.О. Васильєвої), препарати можуть бути знайдені в “кислій” і “лужній” хлороформних витяжках. При направленому методі аналізу можна використати окремий метод екстракції похідних піразолону з органів: водну кислу витяжку відразу підлужують аміаком до рН=8,5-10 і проводять екстракцію хлороформом. При дослідженні біологічних рідин похідні піразолону вилучаються органічними розчинниками з підкислених об’єктів у присутності висолювачів з попереднім осадженням білків у разі потреби.
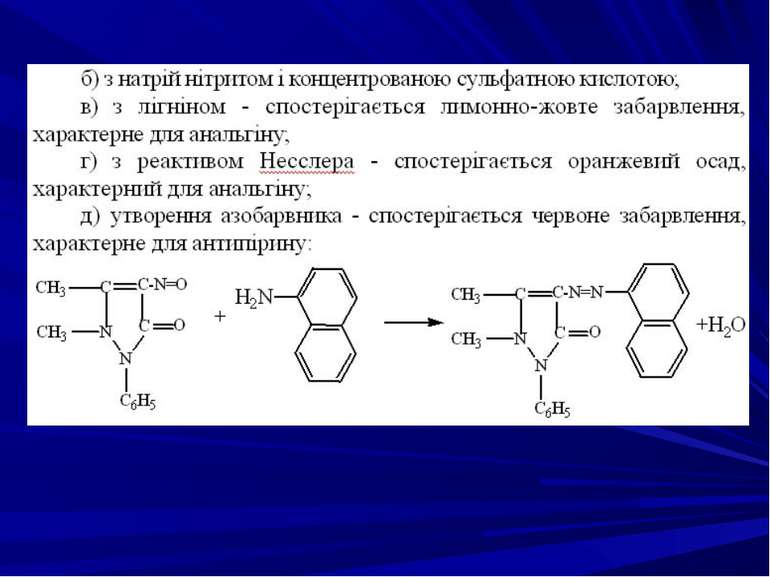
ТШХ-скринінг. Похідні піразолону при проведенні досліджень “кислої” хлороформної витяжки в загальній системі розчинників ацетон-хлороформ (1:9) потрапляють у зону 1 із значеннями Rf= 0-0,25. Проявник: 5 %-вий розчин FеС13 реактив Драгендорфа. Після елюювання метанолом препарати аналізують у поокремій системі ацетон-циклогексан (5:1), сорбент - основний оксид алюмінію. Похідні піразолону при проведенні досліджень “лужної” хлороформної витяжки в загальній системі розчинників хлороформ-діоксан-ацетон- 25 %-вий розчин аміаку (45:47,5:5:2,5) потрапляють у зони 2 і 3 із значеннями Rf= 0,50-0,58 і 0,63-0,83 відповідно. Після елюювання сумішшю метанол-25%-вий розчин аміаку (9:1) препарати аналізують у системах хлороформ-ацетон (5:1) і хлороформ-етанол (20:1).
2. Фізико-хімічні методи ідентифікації: виявлення препаратів за УФ- та ІЧ-спектрами; хроматографічними методами (ГРХ, ВЕРХ, ТШХ). Кількісне визначення похідних піразолону проводиться УФ-спектрофотометричним, фотоколориметричним (в основу якого покладені кольорові реакції амідопірину з бромфеноловим синім, анальгіну з бензохіноном в оцтовокислому середовищі, бутадіону з бензидином), а також хроматографічними (ГРХ, ВЕРХ, ТШХ) методами.
Схожі презентації
Категорії