Презентація на тему:
Оксиди, їх склад, назви.
Завантажити презентацію
Оксиди, їх склад, назви.
Завантажити презентаціюПрезентація по слайдам:
Мета. На прикладі найпростіших за складом і будовою хімічних сполук почати вивчення основних класів неорганічних сполук. Закріпити навички складання формул оксидів та називати їх. Поглибити знання про реакції сполучення, їх роль в утворенні оксидів.
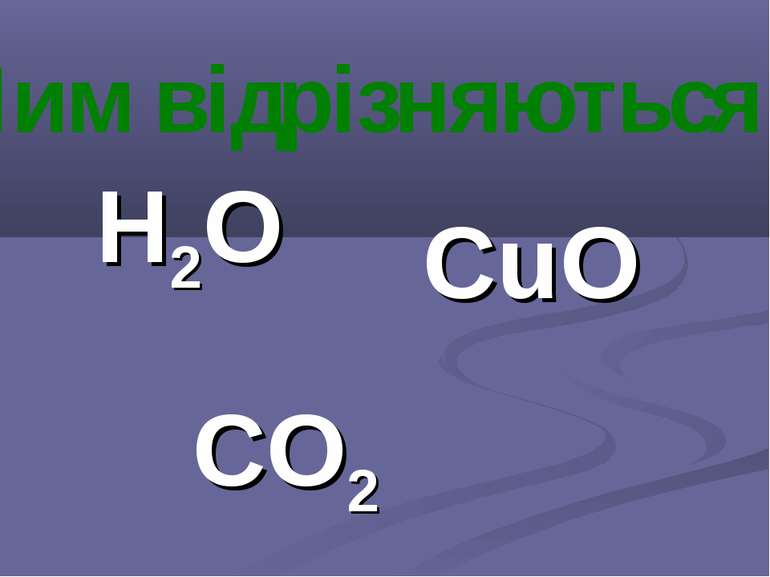
БІНАРНІ СПОЛУКИ Оксиди – це складні речовини, утворені двома елементами, одним з яких обов'язково є Оксиген.
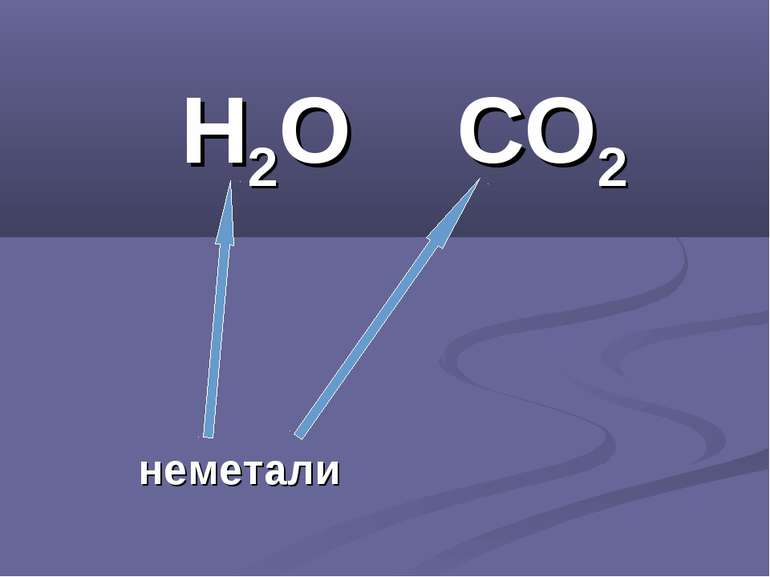
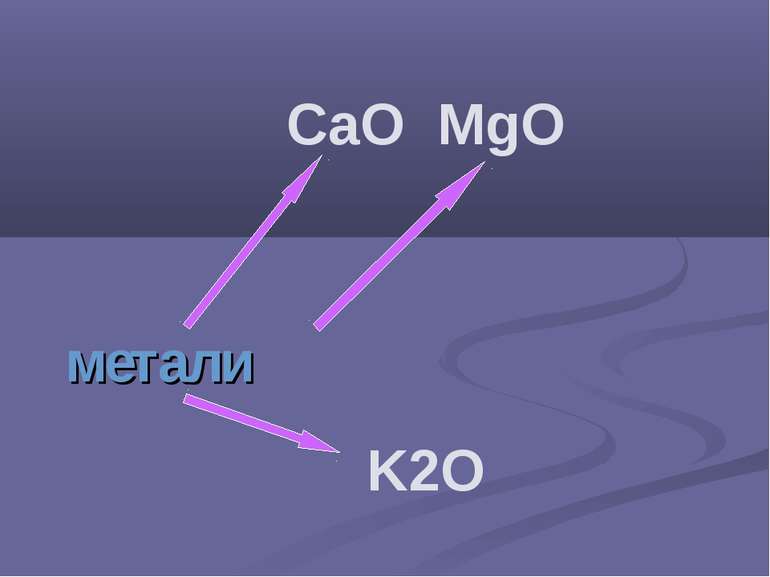
метали і неметали з киснем утворюють оксиди. За складом оксиди поділяють на оксиди металів і оксиди неметалів. Оксиди дуже поширені в природі, оскільки кисень є однією з найактивніших речовин. Найважливішим природним оксидом є вода – джерело життя на Землі, сировина для промисловості, джерело енергії, чинник, що визначає погоду, клімат Землі.
Амфотерність Амфотерність –здатність елементів виявляти подвійні властивості. Be Al Fe Zn Примеры: Al2O3 Fe2O3 ZnO
Ай Плиний Старший, знаменитый естествоиспытатель и историк античного мира живший в I веке, описывает такой случай. Однажды, в очень давние времена, Финикийские купцы везли по Средиземному морю груз добытой в Африке природной соды. По утру, разгребая золу, купцы обнаружили чудесный слиток, который был твёрд, как камень, горел огнём на солнце и был чист и прозрачен, как вода. Это было стекло!
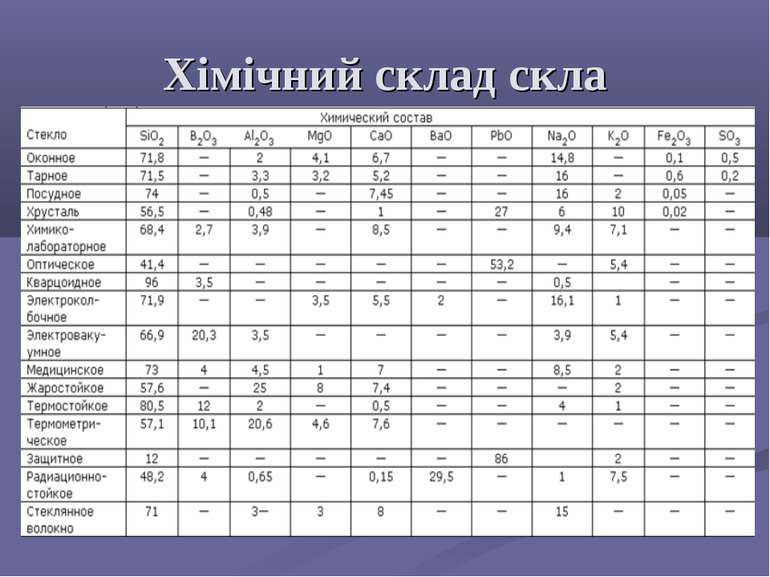
Для получения стекла составляют шихту- смесь соды Na2CO3 (иногда сульфата натрия с углем), известняка CaCO3, кварцевого песка, содержащего 97-99,8% SiO2, и различных добавок. Шихту помещают в специальные печи и сплавляют, постепенно повышая температуру до 1460-1500 градусов.
В процессе варки стекла происходят реакции: Na2CO3+SiO2=Na2SiO3+CO2 CaCO3+SiO2=CaSiO3+CO2 Na2SiO3+CaSiO3+4SiO2=Na2O+CaO+6SiO2
Стекло имеет различные добавки. Роль добавок велика, они предают стеклу особые свойства. Так, MgO повышает химическую устойчивость и механическую прочность стекла; Al2O3 увеличивает термическую и химическую стойкость, твёрдость и прочность, улучшает однородность стекла, B2O3 увеличивает термостойкость стекла и улучшает его оптические свойства. Для получения специальных оптических стёкол в шихту диоксид германия GeO2 и диоксид титана TiO2. Специальные добавки обеспечивают окраску стекла: Mn2O3 придаёт стеклу фиолетовую окраску, CoO- синюю, Cr2O3 или Fe3O4- зелёную, CuO- голубую, CdS- жёлтую.
«Первое начало и сущность всего – …» Фалес из Милета (VI в. до н.э.) Вгадай що знаходиться в перші шкатулці,?
Вода Вода – це найдивовижніша, найпоширеніша і найнеобхідніша речовина на нашій планеті. Вода – джерело життя на Землі, сировина для промисловості, джерело енергії, чинник, що визначає погоду, клімат Землі. Три чверті земної поверхні вкрито водою, що утворює океани, моря, ріки та озера.
Вуглекислий газ До складу повітря входить карбон(IV) оксид СО2 (вуглекислий газ), об’ємна частка якого в повітрі становить 0,3 %.
«…На рукомойнике моем позеленела медь, Но так играет луч на нем, что весело глядеть…» А. Ахматова А що в останій шкатулці ?
Складіть формули оксидів елементів Магния Калия Алюминия Фосфора (V) Хлора (VII ) Железа (III) Углерода (IV) Серы (VI) Випишіть в два стовбчика оксиди металів і неметалів.
Розрахуйте: 1.Массу 1литра углекислого газа (н.у.). 2.Объем 3,4г аммиака.(н.у.) 3.Сколько содержится молекул в 2 г хлороводорода.
Схожі презентації
Категорії