Презентація на тему:
"Оксид алюмінію"
Завантажити презентацію
"Оксид алюмінію"
Завантажити презентаціюПрезентація по слайдам:
Оксид алюмінію— сполука алюмінію з киснем Al2O3 — безбарвна кристалічна речовина. Синонім: глинозем
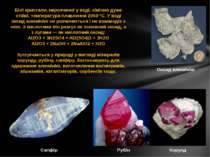
Білі кристали, нерозчинні у воді, хімічно дуже стійкі, температура плавлення 2050 °C. У воді оксид алюмінію не розчиняється і не взаємодіє з нею. З кислотами він реагує як основний оксид, а з лугами — як кислотний оксид: Al2O3 + 3H2SO4 = Al2(SO4)3 + 3H2O Al2O3 + 2NaOH = 2NaAlO2 + H2O Зустрічається у природі у вигляді мінералів корунду, рубіну, сапфіру. Застосовують для одержання алюмінію, виготовлення вогнетривів, абразивів, каталізаторів, сорбентів тощо. Оксид алюмінію Корунд Рубін Сапфір
Промислове виробництво Глинозе м, або оксид алюмінію, є основним вихідним матеріалом для виробництва алюмінію. Крім цього, він використовується й в інших сферах народного господарства
Способи одержання Відкритий у 1899 р. Байєром так званий гідрохімічний спосіб одержання оксиду алюмінію з бокситів і донині є основним у світовій алюмінієвій промисловості. Цей спосіб досить ефективний і простий, але він може застосовуватися тільки при використанні високоякісних, низькокремнистих бокситів з невеликим змістом домішок. Світові запаси таких матеріалів обмежені. Широке поширення одержав спосіб спікання — більш дорогий, але універсальніший, сировиною для якого служать боксити нижчої якості, нефеліни, алуніти, глиниста сировина, каолініти, кам'яновугільний попіл, серицити й інші алюмосилікатні породи, запаси яких практично невичерпні. Тому переробка цієї сировини способом спікання на глинозем, незважаючи навіть на знижений вміст оксиду алюмінію, цілком доцільна і вигідна, тому що крім глинозему при способі спікання утворюються побічні корисні продукти. Крім класичних способів отримання глинозему — гідрохімічного та спікання, у виробництво впроваджені й інші апаратурно-технологічні схеми виробництва глинозему: паралельно і послідовно комбіновані способи Байєр-спікання для переробки низькокремнистих і висококремнистих бокситів, спосіб спікання для переробки висококремнистих бокситів і нефелінів, відновно-лужний спосіб для переробки алунітів, гідролужні способи для переробки низькоякісних бокситів і нефелінів.
Практичний дослід одержання в лабораторії Досліджується можливість отримати оксид алюмінію способом спікання з глинистої сировини. В якості об'єкта дослідження взято глину часів'ярську особливу, яка має наступний хімічний склад: 35 % Al2O3, 4 % Na2O,K2O, 50 % SiO2, 0,5 % Fe2O3 і 1 % CaO (мас. %). В лабораторних умовах на основі глини складалися суміші для спікання з карбонатною породою (крейда). Крейда вводиться в шихту згідно з молярним співвідношенням СаО:SiO2, яке дорівнює 2,0 ± 0,03. Для отримання малорозчинного ортосилікату кальцію (2CaO-SiO2).
вихідні матеріали попередньо подрібнювались, дозувалися та ретельно змішувались. Підготовлену шихту спікали при 1200 °C з витримкою впродовж 30 хвилин у муфельній електричній печі. Ця стадія направлена на зв'язування оксиду кремнію й переводу оксиду алюмінію до розчинної у воді сполуки. Цей процес характеризуються наступною узагальненою хімічною реакцією: (Na,K)2O•Al2O3•2SiO2+ 4CaCO3 = (Na,K)2O•Al2O3 + 2(2CaO•SiO2) + 4CO2
Подрібнений спік для відділення алюмінатів лужних металів від решти спіку піддавали вилуговуванню. Вилуговування проводилося гарячим насиченим лужним розчином. Після вилуджування необхідно знекремнити розчин, тобто видалити кремнезем, який знаходиться у розчині, для підвищення якості глинозему. Знекремнення проводили у дві стадії. На першій стадії створюються умови для найповнішої кристалізації гідроалюмосилікату натрію. Друга стадія — це стадія глибокого знекремнення. Знекремнення проводилось довгим кип'ятінням розчину на електричній плитці. 3CaO•Al2O3•mSiO2•(6-2m)H2O + 3mNa2CO3 + 2mH2O= =3CaCO3 + mNa2SiO2(OH)2 + 2NaAl(OH)4 + 2(2-m)NaOH
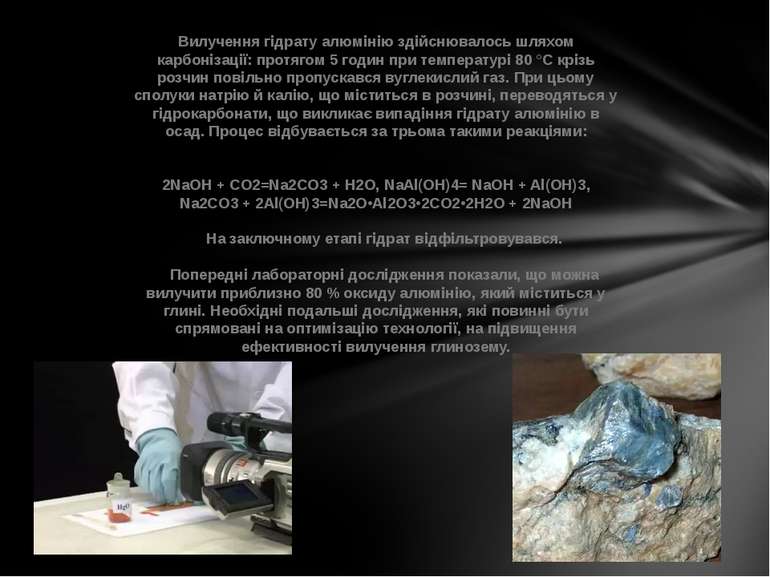
Вилучення гідрату алюмінію здійснювалось шляхом карбонізації: протягом 5 годин при температурі 80 °C крізь розчин повільно пропускався вуглекислий газ. При цьому сполуки натрію й калію, що міститься в розчині, переводяться у гідрокарбонати, що викликає випадіння гідрату алюмінію в осад. Процес відбувається за трьома такими реакціями: 2NaOH + CO2=Na2CO3 + H2O, NaAl(OH)4= NaOH + Al(OH)3, Na2CO3 + 2Al(OH)3=Na2O•Al2O3•2CO2•2H2O + 2NaOH На заключному етапі гідрат відфільтровувався. Попередні лабораторні дослідження показали, що можна вилучити приблизно 80 % оксиду алюмінію, який міститься у глині. Необхідні подальші дослідження, які повинні бути спрямовані на оптимізацію технології, на підвищення ефективності вилучення глинозему.
Схожі презентації
Категорії