Презентація на тему:
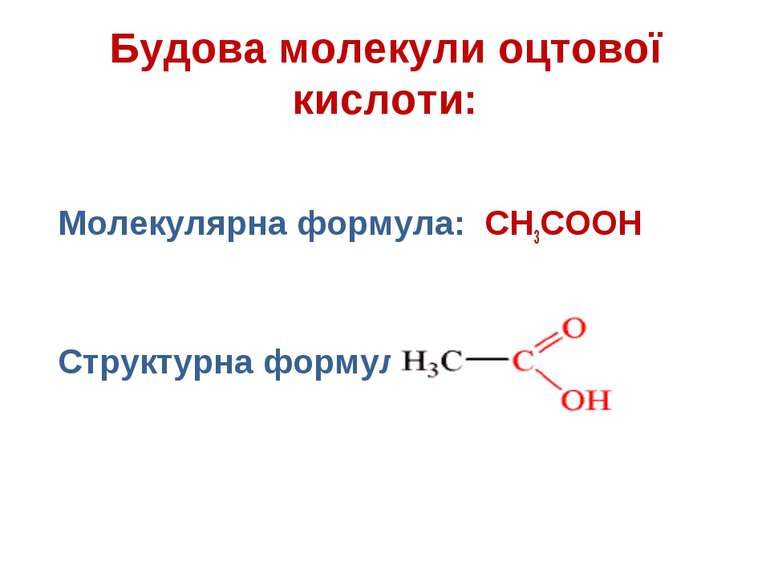
Оцтова кислота, її молекулярна та структурна формули, фізичні властивості
Завантажити презентацію
Оцтова кислота, її молекулярна та структурна формули, фізичні властивості
Завантажити презентаціюПрезентація по слайдам:
Оцтова кислота, молекулярна і структурна формули, фізичні властивості . Хімічні властивості. Застосування Презентацію виконала: вчитель хімії Черкаської загальноосвітньої школи I-III ступенів № 34 Камінська Оксана Олексіївна
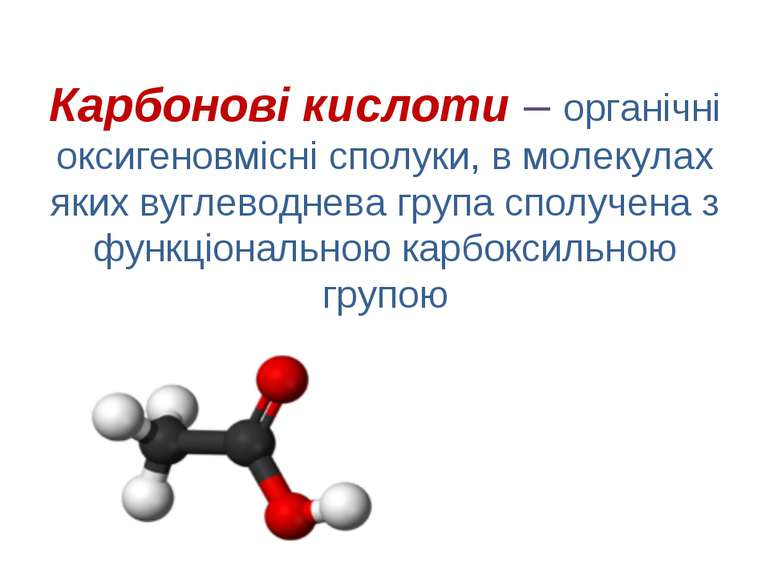
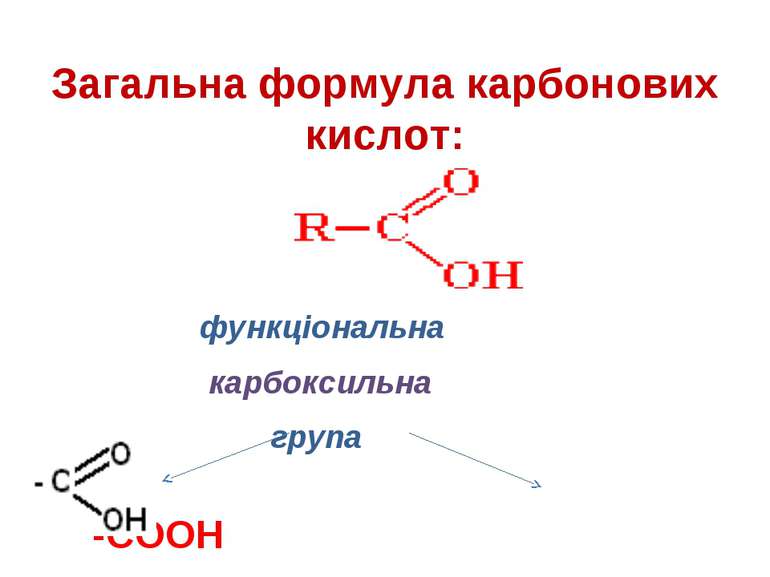
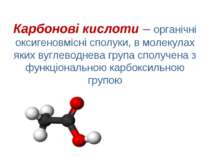
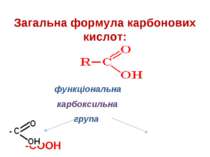
Карбонові кислоти – органічні оксигеновмісні сполуки, в молекулах яких вуглеводнева група сполучена з функціональною карбоксильною групою
Номенклатура карбонових кислот: HCOOH – мурашина кислота (метанова) CH3COOH – оцтова кислота (етанова) CH3 – (CH2)2 – COOH – масляна кислота (бутанова) Вищі карбонові кислоти: C15H33COOH – пальмітинова кислота C17H35COOH – стеаринова кислота C17H33COOH – олеїнова кислота
Фізичні властивості оцтової кислоти: Оцтова кислота – безбарвна рідина, летка, має різкий специфічний запах, змішується з водою в будь-яких пропорціях, розчин кислий на смак; за t < 170 С кристалізується (“крижана кислота “); 3-9% водний розчин – столовий оцет; 86% водний розчин - оцтова есенція
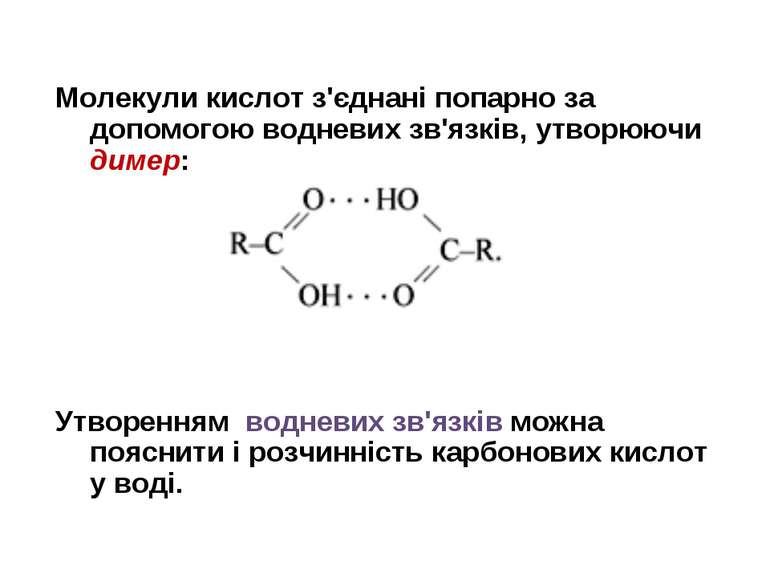
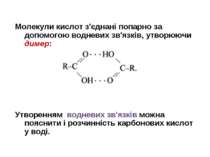
Молекули кислот з'єднані попарно за допомогою водневих зв'язків, утворюючи димер: Утворенням водневих зв'язків можна пояснити і розчинність карбонових кислот у воді.
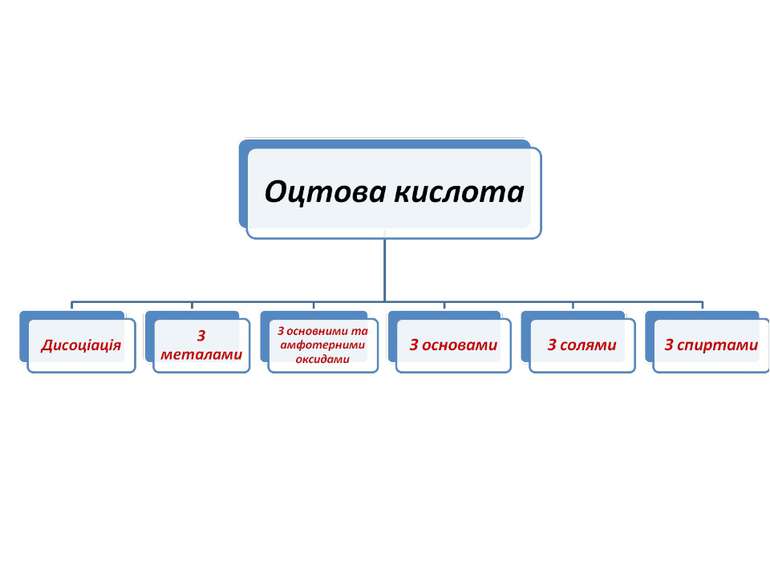
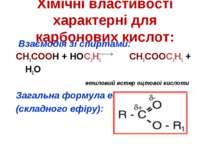
Хімічні властивості оцтової кислоти: 1) електролітична дисоціація: CH3COOH CH3COO1- + H1+ ацетат - йон 2) Взаємодія з металами: 2СН3СООН + Мg Mg(CH3COO)2 + H2 магній ацетат 3) Взаємодія з оксидами металів: 2СН3СООН + СаО Са(СН3СОО)2 + Н2О кальцій ацетат 4) Взаємодія з лугами: СН3СООН + NaOH NaCH3COO + H2O натрій ацетат 5) Взаємодія з солями, утвореними слабшими кислотами: 2СН3СООН + Na2CO3 2 NaCH3COO + CO2+ H2O
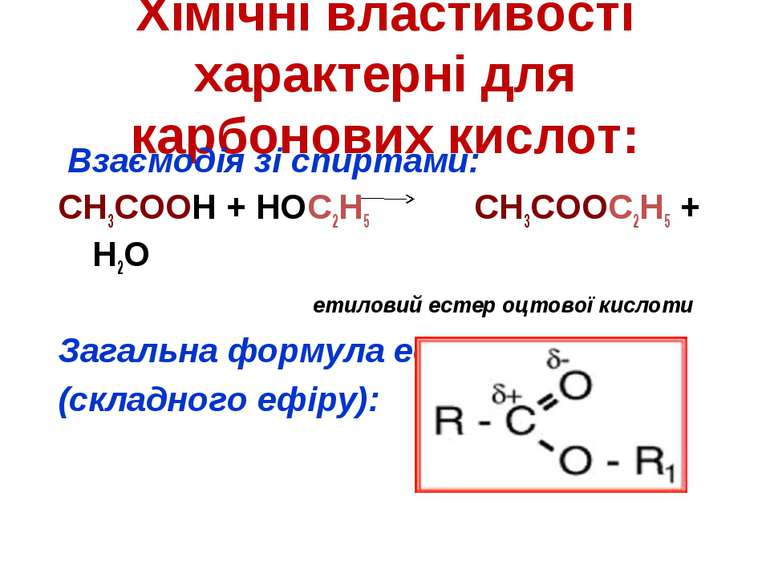
Хімічні властивості характерні для карбонових кислот: Взаємодія зі спиртами: СН3СООН + НОС2Н5 СН3СООС2Н5 + Н2О етиловий естер оцтової кислоти Загальна формула естера (складного ефіру):
Схожі презентації
Категорії