Презентація на тему:
"Кількість речовини. Молярна маса. Молярний об’єм"
Завантажити презентацію
"Кількість речовини. Молярна маса. Молярний об’єм"
Завантажити презентаціюПрезентація по слайдам:
“Кількість речовини. Молярна маса. Молярний об’єм” Урок хімії у 8 класі КЗ Верхівцевського НВК Учитель Кукса Наталія Миколаївна.
Цілі: 1.Розібрати поняття: Кількість речовини. Моль. Число Авогадро. Молярна маса. Молярний об'єм. Закон Авогадро. Відносна густина газів. 2.Навчитися робити розрахунки за формулами.
Мета : 1. Сформувати в ході уроку поняття «кількість речовини», «число Авогадро»,Молярна маса,молярний об’єм,відносна густина газів. 2. Сформувати вміння розв'язувати задачі з використанням понять «кількість речовини», «число Авогадро». 3. Продовжити розвивати експериментальні навички роботи з речовинами, вміння спостерігати, аналізувати, робити висновки, виділяти потрібну інформацію. 4. Продовжити формувати комунікативні навички, вміння працювати в групі.
Існує фізична величина, прямо пропорційна числу частинок, складових даної речовини, які входять у взяту порцію цієї речовини, яку називають кількістю речовини (n).
Кількість речовини - фізична величина, що характеризує кількість однотипних структурних одиниць, які містяться в речовині. Під структурними одиницями розуміються будь-які частки, з яких складається речовина (атоми, молекули, іони або будь-які інші частинки). Одиницею виміру кількості речовини служить моль. Потрібно знати, що моль містить стільки ж структурних частинок, скільки міститься атомів у 12г карбону Число Авогадро (NA) = 6,02 * 1023моль-1.
. Амедео Авогадро, граф Куаренья и Черрето Дата рождения: 9 августа1776 Место рождения: Турин Дата смерти: 9 июля1856(79 лет) Место смерти: Турин Научная сфера: Химия Известен как: Закон Авогадро Дата рождения: 9 августа1776 Место рождения: Турин Дата смерти: 9 июля1856(79 лет) Место смерти: Турин Научная сфера: Химия Известен как: Закон Авогадро
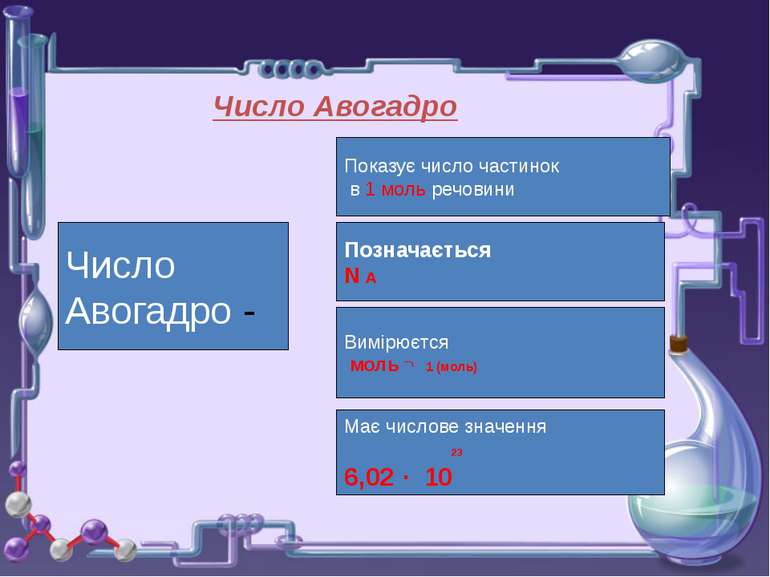
Число Авогадро Число Авогадро - Показує число частинок в 1 моль речовини Позначається N A Вимірюєтся моль ¯¹ 1 (моль) Має числове значення 23 6,02 · 10
Молярна маса -це маса одного моль речовини. М = [г / моль] (Молярна маса чисельно дорівнює молекулярній масі) звідки
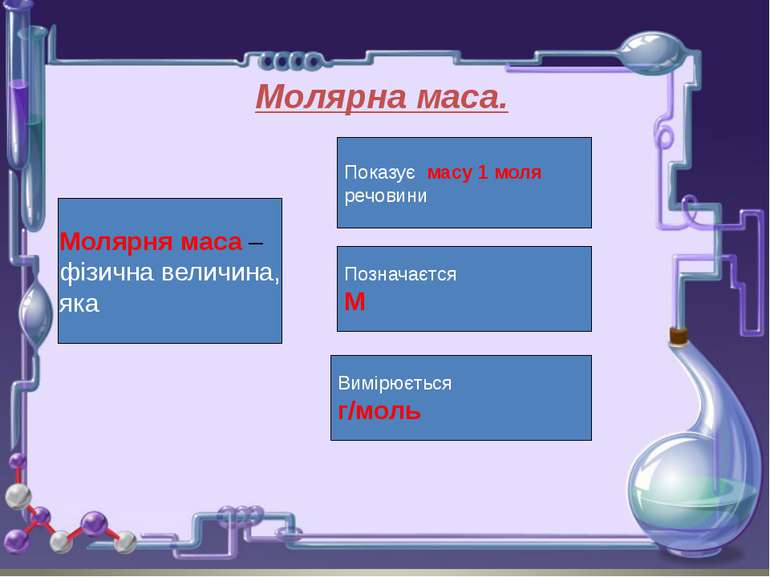
Молярна маса. Молярня маса – фізична величина, яка Показує масу 1 моля речовини Позначаєтся М Вимірюється г/моль
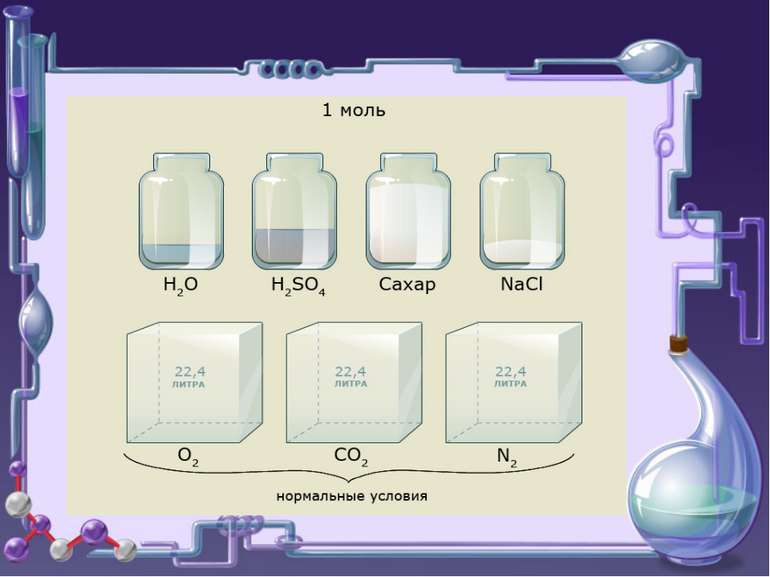
Молярний об’єм. Закон Авогадро (1811 г.) Молярний об'єм - фізична величина, яка Показує об’єм, який займає будь-який газ кількістю речовини 1 моль Поозначаєтся Vm Вимірюється л/моль В рівних об’ємах різних газів при однакових умовах міститься однакове число молекул - закон Авогадро Нормальні умови (н.у.) - температура О ° С і тиск 1атм (101,325 кПа) При н.у. Vm = 22,4 л / моль
Відносна густина газів - фізична величина, яка Показує, у скільки разів 1 моль одного газу важче або легше 1молю іншого газу Позначається D Безрозмірна величина Відносна густина газів
Відношення маси певного об’єму одного газу до маси такого ж об'єму іншого газу, взятого при тих же умовах, називається відносною густиною газів Одне і те ж число молекул різних газів при однакових умовах займає однакові об’єми. При н.у. 1 моль будь-якого газу займає об'єм 22,4 л.
о Закон об’ємних співвідношень Вимірюючи об'єми газів, в результаті реакцій Ж.Л. Гей-Люссак відкрив закон газових (об'ємних) співвідношень : Ж.Л. Гей-Люссак 1808 «При постійному тиску і температурі об’єми газів,що вступають в реакцію, відносяться один до одного як невеликі прості цілі числа»
Напрклад Химическая реакция Отношение объемов газов Н2+Cl2 2HCl 1:1:2 2CH4 C2H2+3H2 2:1:3 2C+O2 2CO 1:2 Хімічнареакція Співвідношенняоб'ємівгазів Н2+F2 2HF 1:1:2 2CH4 C2H2+3H2 2:1:3 2C+O2 2CO 1:2
Закон об'ємних співвідношень дозволив італійському вченому А. Авогадро припустити, що молекули простих газів складаються з двох однакових атомів (Н2, N2, Cl2, О2, F2 ...) Всього лише вісім елементів у природі існують у вигляді двохатомних молекул : H2; N2 ; O2. И всі галогени: F2 ; Cl2 ; Br2 ; I2 ; At2. Молекула азоту має такий вид:
Задачи (закрепление) Найдите число молекул в 2 молях водорода. Найдите массу 3 моль углекислого газа (СО2 ) Рассчитайте массу 112 л водорода (н.у.) Что тяжелее: 2 моль СО2 или 2 моль СаО ? Найдите количество вещества серной кислоты (H2SO4) массой 4,9 г Какой объем займет сернистый газ (SO2) , масса которого равна 3,2 г?
Схожі презентації
Категорії







![Молярна маса -це маса одного моль речовини. М = [г / моль] (Молярна маса чисе... Молярна маса -це маса одного моль речовини. М = [г / моль] (Молярна маса чисе...](https://svitppt.com.ua/images/60/59865/770/img7.jpg)














![Молярна маса -це маса одного моль речовини. М = [г / моль] (Молярна маса чисе... Молярна маса -це маса одного моль речовини. М = [г / моль] (Молярна маса чисе...](https://svitppt.com.ua/images/60/59865/210/img7.jpg)