Презентація на тему:
Карбонільні сполуки. Альдегіди та кетони
Завантажити презентацію
Карбонільні сполуки. Альдегіди та кетони
Завантажити презентаціюПрезентація по слайдам:
Тема: Альдегіди і кетони 1. Номенклатура та ізомерія насичених альдегідів і кетонів. 2. Способи одержання альдегідів і кетонів. 3. Фізичні властивості, будова карбонільної групи. 4. Хімічні властивості. 4.1. Реакції приєднання: а) приєднання водню (гідрування) – відновлення оксосполук. 4.2. Реакції нуклеофільного приєднання: а) реакції простого приєднання; б) реакції приєднання – відщеплення; в) приєднання вуглецевих нуклеофілів: – альдольна конденсація; – кротонова конденсація; – реакції диспропорціонування; – естерова конденсація. г) реакції заміщення; д) реакції окиснення; е) реакції полімеризації.
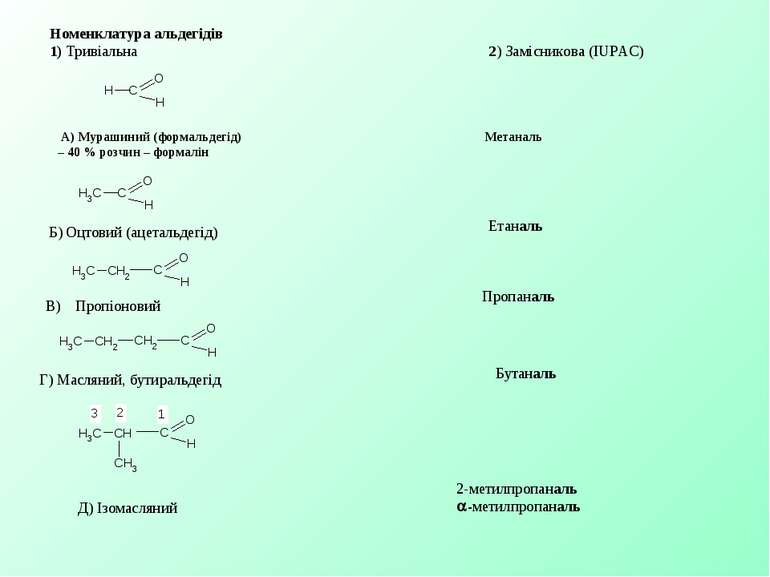
Номенклатура альдегідів 1) Тривіальна 2) Замісникова (IUPAC) А) Мурашиний (формальдегід) Метаналь – 40 % розчин – формалін В) Пропіоновий Б) Оцтовий (ацетальдегід) Етаналь Пропаналь Г) Масляний, бутиральдегід Бутаналь Д) Ізомасляний 2-метилпропаналь -метилпропаналь
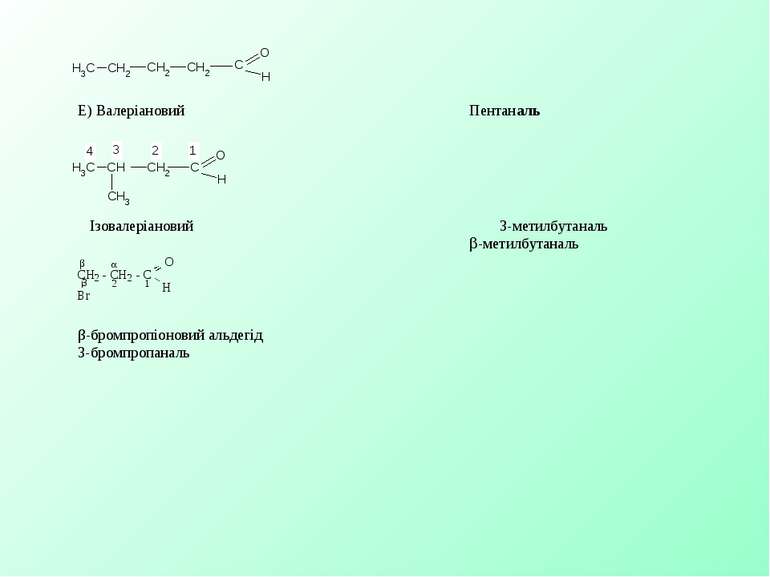
Е) Валеріановий Пентаналь Ізовалеріановий 3-метилбутаналь -метилбутаналь β-бромпропіоновий альдегід 3-бромпропаналь
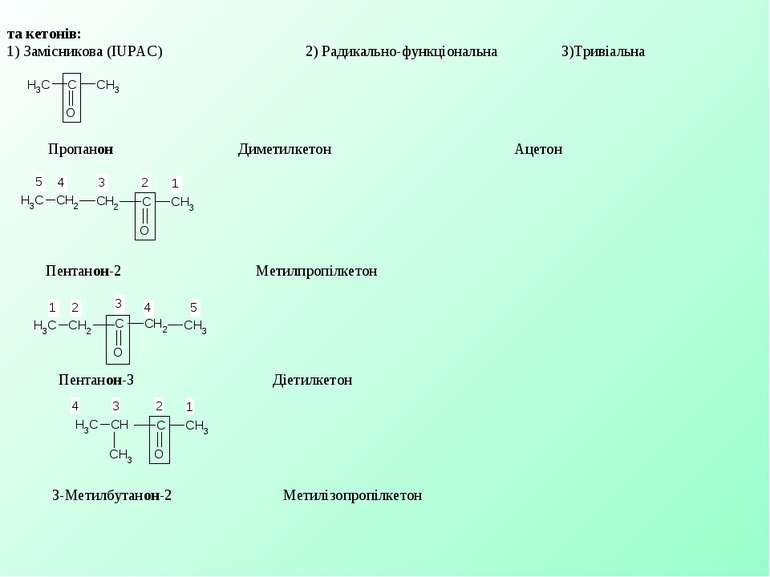
та кетонів: 1) Замісникова (IUPAC) 2) Радикально-функціональна 3)Тривіальна Пропанон Диметилкетон Ацетон Пентанон-2 Метилпропілкетон Пентанон-3 Діетилкетон 3-Метилбутанон-2 Метилізопропілкетон
Введення альдегідної групи обумовлює наркотичну дію і дезинфікуючі властивості сполук. Препарати: 40 % р-н формальдегіду – формалін Хлоральгідрат - 1,2-диокси-2,2,2-трихлоретан – заспокійливий, снодійний, анальгезуючий засіб, викликає наркотичну залежність. Гексаметилентетрамін – уротропін Дезинфікант, консервант, дубильна речовина При взаємодії з HNO3 конц. – утворює 1,3,5-тринітрогексагідро-1,3,5-триазин – або гексоген (циклоніт) – вибухова речовина.
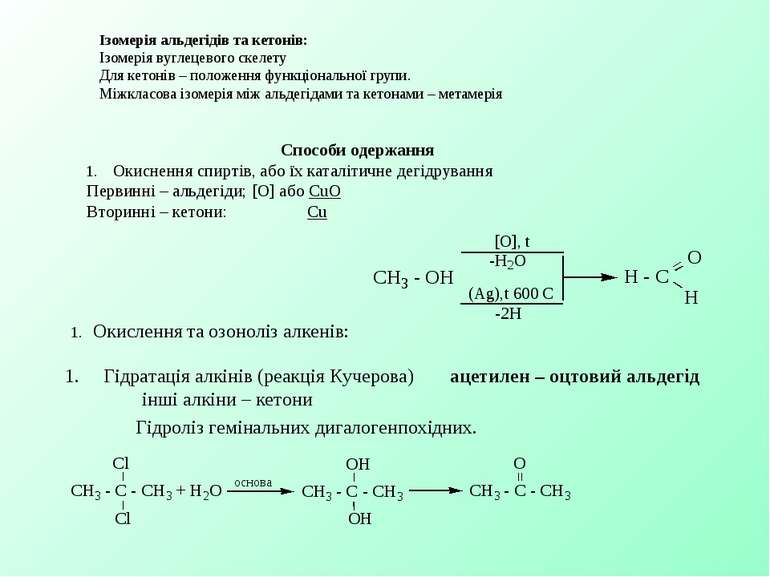
Ізомерія альдегідів та кетонів: Ізомерія вуглецевого скелету Для кетонів – положення функціональної групи. Міжкласова ізомерія між альдегідами та кетонами – метамерія Способи одержання 1. Окиснення спиртів, або їх каталітичне дегідрування Первинні – альдегіди; [O] або СuO Вторинні – кетони: Сu 1. Окислення та озоноліз алкенів: 1. Гідратація алкінів (реакція Кучерова) ацетилен – оцтовий альдегід інші алкіни – кетони Гідроліз гемінальних дигалогенпохідних.
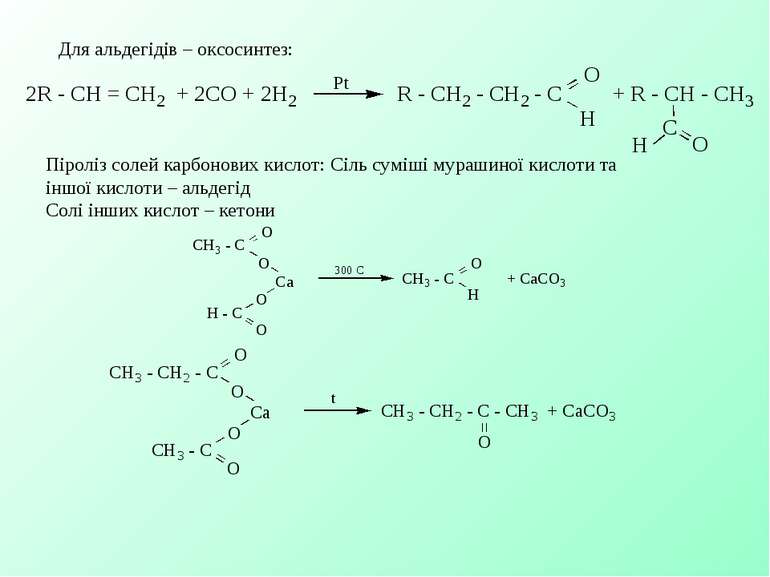
Для альдегідів – оксосинтез: Піроліз солей карбонових кислот: Сіль суміші мурашиної кислоти та іншої кислоти – альдегід Солі інших кислот – кетони
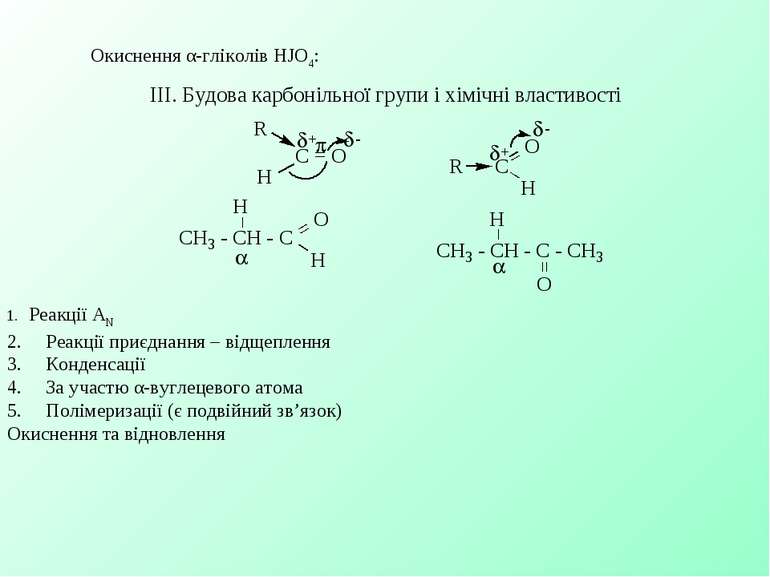
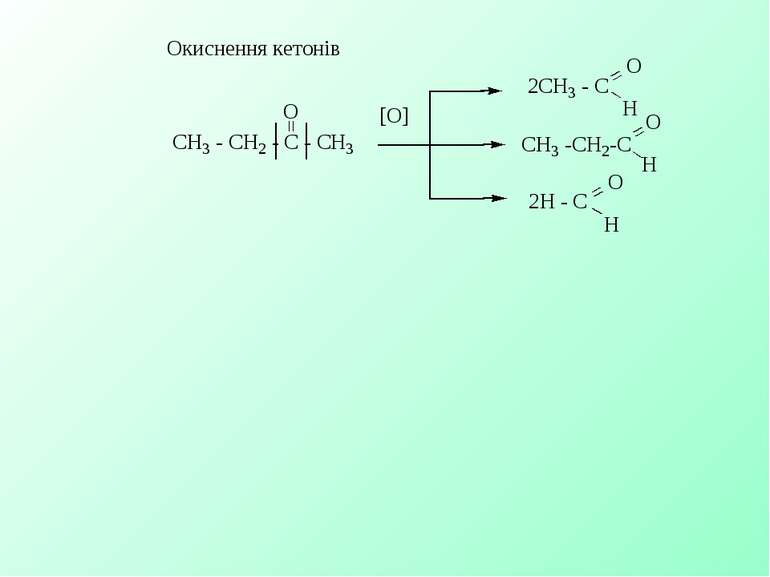
Окиснення α-гліколів HJO4: ІІІ. Будова карбонільної групи і хімічні властивості 1. Реакції АN 2. Реакції приєднання – відщеплення 3. Конденсації 4. За участю α-вуглецевого атома 5. Полімеризації (є подвійний зв’язок) Окиснення та відновлення
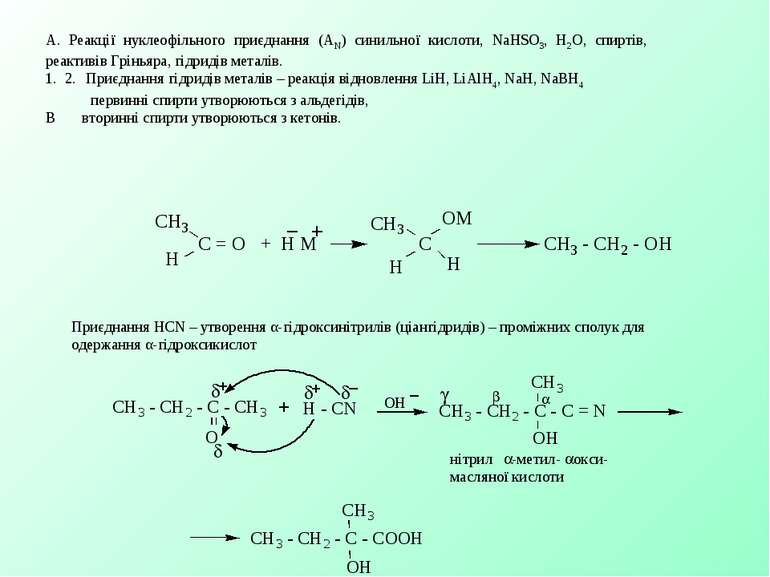
А. Реакції нуклеофільного приєднання (АN) синильної кислоти, NaHSO3, H2O, спиртів, реактивів Гріньяра, гідридів металів. 1. 2. Приєднання гідридів металів – реакція відновлення LiH, LiAlH4, NaH, NaBH4 первинні спирти утворюються з альдегідів, В вторинні спирти утворюються з кетонів. Приєднання HCN – утворення α-гідроксинітрилів (ціангідридів) – проміжних сполук для одержання α-гідроксикислот
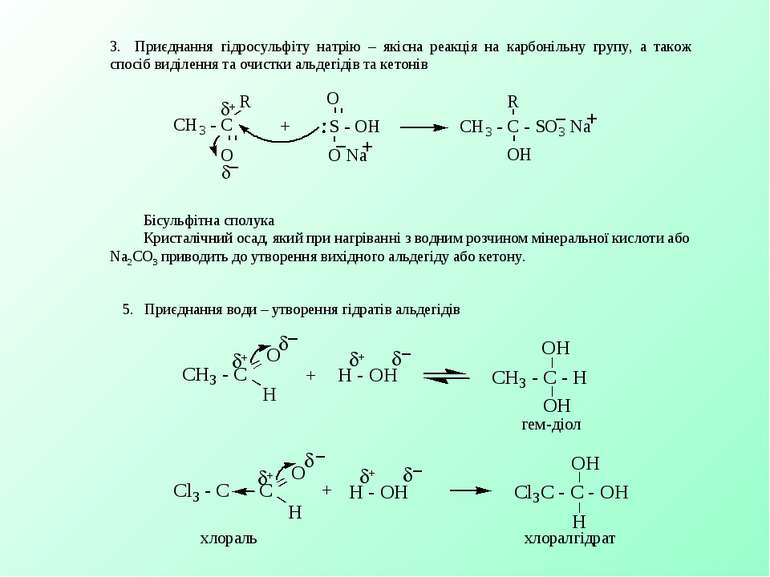
3. Приєднання гідросульфіту натрію – якісна реакція на карбонільну групу, а також спосіб виділення та очистки альдегідів та кетонів Бісульфітна сполука Кристалічний осад, який при нагріванні з водним розчином мінеральної кислоти або Na2CO3 приводить до утворення вихідного альдегіду або кетону. 5. Приєднання води – утворення гідратів альдегідів
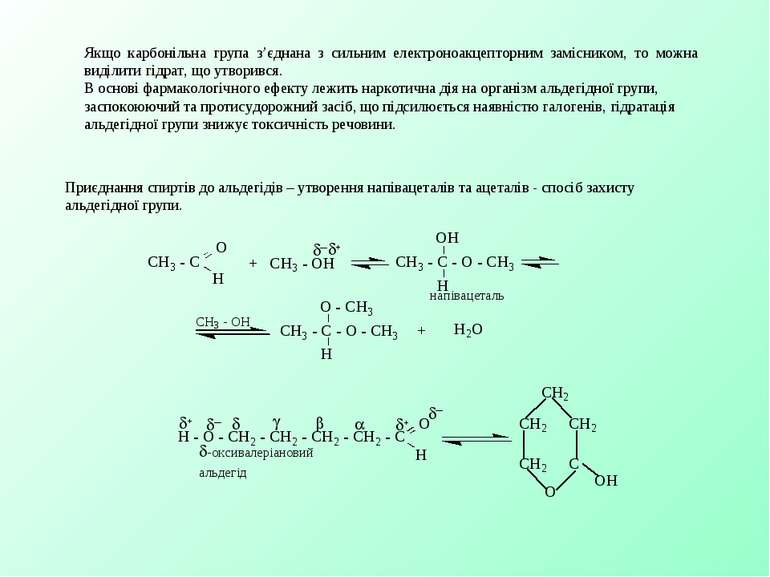
Якщо карбонільна група з’єднана з сильним електроноакцепторним замісником, то можна виділити гідрат, що утворився. В основі фармакологічного ефекту лежить наркотична дія на організм альдегідної групи, заспокоюючий та протисудорожний засіб, що підсилюється наявністю галогенів, гідратація альдегідної групи знижує токсичність речовини. Приєднання спиртів до альдегідів – утворення напівацеталів та ацеталів - спосіб захисту альдегідної групи.
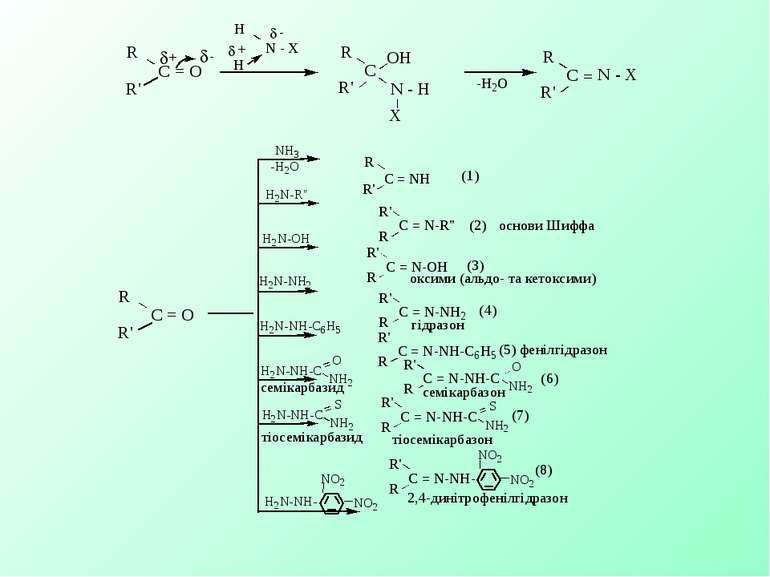
Ацеталі – стійкі в лужному середовищі, але легко гідролізуються до вільного альдегіду у вільних кислотах. Якщо альдегідна група і спиртова знаходяться в одній молекулі, то за рахунок внутрішньомолекулярної реакціївони утворюють циклічні напівацеталі – стійкі, 5- та 6-ти членні. Взаємодія з магнійорганічними сполуками (реактивом Гріньяра) – спосіб одержання одноатомних спиртів. Б. Реакції приєднання – відщеплення. Альдегіди та кетони взаємодіють з аміаком та амінами типу H2N – х (де х = Alk, OH, Ar, NH2 та ін.) з утворенням на першій стадії нестійких продуктів приєднання, які стабілізуються за рахунок відщеплення води (ІІ стадія) Ці реакції використовують для виділення альдегідів та кетонів з реакційної суміші та їх ідентифікації, оскільки утворені похідні, як правило, є кристалічними речовинами з чіткими t пл.
В результаті реакції (1) утворюються альдіміни, які полімеризуються – так Бутлеров одержав при взаємодії формальдегіду з аміаком у співвідношенні 6:4 – уротропін (гексаметилентетрамін) – дезинфікуючий засіб при запаленні сечовивідних шляхів – в кислому середовищі розщеплюється з виділення формальдегід. Іміни (реакція 2) – основи Шиффа – проміжні продукти в багатьох ферментативних процесах, біосинтезі α-амінокислот в організмі, синтезі амінів з альдегідів і кетонів з подальшим відновленням імінів Реакція (4) дозволяє окрім гідразонів одержувати ще й азини:
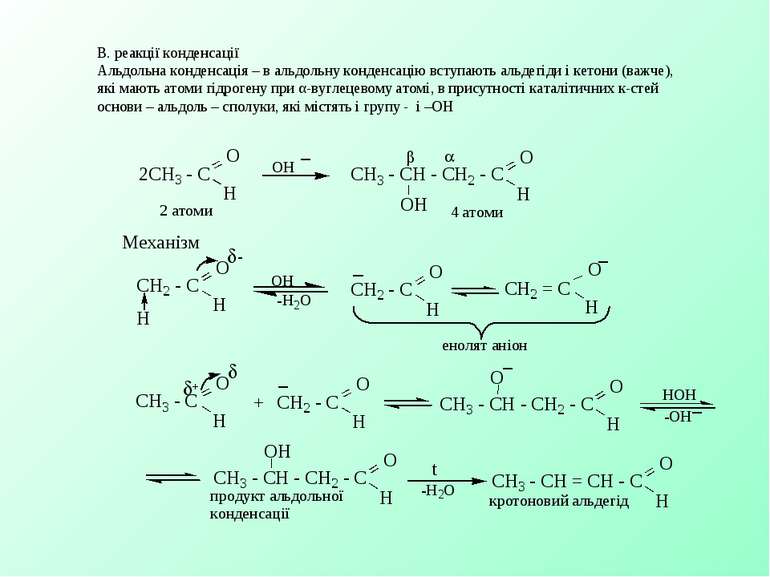
В. реакції конденсації Альдольна конденсація – в альдольну конденсацію вступають альдегіди і кетони (важче), які мають атоми гідрогену при α-вуглецевому атомі, в присутності каталітичних к-стей основи – альдоль – сполуки, які містять і групу - і –ОН
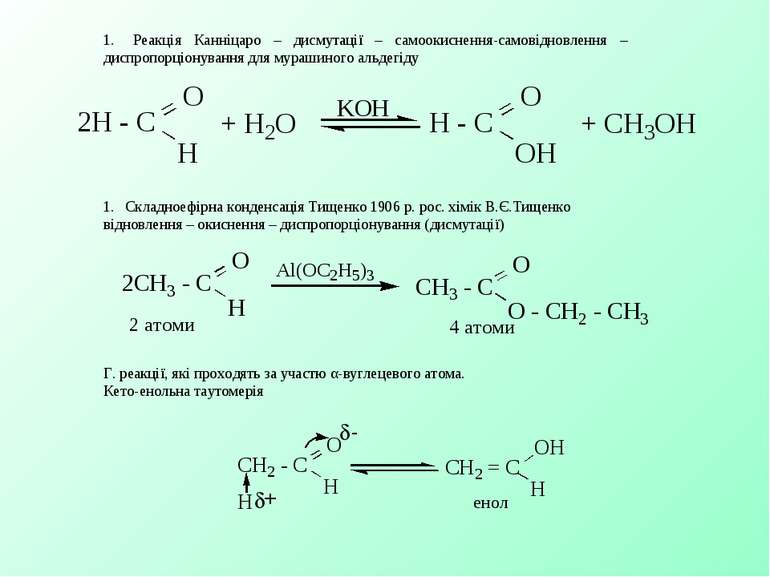
1. Реакція Канніцаро – дисмутації – самоокиснення-самовідновлення – диспропорціонування для мурашиного альдегіду 1. Складноефірна конденсація Тищенко 1906 р. рос. хімік В.Є.Тищенко відновлення – окиснення – диспропорціонування (дисмутації) Г. реакції, які проходять за участю α-вуглецевого атома. Кето-енольна таутомерія
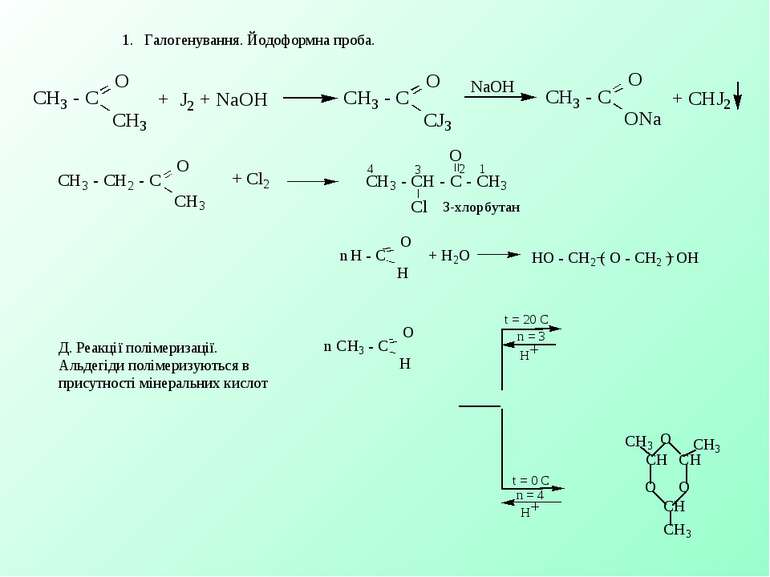
1. Галогенування. Йодоформна проба. Д. Реакції полімеризації. Альдегіди полімеризуються в присутності мінеральних кислот
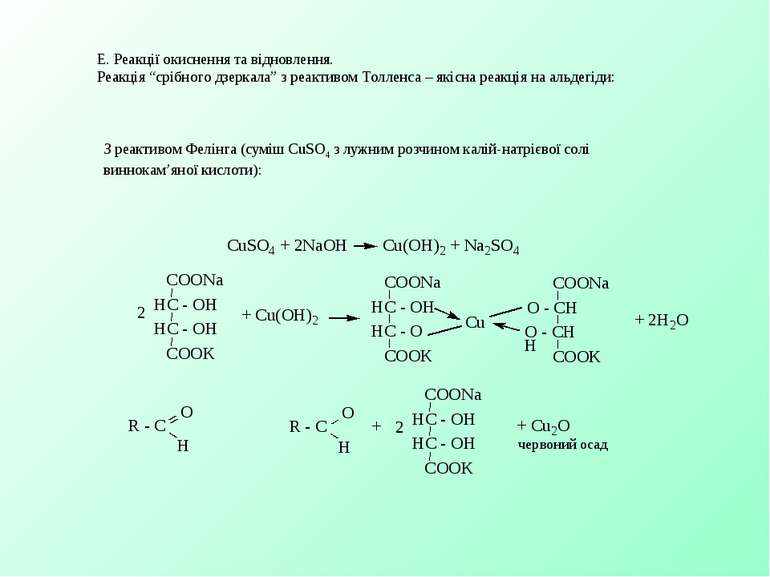
Е. Реакції окиснення та відновлення. Реакція “срібного дзеркала” з реактивом Толленса – якісна реакція на альдегіди: З реактивом Фелінга (суміш CuSO4 з лужним розчином калій-натрієвої солі виннокам’яної кислоти):
Установка для отримання води очищеної з кондуктометричним датчиком для контролю якості води очищеної
Схожі презентації
Категорії