Презентація на тему:
Етилен і ацетилен. Молекулярні і структурні формули
Завантажити презентацію
Етилен і ацетилен. Молекулярні і структурні формули
Завантажити презентаціюПрезентація по слайдам:
1. Алкани відносяться до хімічно активних речовин. 2. Наявність в молекулах алканів лише одинарних (простих) зв’язків обумовлює особливості хімічних властивостей алканів. 3. Під дією метану фіолетовий розчин калій перманганату знебарвлюється. 4. Всі алкани горять, вивільняючи значну кількість теплоти, реакції горіння – це екзотермічні реакції. 5. Реакція С2Н6 + Cl2 → С2Н5Cl + НCl називається реакцією хлорування. 6. Метан та його гомологи розкладаються при сильному нагріванні без доступу кисню на водень і сажу. 7. Алкани можуть вступати в реакції приєднання галогенів. 8. Алкани застосовуються як паливо завдяки здатності вступати в реакції термічного розкладу. 9. Якщо через розчин брому, що має бурий колір, пропустити метан, то розчин знебарвиться. 10. Гомологи метану С5 ─ С11 є основою пального для автомобільних двигунів.
Мета урока: познайомимося з алкенами та алканами. Навчитися складати їх формули, називати, описувати особливості будови. Розглянути типи ізомерії характерні для ненасичених вуглеводнів. План уроку: 1. Гомологічні ряди алкенів і алкінів. 2. Будова молекул етилену і ацетилену. 3. Порівняння будови алканів, алкенів, алкінів. 4. Види ізомерії. 5. Фізичні властивості етилену і ацетилену.
Алкени (або етиленові вуглеводні) – вуглеводні із загальною формулою СnН2n, в молекулах яких між атомами Карбону є один подвійний зв’язок. Молекулярна формула : С2Н4 Структурна формула: СН2 = СН2 Назва: етен
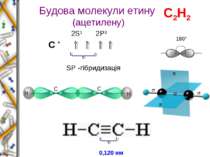
Алкіни (або ацетиленові вуглеводні) – вуглеводні із загальною формулою СnН2n-2, в молекулах яких між атомами Карбону є один потрійний зв’язок. Молекулярна формула: С2Н2 Структурна формула: СН ≡ СН Назва: етин
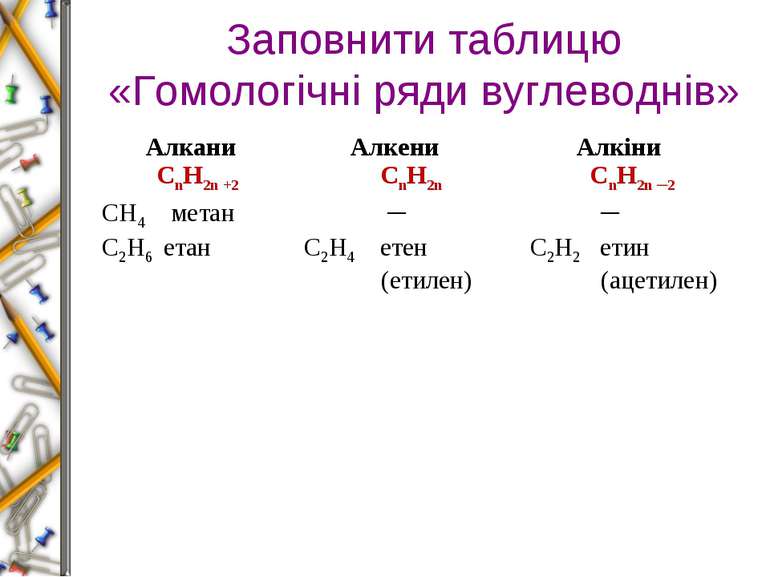
Заповнити таблицю «Гомологічні ряди вуглеводнів» Алкани СnН2n +2 Алкени СnН2n Алкіни СnН2n ─2 СН4 метан ─ ─ С2Н6 етан С2Н4 етен (етилен) С2Н2 етин (ацетилен)
Будова молекул етилену і ацетилену Ознака Етилен (алкен) Ацетилен (алкін) Особливості будови Молекулярна формула Електронна формула Структурна формула
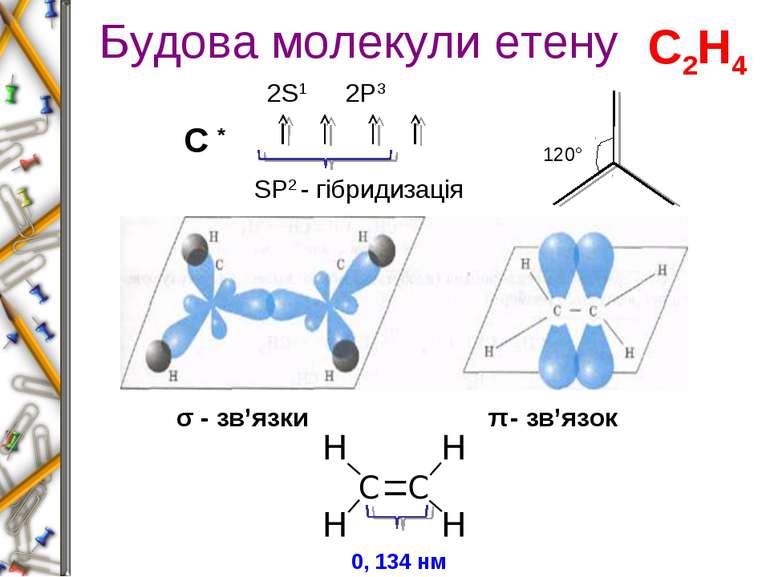
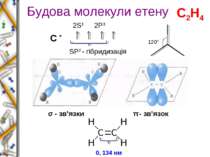
Будова молекули етену С * 2S1 2P3 SP2 - гібридизація σ - зв’язки π - зв’язок 120° 0, 134 нм С2Н4
Заповніть таблицю Алкани (етан) Алкени (етен) Алкіни (етин) Структурні формули 2.Тип гібридизації в атомах С 3. Кількість гібридних хмар 4.Кут між осями гібридних хмар 5.Зв’зки між атомами С 6.Відстань між атомами С
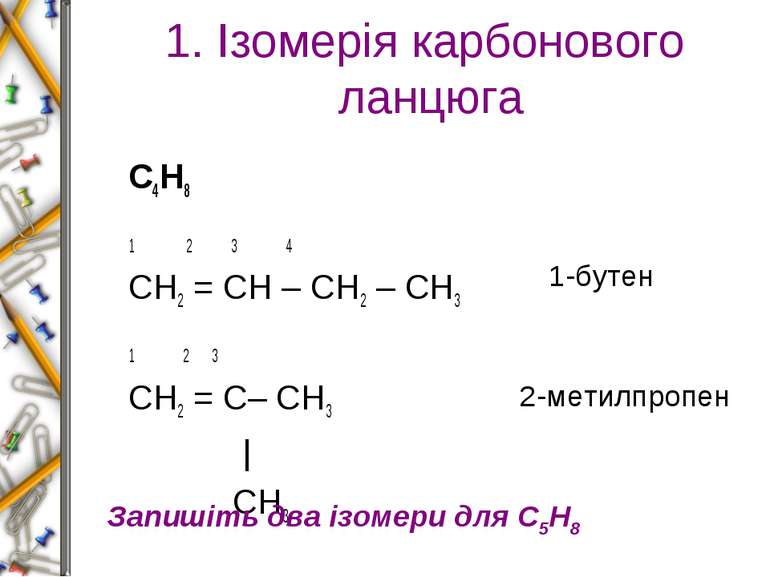
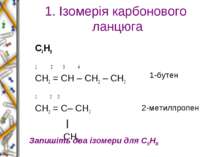
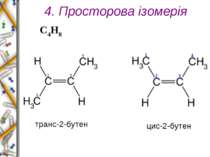
1. Ізомерія карбонового ланцюга С4Н8 1 2 3 4 СН2 = СН – СН2 – СН3 1 2 3 СН2 = С– СН3 | СН3 1-бутен 2-метилпропен Запишіть два ізомери для С5Н8
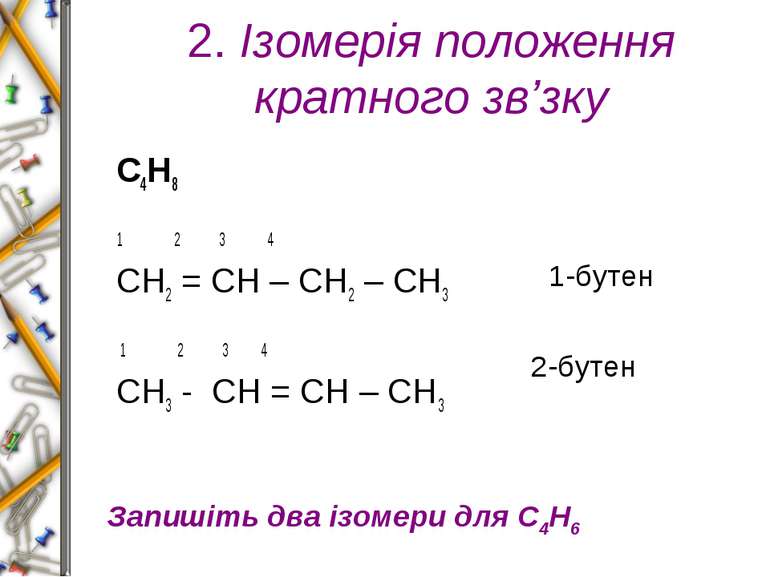
2. Ізомерія положення кратного зв’зку С4Н8 1 2 3 4 СН2 = СН – СН2 – СН3 1 2 3 4 СН3 - СН = СН – СН3 1-бутен 2-бутен Запишіть два ізомери для С4Н6
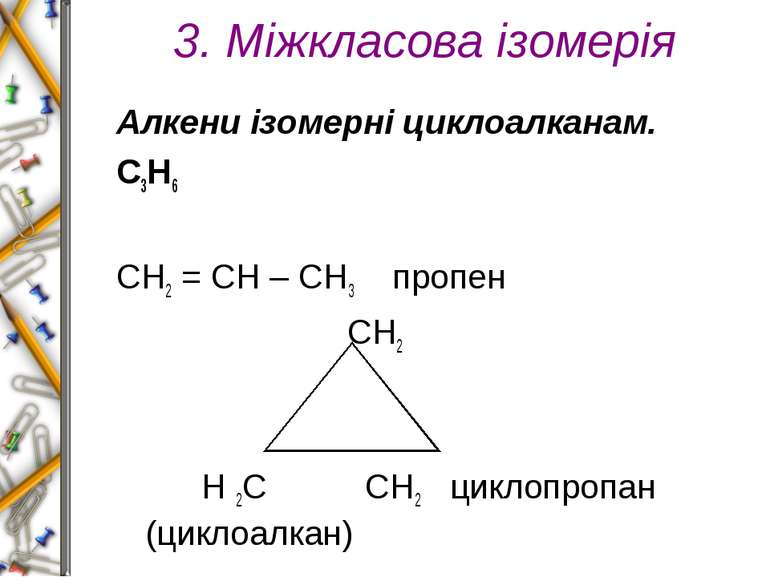
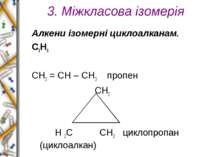
3. Міжкласова ізомерія Алкени ізомерні циклоалканам. С3Н6 СН2 = СН – СН3 пропен СН2 Н 2С СН2 циклопропан (циклоалкан)
Алкіни ізомерні алкодієнам. С4Н6 1 2 3 4 СН ≡ С – СН2 – СН3 1-бутин 1 2 3 4 СН2 = СН – СН = СН2 1,3-бутадієн (дієнові вуглеводні)
Фізичні властивості етилену і ацетилену Опрацюйте ст. 143 Н.М.Буринська, 2009 і випишіть фізичні властивості ненасичених вуглеводнів у зошит. Гази – прозорі. Безбарвні Майже без запаху (С2Н4 слабкий солодкуватий запах) Малорозчинні у воді Легші за повітря: М(С2Н4) = 28 г/моль М (С2Н2) = 26 г/моль М(повітря) = 29 г/моль
1. Складіть молекулярні формули алкену і алкіну, що містять по п’ять атомів Карбону. Напишіть структурні формули можливих ізомерів.
3. Визначте молекулярну формулу алкену, якщо його відносна молекулярна маса дорівнює 56. 4. Обчисліть масові частки Карбону і Гідрогену в молекулі ацетилену.
§ 22 (с. 142 – 144) Впр. 12, 13, ст. 149 Н.М.Буринська, 2009 Для речовини СН2=СН-СН2-СН2-СН3 написати 2 гомолога і 2 ізомера (для бажаючих)
Схожі презентації
Категорії