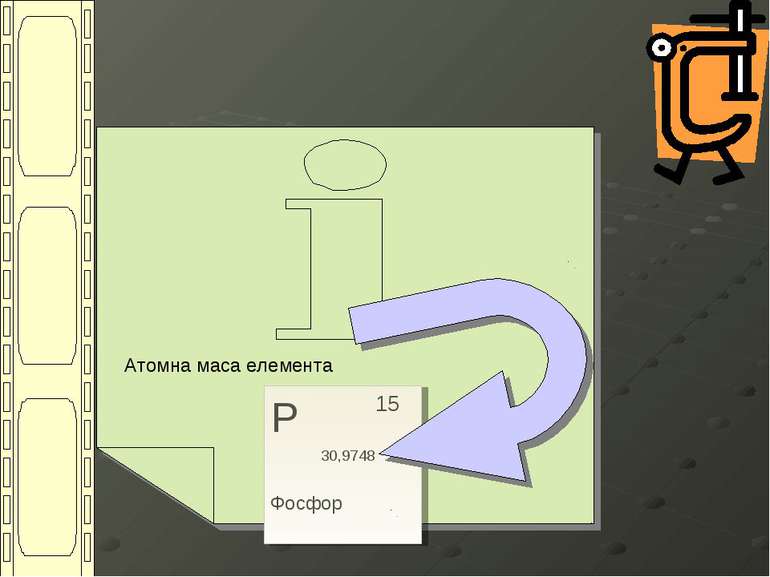
Презентація на тему:
Атомна одиниця маси
Завантажити презентацію
Атомна одиниця маси
Завантажити презентаціюПрезентація по слайдам:
Мета Розширити знання учнів про періодичну систему елементів; закріпити знан ня про хімічний елемент, хімічну символіку. Ознайомити учнів з поняттям абсолютної та відносної атомної маси, одиницею вимірювання відносної атомної маси — атомною одиницею маси (а.о.м.). Навчити визначати від носну атомну масу за періодичною системою
Кожен атом хімічного елемента має певну масу. Наприклад, маса атома найлегшого з хімічних елементів – атома Гідрогену становить 0,000 000 000 000 000 000 000 001 67 г.
Зрозуміло, що подібними числами, навіть записаними у стандартному вигляді, користуватися незручно. Тому на практиці замість абсолютних мас атомів використовують відносні атомні маси, порівнюючи маси атомів різних елементів між собою або з певною частиною маси атома іншого елемента.
Нині за одиницю порівняння вибрано 1/12 частину маси атома Карбону. Вона називається атомною одиницею маси – а.о.м. (1 а.о.м. = 1,66·10-27 кг, 1,66·10-24 г).
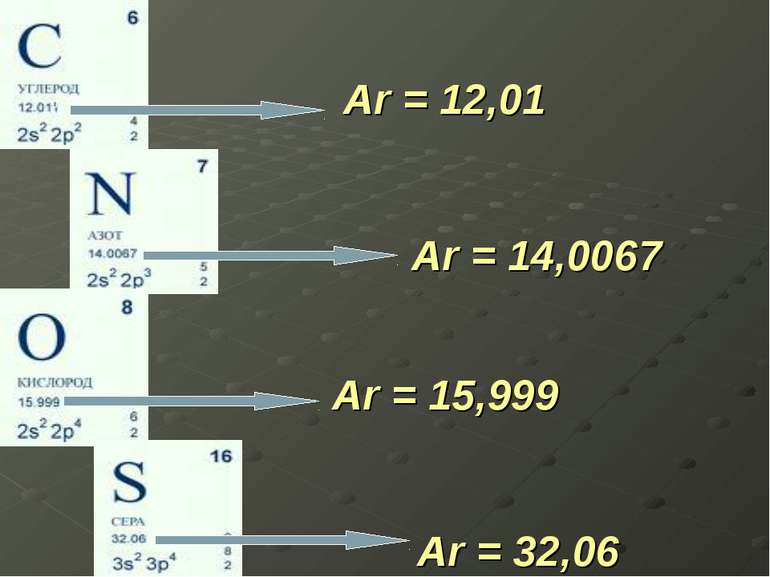
Зрозуміло, що відносна маса атома Карбону, виражена в атомних одиницях маси, дорівнює 12 а.о.м. Отже, Відносна атомна маса – це фізична величина, що визначається відношенням маси атома елемента до 1/12 маси атома Карбону.
Відносна атомна маса позначається символом Ar. А – перша літера слова “атомна”, r – перша літера латинського слова “relativus”, що означає “відносний”.
Наприклад, маса атома Флуору F дорівнює 3,15481·10 -23г. Якщо її поділити на 1/12 маси атома Карбону, тобто на атомну одиницю маси, що дорівнює 1,66057·10-24г, то дістанемо відносну атомну масу Флуору: Ar (F) =
Висновки Відносна атомна маса елемента – безрозмірна величина, що дорівнює відношенню маси атома даного елемента до 1/12 маси атома Карбону. 1/12 маси атома Карбону – це і є атомна одиниця маси, позначається а.о.м. Вона являє собою величину, що дорівнює 1,66·10-24г. Значення відносної атомної маси і маси атома, вираженої в а.о.м., чисельно збігаються. Усі відомі хімічні елементи містяться в періодичній системі хімічних елементів Д.І. Менделєєва.
Тести для самоконтролю Елемент з відносною атомною масою 56 це Барій Ферум Залізо Кобальт У порядку зростання відносних атомних мас розміщені елементи в ряду Купрум, Карбон, Сульфур, Гідроген, Бром Гідроген, Карбон, Купрум, Сульфур, Бром Гідроген, Карбон, Бром, Купрум, Сульфур Гідроген, Карбон, Сульфур, Купрум, Бром
Схожі презентації
Категорії