Презентація на тему:
Амоніак та його властивості
Завантажити презентацію
Амоніак та його властивості
Завантажити презентаціюПрезентація по слайдам:
Амоніак та його властивості Роботу виконала учениця 10-Ф класу СШ№28 м.Черкаси Коваленко Вероніка
План: Визначення; Фізичні властивості; Хімічні властивості; Гідроксид амонію; Добування аміаку; Застосування; Виробництво в Україні; Література.
Амоніак - неорганічна сполука, безбарвний газ із різким задушливим запахом, легший за повітря, добре розчинний у воді. Одержують каталітичним синтезом з азоту і водню під тиском.
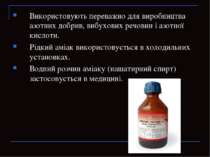
Використовують переважно для виробництва азотних добрив, вибухових речовин і азотної кислоти. Рідкий аміак використовується в холодильних установках. Водний розчин аміаку (нашатирний спирт) застосовується в медицині.
Фізичні властивості: Він майже у два рази легший від повітря. При -33,35°С і звичайному тиску аміак скраплюється в безбарвну рідину, а при −77,75 °C замерзає, перетворюючись у безбарвну кристалічну масу. Його зберігають і транспортують у рідкому стані в стальних балонах під тиском 6-7 атм.
У воді аміак розчиняється дуже добре: при 0°С і звичайному тиску в 1 об'ємі води розчиняється близько 1200 об'ємів NH3, а при 20°С — 700 об'ємів. Концентрований розчин містить 25% NH3 і має густину 0,91 г/см3. Розчин аміаку у воді називають аміачною водою або нашатирним спиртом. Звичайний медичний нашатирний спирт містить до 10%: NH3, амічна вода від 10% і більше. При нагріванні розчину аміак легко випаровується.
Хімічні властивості: Молекули аміаку утворюються за допомогою ковалентних зв'язків. Електронна і структурна формули молекули аміаку такі:
Однак зв'язки N - Н в молекулі аміаку полярні, оскільки електронна пара зміщена до атома азоту. Тому атом азоту має негативний заряд, а атом водню - позитивний. У хімічному відношенні аміак є відновником, а сам звичайно окиснюється до вільного азоту. Так, в атмосфері кисню аміак горить за реакцією: 4NH3 + 3O2 = 2N2 + 6H2O
Амоніак також легко відновлює монооксид міді до металічної міді при високій температурі за реакцією: 3CuO + 2NH3 = 3Cu + N2 + 3H2O
Гідроксид амонію: При розчиненні аміаку в воді частина його молекул взаємодіє з водневими іонами води з утворенням складного катіона амонію NH+Разом з тим відповідна кількість гідроксильних груп OH- води звільняється. Цей процес рівноважний. Його можна зобразити таким рівнянням: Звідси виходить, що в розчині аміаку в рівновазі одночасно існують молекули аміаку, води і гідроксиду амонію та іони амонію і гідроксилу.
Гідроксид амонію є дуже нестійкою речовиною і може існувати лише в розчині. При нагріванні розчину рівновага зміщується вліво, і розчин розкладається на вихідні речовини. Цей розклад частково відбувається і при звичайній температурі, тому розчини аміаку завжди мають специфічний запах. При тривалому кип'ятінні розчину можна повністю видалити аміак. Цим інколи користуються в лабораторіях для одержання невеликих кількостей аміаку. Розчин гідроксиду амонію забарвлює лакмус у синій колір. З кислотами розчин гідроксиду амонію утворює солі, наприклад:
Добування аміаку: В лабораторних умовах аміак добувають звичайно нагріванням суміші хлориду амонію NH4Cl з гашеним вапном Ca(OH)2. Процес утворення аміаку при цьому відбувається в дві стадії: спочатку виникає гідроксид амонію, а потім він розкладається з виділенням аміаку: 2NH4Cl + Ca(OH)2 = 2NH4OH + CaCl2 NH4OH = NH3↑ + H2O
Інколи аміак добувають нагріванням до кипіння концентрованого розчину аміаку (гідроксиду амонію). Ця реакція відбувається лише при дуже високих тисках (кілька сот атмосфер), високій температурі і наявності каталізатора. На сучасних заводах синтез проводять у більшості випадків при тисках 250–350 атм, а інколи навіть при 700–1000 атм. Чим більший тиск, тим більше рівновага реакції зміщується в бік утворення NH3, тобто в бік збільшення виходу аміаку. Але процес при дуже високих тисках дуже дорогий і економічно невигідний. Температуру підтримують близько 400–450°С. Нижче 400°С реакція відбувається дуже повільно, а вище 450–500°С аміак помітно розкладається на азот і водень. Каталізатором служить губчасте залізо з домішками оксидів калію, алюмінію й інших речовин.
При цьому слід ще раз відмітити, що не вся азотоводнева суміш перетворюється в аміак навіть при найвищих тисках. Частина її залишається непрореагованою. Тому одержуваний аміак відділяють від непрореагованої суміші скрапленням його під тиском, а до решти суміші додають нові порції азото-водневої суміші і знову направляють на синтез.
Значні кількості аміаку одержують як побічний продукт при коксуванні кам'яного вугілля, в якому міститься від 1 до 2,5% азоту. При коксуванні вугілля більша частина цього азоту виділяється у вигляді аміаку. Його видаляють, з коксового газу пропусканням газу через воду. Аміачну воду нейтралізують сульфатною кислотою і одержують сульфат амонію. До кінця XIX століття цей спосіб був єдиним промисловим способом добування аміаку. Лише в 20-х роках, XX століття, коли поширився синтетичний спосіб, він втратив своє значення.
Застосування: Амоніак - один з найважливіших продуктів сучасної хімічної промисловості. Головною галуззю його застосування є виробництво нітратної кислоти і азотних добрив. Крім того, аміак використовують для виробництва багатьох інших хімічних продуктів. Зріджений аміак і водний розчин аміаку застосовують безпосередньо як азотне добриво.
Виробництво в Україні: Дмитро Фірташ та пов'язані з ним структури зосередили у своїх руках виробництво 100% селітри в Україні, 80% карбаміду та 75% аміаку.
Література: Українська радянська енциклопедія. В 12-ти томах / За ред. М. Бажана. - 2-ге вид. - К.: Гол. редакція УРЕ, 1974-1985. Ф. А. Деркач «Хімія» Л. 1968.
Схожі презентації
Категорії