Презентація на тему:
історія вивчення атома
Завантажити презентацію
історія вивчення атома
Завантажити презентаціюПрезентація по слайдам:
План уроку Історія вивчення атома Схема дослідів Резерфорда Результати дослідів Резерфорда Планетарна модель атома Історична довідка про Е.Резерфорда Історична довідка про Дж.Томсона
Історія вивчення атома Усі тіла навколишньої живої і неживої природи складаються з дрібних частинок – атомів. Першими, хто висловив припущення про це, вважаються давньогрецькі філософи Левкіпп і Демокріт. Саме вони назвали атомом дрібну неподільну частинку, що утворює речовину. Вони вважали, що речовини утворюються в результаті зіткнення атомів і появи зв'язків між ними.
Наприкінці XIX ст. науковці з'ясували деякі факти, які свідчили на користь того, що атом є складною електричною системою.
Електризація тіл тертям, фотоефект, проходження струму через рідини й гази засвідчило, що до складу атомів входять заряджені частинки.
Наявність усередині атома заряджених частинок була підтверджена здатністю атомів випромінювати й поглинати електромагнітні хвилі характерної для кожного елемента довжини. Було відкрито і досліджено катодне випромінювання, яке являло собою потік негативно заряджених частинок – електронів.
1897 рік. Дж.Томсон експериментально відкрив електрон як складову частинку атома і носія найменшого електричного заряду. Він припустив, що атом – це позитивно заряджена куля, всередині якої містяться негативно заряджені електрони.
1911 рік. Дослід Е.Резерфорда. Цілі досліду: дослідити будову атома. Ідея досліду: розсіювання ⍶-частинок під час проходження тонких шарів речовини
Схема дослідів Резерфорда “…відтепер мені відомо, як виглядає атом” 1 – пучок ⍶-частинок 2 – золота чи платинова пластинка 3 – екран 4 – оптичний пристрій
Результати дослідів Резерфорда більшість ⍶-частинок не відхиляються від початкового напрямку руху. незначна кількість ⍶-частинок відхилилась від початкового напрямку руху на невеликі кути. незначна кількість ⍶-частинок практично відкинута назад.
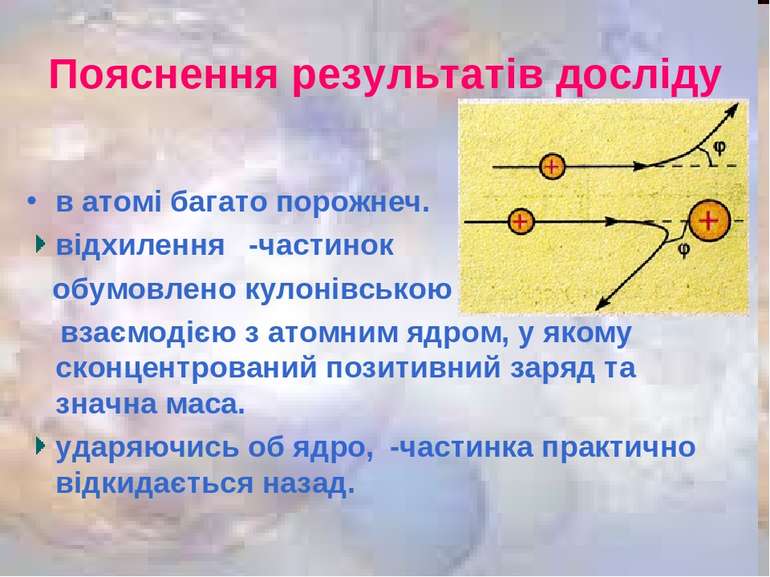
Пояснення результатів досліду в атомі багато порожнеч. відхилення ⍶-частинок обумовлено кулонівською взаємодією з атомним ядром, у якому сконцентрований позитивний заряд та значна маса. ударяючись об ядро,⍶-частинка практично відкидається назад.
Планетарна модель атома атом загалом нейтральний у центрі атома перебуває позитивне ядро, у якому сконцентрована практично вся маса атома. Ядро складається з протонів і нейтронів (нуклонів). розміри ядра набагато менші від розмірів атома. на значній відстані від ядра обертаються електрони
Схожі презентації
Категорії