Презентація на тему:
Лужні елементи та лужні метали. Версія 1
Завантажити презентацію
Лужні елементи та лужні метали. Версія 1
Завантажити презентаціюПрезентація по слайдам:
План уроку 1.Загальні відомості про лужні метали 2. Фізичні властивості лужних металів 3. Біологічна роль лужних елементів у житті людини 4. Хімічні властивості лужних металів
Мета уроку Пригадати будову атомів лужних металів Ознайомитись з фізичними та хімічними властивостями лужних металів, їх оксидів Пояснити біологічну роль лужних металів
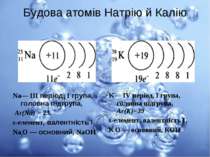
23 +11 0 2 8 1 Краткая электронная запись: Будова електронної оболонки Натрію Ступінь окиснення атомів у сполуках = +1.
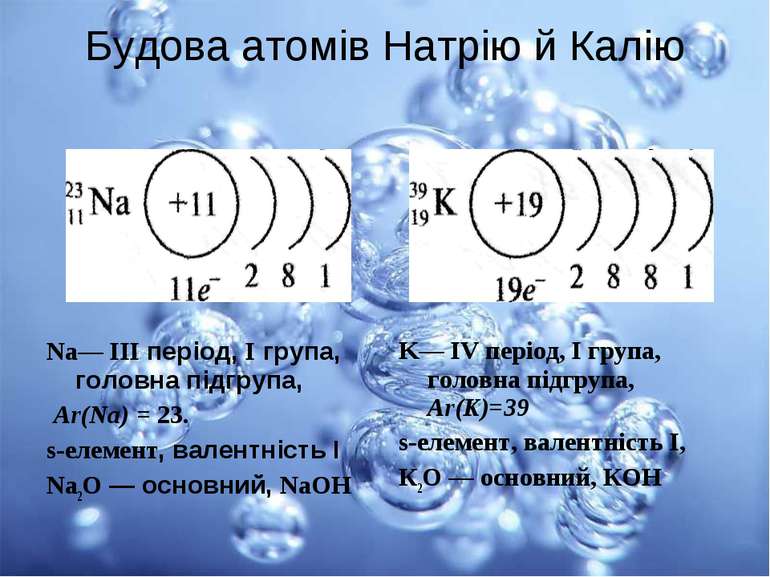
Будова атомів Натрію й Калію K— IV період, І група, головна підгрупа, Аr(K)=39 s-елемент, валентність І, К2О — основний, КОН Na— III період, I група, головна підгрупа, Аr(Na) = 23. s-елемент, валентність І Na2О — основний, NaОН
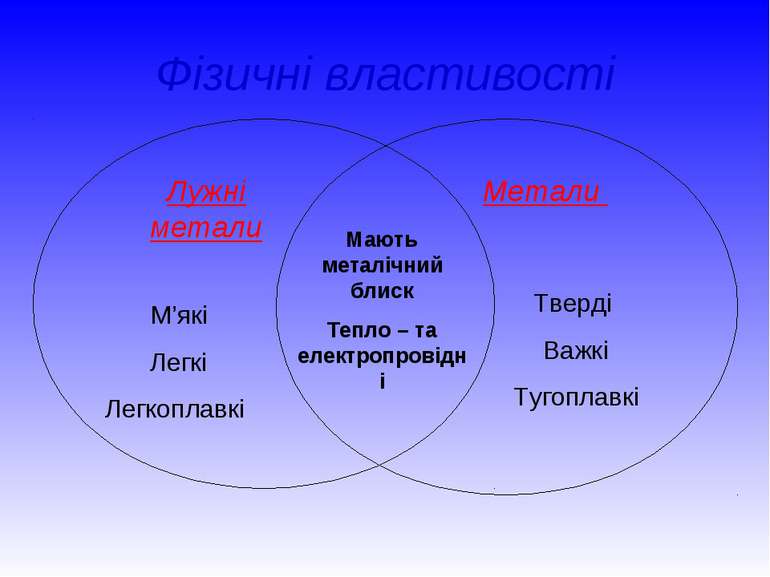
Фізичні властивості Лужні метали Метали М’які Легкі Легкоплавкі Тверді Важкі Тугоплавкі Мають металічний блиск Тепло – та електропровідні
Природні сполуки Натрію Кам’яна сіль або галіт - NaCl Глауберова сіль або мірабіліт - Na2SO4 ∙ 10 H2O Польовий шпат -Na2O ∙ Al2O3 ∙ 6SiO2
Кількісний вміст лужних металів в організмі людини Де накопичуються Натрій, Калій, Рубідій, Цезій та Францій Застосування сполук лужних металів в медицині
Макроелементи: Натрій – 0,08 % Калый – 0,23 % Мікроелементи: Літій - 10-4 % Рубідій - 10-5% Цезій - 10-4 %
У організмі людини лужні метали знаходяться у вигляді катіона Е+. Натрій і Літій накопичуються в позаклітинній рідині; Калій, Рубідій і Цезій — у внутрішньоклітинній речовині.
Натрій і Калій — антагоністи. Антагонізм (хім.) — явище зменшення або зниження активності якої-небудь речовини в присутності іншої.
Натрій Na Із загального вмісту в організмі людини 44 % Натрію міститься в позаклітинній рідині, 9 % — у внутрішньоклітинній.
Рубідій та Цезій Рубідій є аналогом Калію; також накопичується у внутрішньоклітинній рідині й може в різних процесах заміщати еквівалентну кількість Калію. Радіоактивні ізотопи 137Сs і 87Rb використовують у радіотерапії злоякісних пухлин
Францій Це радіоактивний хімічний елемент, одержаний штучним шляхом. Є дані, що Францій здатний вибірково накопичуватися в пухлинах на найбільш ранніх стадіях їх розвитку.
Лужні метали подібні за своїм впливом на біологічні процеси Натрій і Калій — життєво необхідні елементи, постійно містять ся в організмі, беруть участь в обміні речовин. Літій, Рубідій, Цезій — також постійно є в організмі, проте їх фізіологічна й біохімічна роль мало з'ясована, їх можна віднести до домішкових мікроелементів. .
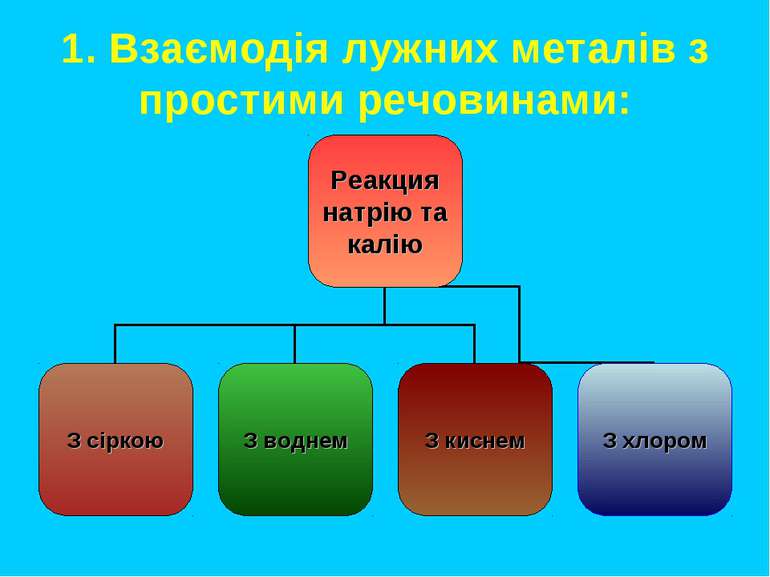
1. Здійснити перетворення: (робота в парах) Варіант 1. K→KOH→K2SO4→ KCl→ K2CO3 →КCl →K Варіант 2. Na→NaOH→Na→Na2O→Na2СO3→NaBr → →Na
Варіант 1. 2K + 2H2O = 2KOH + H2 2KOH + H2SO4 = K2SO4 + 2H2O або 2KOH + SO3 = K2SO4+ H2O K2SO4 + BaCl2 = KCl + BaSO4↓ 2KCl + Ag2CO3 = K2CO3 + 2AgCl↓ K2CO3 + 2HCl = 2KCl + CO2 + H2O 2KCl→2K + Cl2 (електроліз) Варіант 2. 2Na + 2H2O = 2NaOH + H2 4NaOH = 4Na+2H2O+O2 4Na + O2 = 2Na2O Na2O + CO2 = Na2CO3 Na2CO3 + 2HBr = 2NaBr + CO2 + H2O 2NaBr → 2Na + Br2 (електроліз)
Перевіримо свої знання На аркуші для міні - тестів напишіть своє прізвище. Виконайте завдання. На виконання теста відводиться 5 хвилин. Бажаю успіху!
1. Який рядок складається тільки з лужних металів: А. Li, Na, Ba, K. Б. Li, Na, Ca, K. В. K, Fe, Cs, Na. Г. Na, Li, Rb, Cs 2. Виберіть правильне твердження стосовно будови атомів лужних металів: А. На зовнішньому електронному шарі знаходяться два електрони. Б. Порядковий номер елемента дорівнює заряду ядра його атома. В. …ns2 - електронна формула зовнішнього електронного шару атомів лужних металів. Г. В атомів лужних металів найменший радіус серед усіх елементів відповідних періодів.
3. Виберіть правильне твердження стосовно положення лужних металів в Періодичній системі хімічних елементів А. Лужні метали – це головна підгрупа в періодичній системі хімічних елементів. Б. Лужні метали знаходяться в ІІІ групі. В. Лужні метали знаходяться в І періоді. Г. Лужні метали знаходяться в побічній підгрупі І групи. 4. Виберіть правильне твердження стосовно загальної характеристики лужних металів. А. Лужні метали з усіх металів найактивніші. Б. Значення електронегативностей лужних металів найбільші. В. Літій плавиться при t ≈ 20º С. Г. У ряді Бекетова (ряд активності металів) лужні метали стоять у кінці
5. Серед тверджень стосовно хімічних властивостей лужних металів укажіть усі правильні. А. Лужні метали реагують з неметалами, утворюючі солі. Б. Лужні метали реагують з водою, утворюючі луги. В. Лужні метали реагують з киснем, утворюючі оксиди. Г. Лужні метали реагують з воднем, утворюючі гідроксиди. 6. За вмістом в організмі людини до мікроелементів належать: А. Натрій Б.Літій В.Калій Г.Рубідій
7.У позаклітинній рідині накопичуються: А.Натрій Б.Калій В.Літій Г.Францій 8. Під час згорання натрію полум’я забарвлюється в колір: А. червоний Б. жовтий В. фіолетовий Г. зелений
Ключ до тестування: 1. Г 2. Б 3. А 4. А. 5. А, Б, В. 6. А, В 7. А 8. Б За кожну правильну відповідь зарахуйте 1,5 бали
Домашнє завдання: Опрацювати § 20 Виконати завдання: № 190 (на 9 балів) №192,197 (на 12 балів) Дякую за урок! До нових зустрічей!
Схожі презентації
Категорії