Презентація на тему:
Як зробити урок хімії цікавим
Завантажити презентацію
Як зробити урок хімії цікавим
Завантажити презентаціюПрезентація по слайдам:
Як зробити урок хімії цікавим та ефективним Уміє вчити той, хто вчить цікаво Альберт Ейнштейн
Центр інноваційної освіти Потоваришуйте з учнями Ніколи не переказуйте того, що можна прочитати в підручнику Використовуйте різноманітні методики Максимально поєднуйте теорію з практикою Давайте учням цікаві домашні завдання Намагайтесь проводити уроки надворі Проводьте кожен урок так, ніби проводите його востаннє
1. Які органічні сполуки називають насиченими вуглеводнями (алканами)? 2. Які назви алканів вам ще відомі? 3. Наведіть загальну формулу алканів. 4. Яка формула алкану, що містить 6 атомів Карбону? ….. 130 атомів Карбону? ……. Раз! Два! Три! Продано! Вам пропонується назвати по одній властивості найпростішої органічної сполуки – метану. Учні відповідають ланцюжком, отримуючи жетони по 1 балу за кожну вірну відповідь. Раз! Два! Три! Продано! Аукціон хімічних знань Насичені вуглеводні
Інтерактивні методи проводять дослідження, спостерігають, порівнюють; об’єднуються в пари, розподіляють обов’язки, складають план дій; систематизують, роблять узагальнюючі висновки Організація дослідницької діяльності
Інтерактивні методи Алгоритм діяльності учнів Позиція: “я вважаю, що…” Обґрунтування “тому, що ….” Приклад “наприклад…” Висновок “отже… таким чином…”
Поєднайте : назву органічної сполуки і її хімічну формулу А: метан 1: С3Н8 Б: етан 2: СН4 В: пропан 3: С4Н10 Г: бутан 4: С2Н6
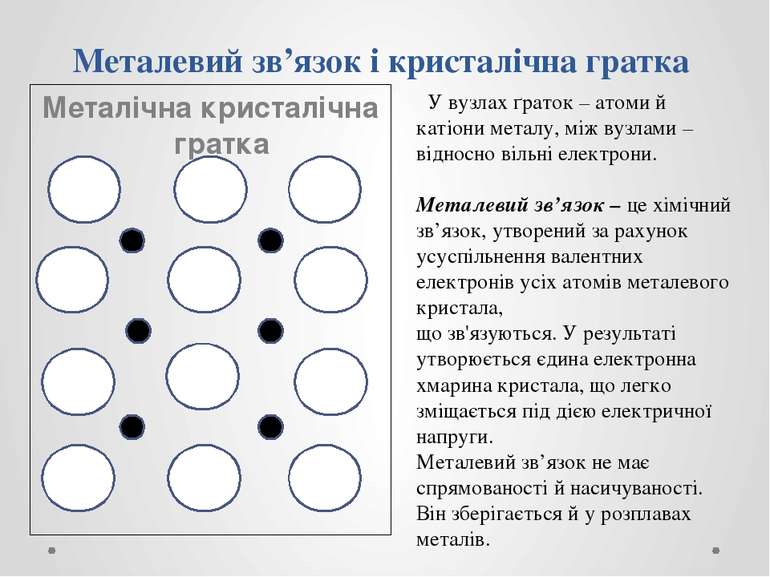
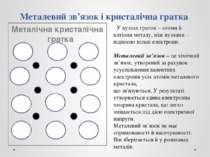
Металевий зв’язок і кристалічна гратка Металічна кристалічна гратка + + + + У вузлах ґраток – атоми й катіони металу, між вузлами – відносно вільні електрони. Металевий зв’язок – це хімічний зв’язок, утворений за рахунок усуспільнення валентних електронів усіх атомів металевого кристала, що зв'язуються. У результаті утворюється єдина електронна хмарина кристала, що легко зміщається під дією електричної напруги. Металевий зв’язок не має спрямованості й насичуваності. Він зберігається й у розплавах металів. + +
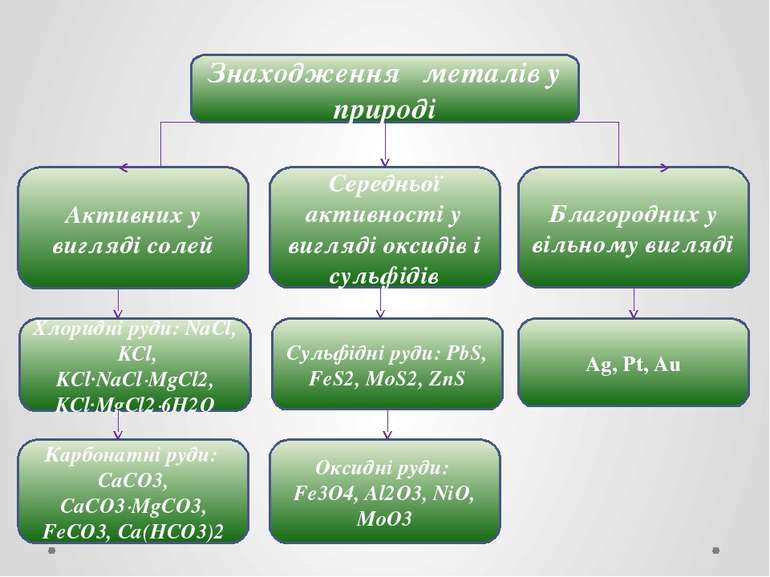
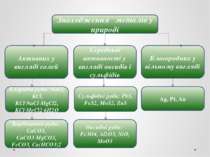
Благородних у вільному вигляді Ag, Pt, Au Середньої активності у вигляді оксидів і сульфідів Активних у вигляді солей Сульфідні руди: PbS, FeS2, MoS2, ZnS Хлоридні руди: NaCl, KCl, KCl∙NaCl∙MgCl2, KCl∙MgCl2∙6H2O Оксидні руди: Fe3O4, Al2O3, NiO, MoO3 Карбонатні руди: CaCO3, CaCO3∙MgCO3, FeCO3, Ca(HCO3)2 Знаходження металів у природі
Загальні способи одержання металів 1. Найактивніші (K, Ca, Mg, Na) відновлюють електролізом. Електроліз – окисно-відновна реакція під дією постійного електричного струму. 2NaCl = 2Na + Cl₂ На катоді: Na⁺ + e⁻ = Na° - відновлення катіонів. На аноді: Cl⁻ - e⁻ = Cl° - окиснення аніонів.
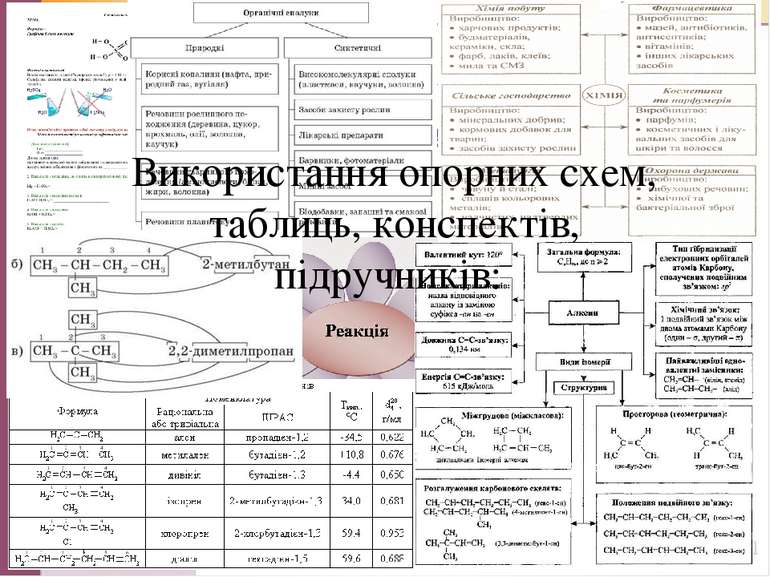
Використання опорних схем, конспектів, підручників Використання опорних схем, таблиць, конспектів, підручників:
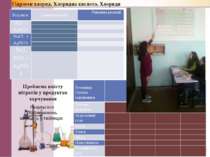
Результати спостережень запишіть у таблицю: Гідроген хлорид. Хлоридна кислота. Хлориди Проблема вмісту нітратів у продуктах харчування Реагенти Ознаки реакцій Рівняння реакцій HCl i AgNO3 NaCl i AgNO3 Na2SO4i AgNO3 Речовини Ознаки порівняння Хімічна формула Агрегатний стан Колір Блиск Запах Пластичність Розчинність у воді
Застосування хімічного експерименту Спонукає до успішного засвоєння теоретичного матеріалу; формує уміння й навички використання хімічних знань при роботі з хімічними речовинами та обладнанням; удосконалює мислення, спостережливість та допитливість.
Схожі презентації
Категорії