Презентація на тему:
Теорія як вища форма наукових знань.
Завантажити презентацію
Теорія як вища форма наукових знань.
Завантажити презентаціюПрезентація по слайдам:
Теорія хімічної будови органічних сполук О.М. Бутлерова Теорія як вища форма наукових знань.
Мета. Показати залежність властивостей органічних речовин від їх будови. Розширити і поглибити знання учнів про взаємозв'язок між будовою та властивостями речовин. Ознайомити з основними положеннями теорії хімічної будови органічних сполук О.Бутлерова, простежити її розвиток, визначити її наукове значення.
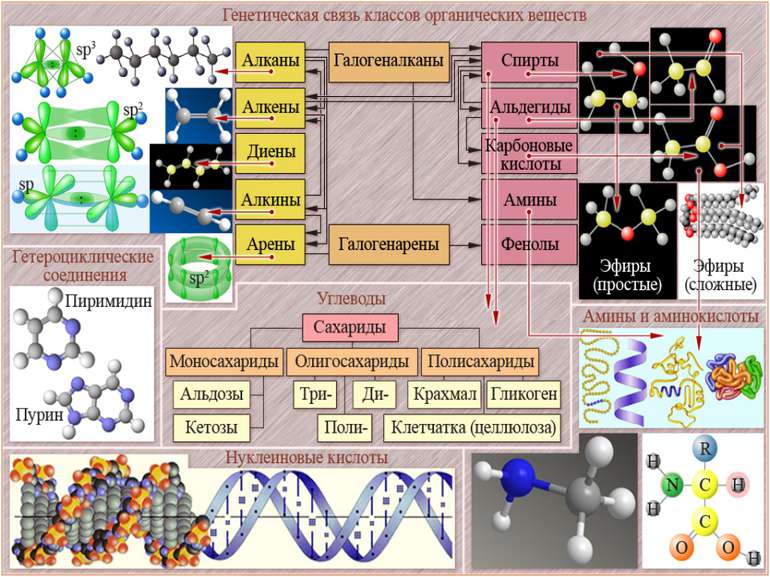
Основні «протиріччя» органічної хімії Різноманіття речовин - утворене невеликим числом елементів; Як здається невідповідність валентності в органічних речовинах - С3Н8; Різні фізичні і хімічні властивості сполук, які мають однакову молекулярну формулу (С6Н12О6 - глюкоза, фруктоза; С4Н10О - бутиловий спирт, діетиловий ефір)
Передумови виникнення. 2.Откривалісь все нові і нові сполуки карбону, кількість яких лавиноподібно зростала. 1.Теорія будови органічних сполук стала результатом узагальнення багатющого фактологічного матеріалу, який накопичила органічна хімія на початку XIX ст. 3.Вчені початку XIX ст. не могли пояснити різноманіття органічних сполук, а так само і явище ізомерії.
Фрідріх Велер 1800-1882 Фрідріх Велер в одному з листів до Йенс Берцеліус так описував органічну хімію: «Органічна хімія може зараз кого завгодно звести з розуму. Вона здається мені дрімучим лісом, повним дивних речей, безмежної хащі, з якої не можна вибратися, куди не насмілюєшся проникнути ... »
4. Англійський учений Едуард Франкланд, спираючись на ідеї атомістики, в 1853 р. ввів поняття валентність. Э. Франкланд 1825-1899 Валентність - це властивість атомів хімічних елементів утворювати хімічні зв'язки. Вона визначає число хімічних зв'язків, якими даний атом сполучений з іншими атомами в молекулі.
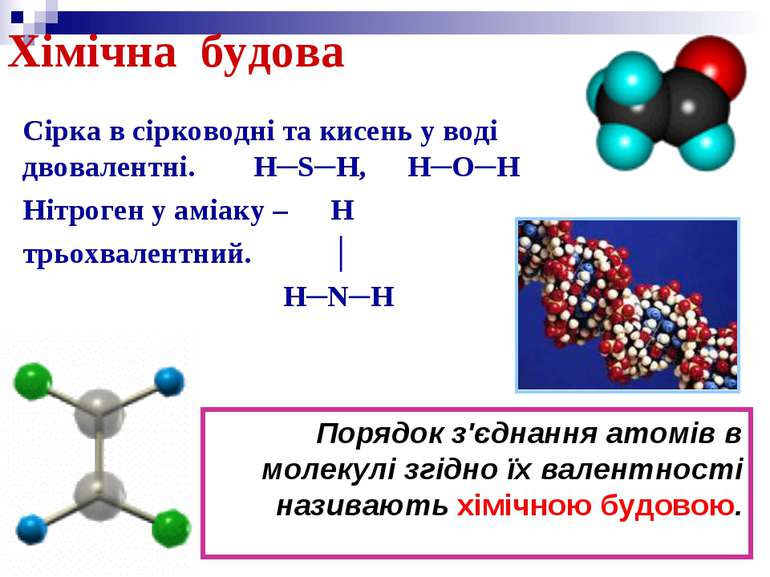
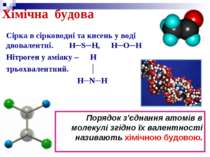
Хімічна будова Сірка в сірководні та кисень у воді двовалентні. H─S─H, H─O─H Нітроген у аміаку – H трьохвалентний. │ H─N─H Порядок з'єднання атомів в молекулі згідно їх валентності називають хімічною будовою.
Теорія хімічної будови - результат узагальнення ідей видатних вчених-органіків з трьох європейських країн: німця Ф. Кекуле, англійця А. Купера та російської А. Бутлерова. У 1861 р. А. М. Бутлеров створив наукову теорію будови органічних речовин. У 1857 р. Ф. Кекуле відніс вуглець до чотирьохвалентних елементів. В1858 р. А. Купер зазначив, що атоми вуглецю здатні з'єднаються один з одним в різні ланцюги. Ф. Кекуле 1829-1896 А.М.Бутлеров 1828-1886
Бутлеров Олександр Михайлович Учень Mиколи Зініна. У 1849 році закінчив Казанський університет і там же викладав у 1850—68 роках. З 1869 року — професор Петербурзького університету, з 1874 — ординарний академік Петербурзької академії наук. Наукова діяльність Бутлерова була спрямована на створення і утвердження теорії будови органічних сполук. За цією теорією властивості хімічні сполуки залежать від кількості і якості атомів, з яких складається молекула, від послідовності і характеру їхнього зв'язку та взаємного впливу.
Бутлеров вважав, що кожній молекулі речовини відповідає певна будова, яку можна виразити за допомогою формули, де більш-менш точно відображені реальні зв'язки та розташування атомів у молекулі.
Теорія Бутлерова пояснила явище ізомерії, дала можливість визначити будову органічних речовин і передбачити нові класи органічних сполук. Бутлеров добув полімер формальдегіду (1859), синтезував уротропін (1860), вперше добув штучну цукристу речовину (1861). Він синтезував третинні спирти, передбачені його ж теорією, добув ізобутилен і відкрив реакцію його полімеризації. В 1864—66 роках опублікував підручник «Вступ до повного вивчення органічної хімії», в якому теорія хімічної будови була вперше поширена на всі класи органічних сполук.
Пам'ятник Олександру Бутлерову в Казані Учень знаменитого академіка Зініна, він став хіміком не в чужих краях, а в Казані Через шість років Бутлеров був обраний академіком Петербурзької академії наук. Помер Олександр Михайлович в 1886 році, не доживши кількох днів до свого пятідесятівосьмілетія.
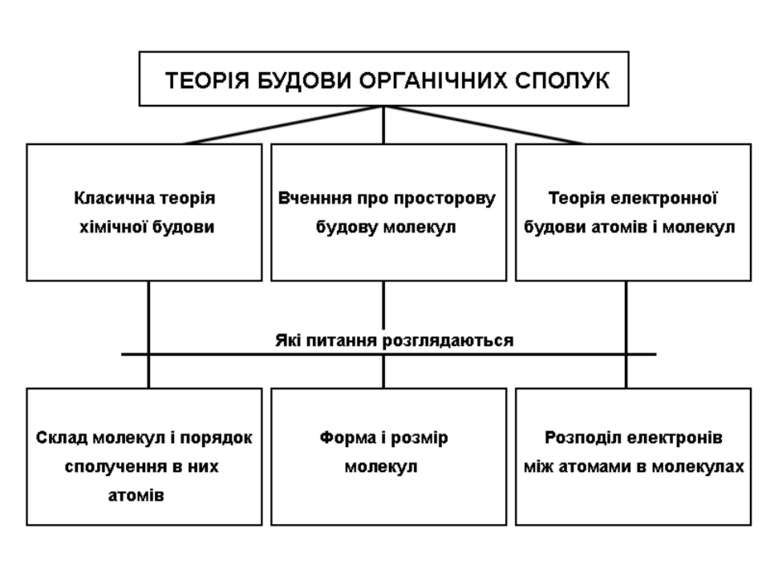
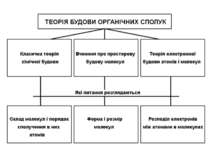
Основні положення теорії хімічної будови органічних сполук • у хімічних сполуках атоми зєднуються між собою у перному порядку відповідно до їх валентності, що визначає хімічну будову молекул; • хімічні і фізичні властивості огранічних сполук залежать як від природи і кількості атомів, що входять до їх складу, так і від хімічної будови молекул;
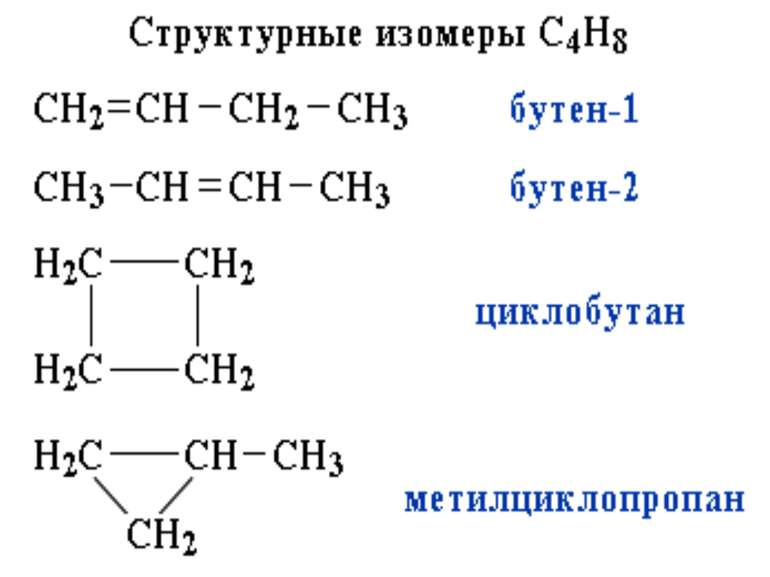
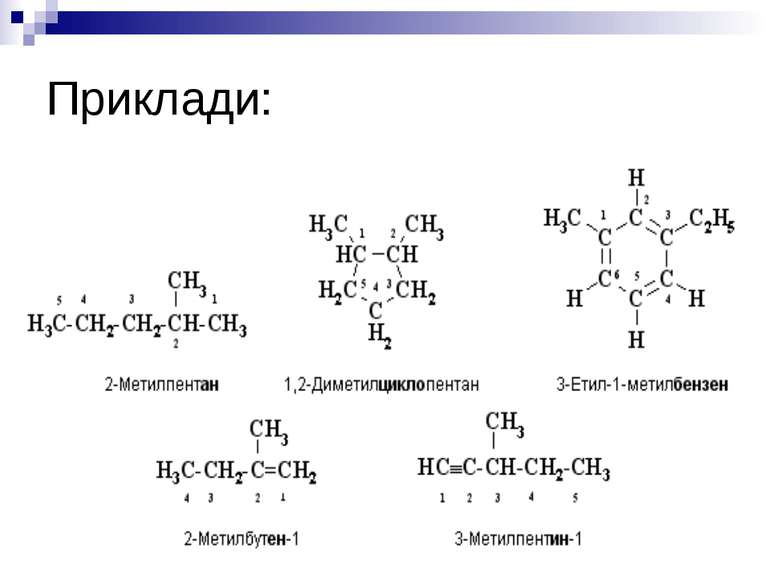
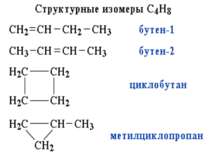
для кожної емпіричної формули можна вивести певну кількість теоретично можливих структур (ізомерів); кожна органічна речовина має лише одну формулу хімічної будови, яка дає уявлення про властивості даної сполуки; у молекулах існує взаємний вплив атомів як бепосередно звязаних, так і безпосередньо не звязаних один з одним. Основні положення теорії хімічної будови органічних сполук
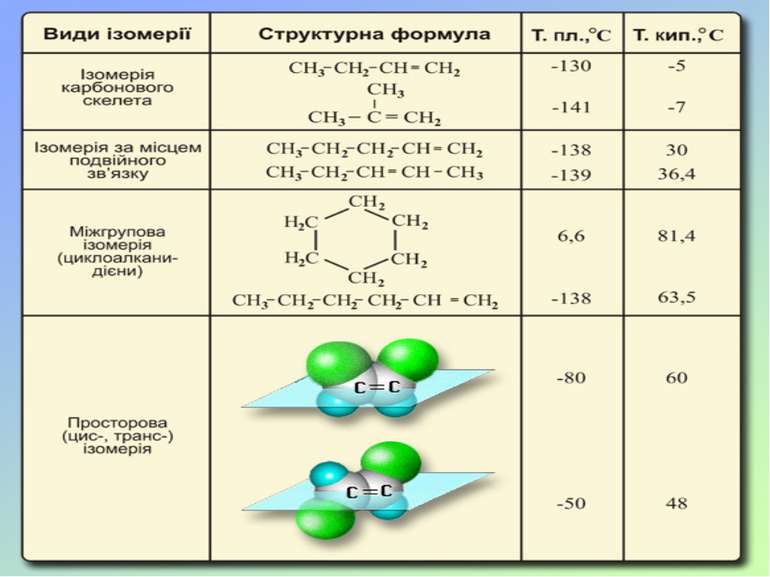
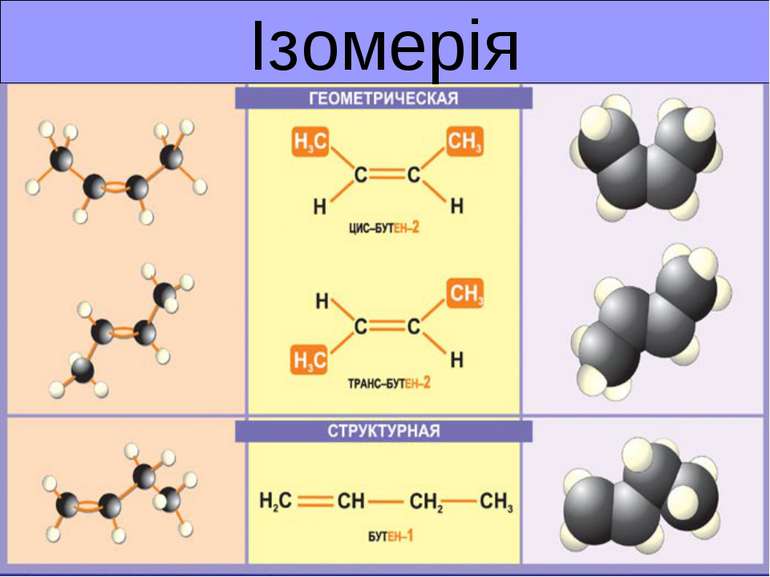
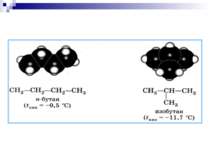
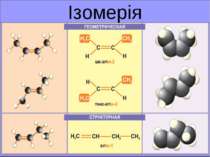
Ізомерія - це явище існування різних речовин - ізомерів, що мають однаковий якісний і кількісний склад, але різну будову і, отже, різні властивості. Етиловий спирт Диметиловий етер
Теорія О.М.Бутлерова має фундаментальне значення для розвитку хімії, оскільки визначає основні особливості хімічної будови молекул. На основі терії О.М.Бутлерова розроблено сучасну номенклатуру і класифікацію органічних сполук.
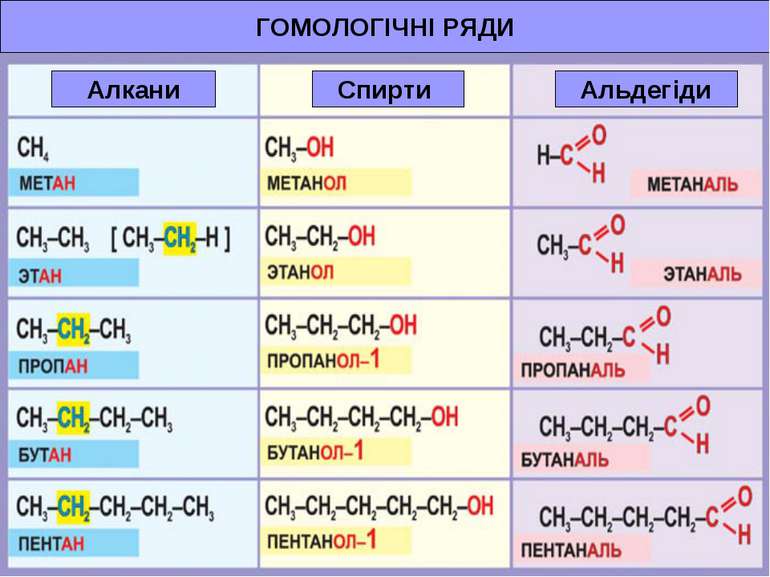
Гомологічний ряд. Гомологи. Гомологічним рядом називають відповідний ряд речовин розташованих поруч в порядку зростання їх Mr, подібних за будовою і хімічними властивостями, де кожен член - гомолог, який відрізняється від попереднього гомологічною різницею ─ CH2 ─ гомологічний ряд алканів
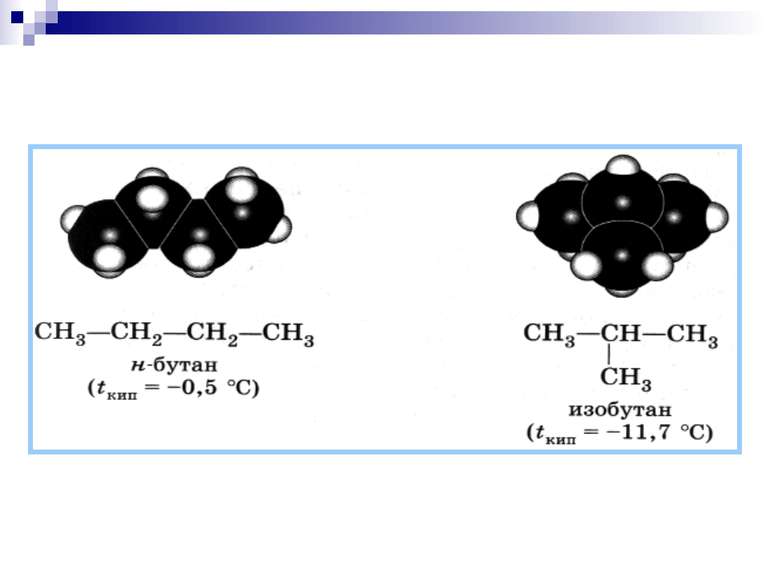
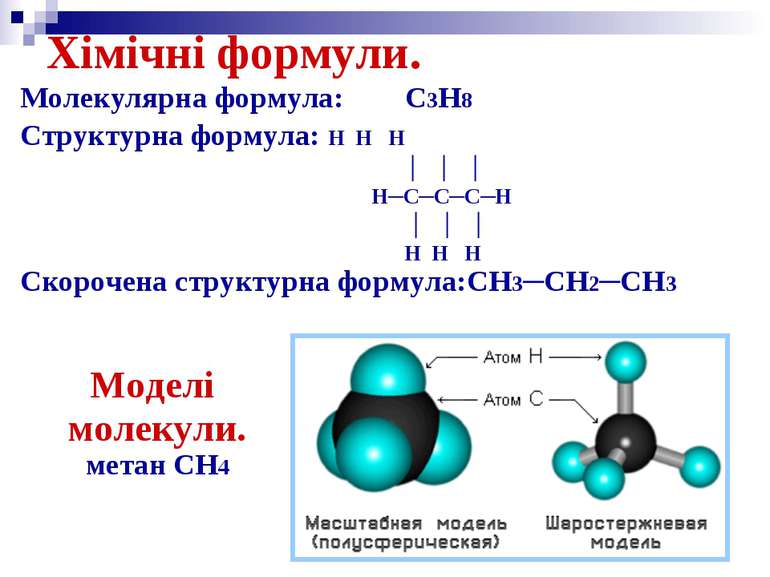
Хімічні формули. Молекулярна формула: C3H8 Структурна формула: H H H │ │ │ H─C─C─C─H │ │ │ H H H Скорочена структурна формула:CH3─CH2─CH3 Моделі молекули. метан CH4
Схожі презентації
Категорії