Презентація на тему:
"Лужні, лужноземельні метали та магній"
Завантажити презентацію
"Лужні, лужноземельні метали та магній"
Завантажити презентаціюПрезентація по слайдам:
«Лужні, лужноземельні метали та магній». Урок в 10 класі КЗ Верхівцевського НВК Учитель Кукса Н.М.
1.Узагальнити і систематизувати знання про лужні та лужноземельні метали. 2.Вміти характеризувати елементи за положенням в періодичній таблиці. 3.Знати фізичні і хімічні властивості . 4.Вміти пояснити біологічну роль елементів та значеня в промисловості. 5.Захист довкілля від шкідливого впливу мийних засобів. 4. 4. Цілепокладання:
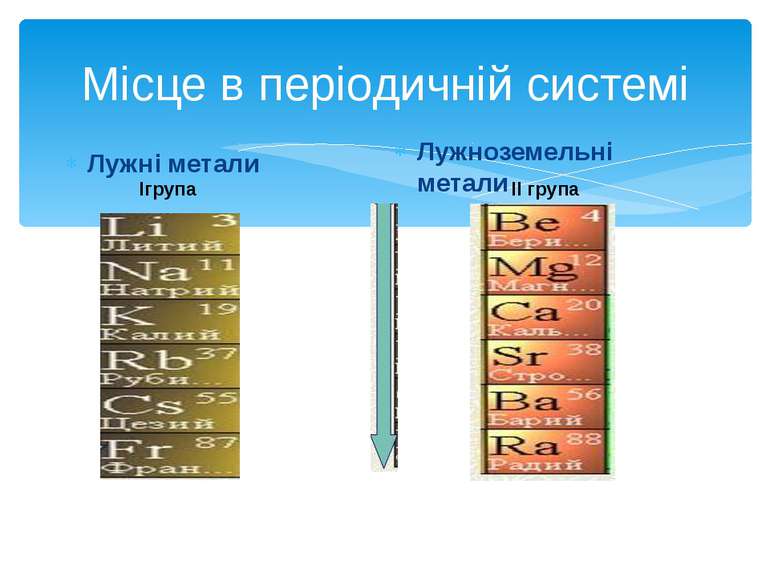
Фізичні властивості Лужні метали Лужні метали — м'які (натрій ріжеться ножем, як вершкове масло, інші трохи жорсткіші) метали від сріблисто-білого до сірого кольору з характерним блиском, що дуже швидко тьмяніють на повітрі. Легкоплавкі й рухливі. Агресивні, вибухонебезпечні (зберігаються під шаром гасу (керосин)) Лужноземельні метали. Практично всі ці елементи являють собою тверді речовини сіруватого кольору (принаймні, при нормальних умовах і кімнатній температурі) Володіють вищими за лужні метали t°пл. і t°кип., потенціалами іонізації, щільністю і твердістю. Знайдіть у підручнику , які фізичні властивості має магній, чи дуже вони відрізняються від властивостей лужноземельних металів
Физичні властивості Mg Колір – блискучий, сріблясто-білий t пл. = 651°C. t кип. ≈ 1107°C. електропровідний Легкий, густина ρ = 1,74 г/см3 Відносно м’який, пластичний.
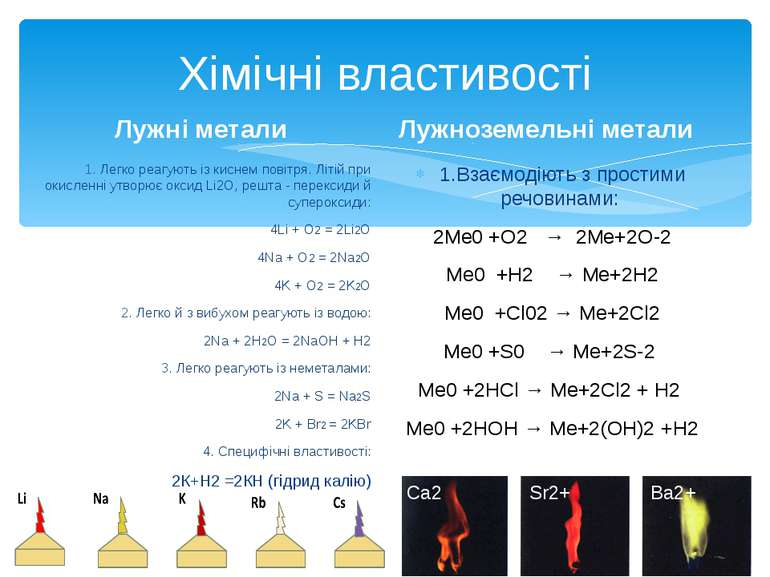
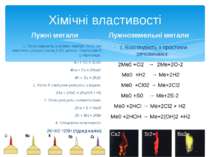
Хімічні властивості Лужні метали 1. Легко реагують із киснем повітря. Літій при окисленні утворює оксид Li2O, решта - перексиди й супероксиди: 4Li + O2 = 2Li2O 4Na + O2 = 2Na2O 4K + O2 = 2K2O 2. Легко й з вибухом реагують із водою: 2Na + 2H2O = 2NaOH + H2 3. Легко реагують із неметалами: 2Na + S = Na2S 2K + Br2 = 2KBr 4. Специфічні властивості: 2К+Н2 =2КН (гідрид калію) Лужноземельні метали 1.Взаємодіють з простими речовинами: 2Me0 +O2 → 2Me+2O-2 Me0 +H2 → Me+2H2 Me0 +Cl02 → Me+2Cl2 Me0 +S0 → Me+2S-2 Me0 +2HCl → Me+2Cl2 + H2 Me0 +2HOH → Me+2(OH)2 +Н2 Ca2 Sr2+ Ba2+
Відмінні властивості магнію. 4Mg + Fe3O4 = 4MgO + 3Fe 3Mg + Al2O3 = 3Mg O + 2Al Магнйтермія - відновленням оксидів металів магнієм, яке супроводжується виділенням значної кількості теплоти.
Основний характер оксидів та гідроксидів металів. Ме―Ме2О―МеОН―сіль Ме―МеО―Ме(ОН)2―сіль Складіть будь ласка ланцюжки для Li,та Mg
Поширення в природі У природі лужні елементи трапляються лише у вигляді солей. Найважливішими мінералами Натрію є кам’яна сіль або галіт NaCl, чилійська селітра NaNO3, глауберова сіль або мірабіліт Na2SO4 • 10H2O. Велика кількість солей Натрію кристалізується при випаровуванні морської води. Масова частка Натрію у земній корі становить 2,6 %. Калій, як і Натрій, є досить розповсюдженим хімічним елементом. Масова частка Калію в земній корі — 2,5%. Природні солі Калію : сильвін KCl, сильвініт КCl ∙ NaCl карналіт КCl ∙ MgCl2 ∙ 6H2O Калій входить до складу польових шпатів і слюди. Літій досить широко поширений в земній корі польовий шпат
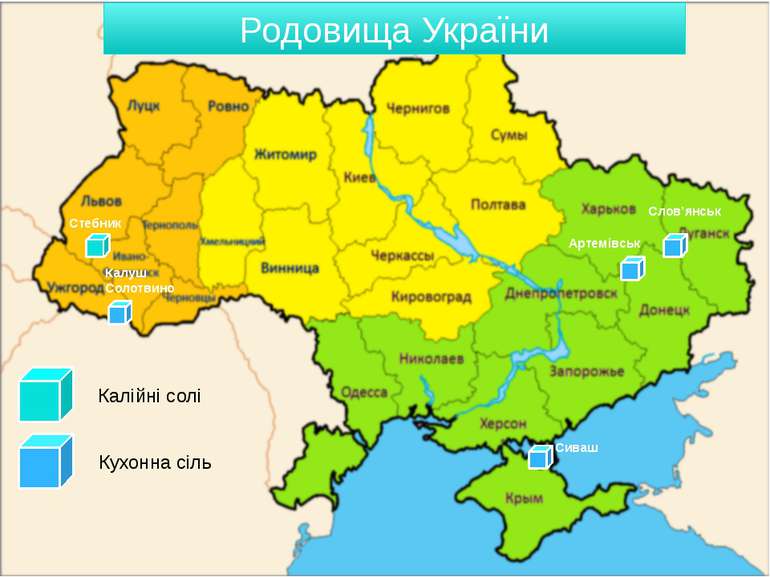
Поширення в природі У зв'язку з високою хімічною активністю у вільному стані в природі він не зустрічаються, а тільки у вигляді різних сполук. Деякі з них, як хлорид калію, утворюють потужні родовищ Найбагатші у світі родовища солей калію у вигляді мінералів сильвіну KCl, сильвініту KCl·NaCl, карналіту КCl ∙ MgCl2 ∙ 6H2O і каїніту KCl·MgSO4·3H2O розташовані поблизу м. Солікамська. Крім того, значні поклади сполук калію знайдені в Білорусії (м. Солігорськ) і в Україні (м. Калуш і м. Стебник у Прикарпатті). хлорид калію нітрат калію
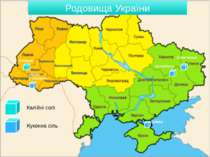
Родовища України Калійні солі Кухонна сіль Стебник Калуш Солотвино Слов’янськ Артемівськ Сиваш
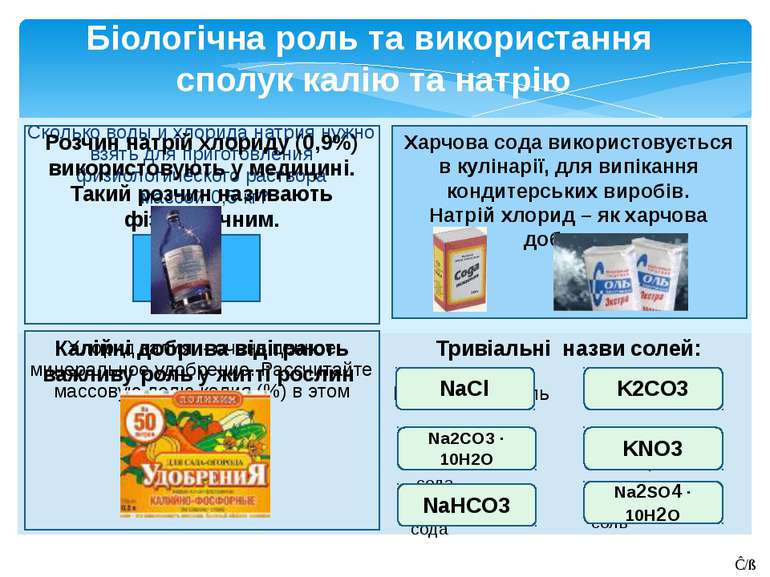
Біологічна роль та використання сполук калію та натрію ответ ответ ответ NaCl Кристалли-ческая сода Na2CO3 · 10H2O Питьевая сода NaHCO3 поташ K2CO3 Калийная селитра KNO3 Глауберова соль Na2SO4 · 10H2O Ĉ/ß Розчин натрій хлориду (0,9%) використовують у медицині. Такий розчин називають фізіологічним. Харчова сода використовується в кулінарії, для випікання кондитерських виробів. Натрій хлорид – як харчова добавка. Калійні добрива відіграють важливу роль у житті рослин Скольководы и хлорида натрия нужно взять для приготовления физиологического раствора массой 0,5 кг? 4,5г соли 495,5 г воды Смесь хлорида и гидрокарбоната натрия массой 15 г обработали уксусной кислотой,при этом выделилось 2,8 л (н.у.) газа. Определите массовые доли в процентах компонентов смеси. 70%NaHCO3 30%NaCl Хлорид калия - очень ценное минеральное удобрение. Рассчитайте массовую долю калия (%) в этомвеществе. 52% Тривіальніназвисолей: Повареннаясоль Для работы слайда необходимо кликнуть мышью на любой синий прямоугольник. Для 1-3 ячейки таблицы это задача. Для 4 ячейки - проверка знаний тривиальных названий веществ.
Поширення в природі лужноземельних металів. У зв'язку з високою хімічною активністю у вільному стані в природі вони не зустрічаються, а тільки у вигляді різних сполук. Наприклад: Гіпс CaSO4∙ 2H2O , барітова каша BaSO4 Апатит Ca3(PO4)2 , вапняк,мармур CaCO3 Вапно Са(ОН)2 Та інші.
Біологічна роль та використання магнію Ĉ/ß Магнійвходить до складухлорофілуі,отже,відіграєнезаміннуроль уфотосинтезіі вгазообмініпланети;загальнийвмістмагніюв тканинахрослиннаЗемлізадеякимиоцінкамискладаєблизько1011 тонн. Крімхлорофілу,магнійувсіхтканинахрослинбереучастьтакожвутворенніжирів, уперетворенніфосфорнихсполук. Особливобагатомагніюв сокукаучуконоснихрослин. Бракмагніюпризводитьдозменшеннякількостіхлорофілуі до побледнению ізмінізабарвленнялистяначервонуіжовту Англійськасіль(MgSO4 ? 7H2O )використовуєтьсяякпроноснеіжовчогіннийзасіб. Приін'єкціяхвонавикликаєстан,близькийдонаркотичного, івикористовуєтьсядляборотьбизсудомами, длялікуваннягіпертонії,психічногозбудження; впоєднаннізіншимипрепаратами - длязнеболюванняпри пологах. Воднірозчинитіосульфатумагніювикористовуютьсядлялікуванняопіківтаіншихзахворюваньшкіри. Біламагнезія(MgCO3 )входить до складузубнихпорошківіприсипок;крімтого, воназменшуєкислотністьшлунковогосоку. Паленамагнезія(MgO)тежнейтралізуєшлунковийсік.Крімтого, воназастосовуєтьсявсерединуприкислотнихотруєннях. Для работы слайда необходимо кликнуть мышью на любой синий прямоугольник. Для 1-3 ячейки таблицы это задача. Для 4 ячейки - проверка знаний тривиальных названий веществ.
Так як у лужному середовищі гинуть мікроорганізми,то речовини з цим середовищем є добрими антисептиками: мило, СМС. Ці речовини,також добре розчиняють жири. Застосування лужних властивостей сполук металів.
Користь,та шкода лужного середовища. Тому, регулярне миття рук з милом , захистить вас від хвороб Але в лужному середовищі гинуть як шкідливі,так і корисні мікроорганізми.
Перевірка знань Порівняйте атоми елементів, поставивши знаки або = замість *: а) заряд ядра: Mg * Ca, Na * Mg, Ca * К; б) число електронних шарів: Mg * Ca, Na * Mg, Ca * К; в) число електронів на зовнішньому рівні: Mg * Ca, Na * Mg, Ca * К; г) радіус атома: Mg * Ca, Na * Mg, Ca * K
Рефлексія: Продовжіть ланцюжок: Я знаю ….. Я вмію ….. Я використовую …… Мені це буде необхідно для ….. Я навчився …… Я набув вміння …….
Схожі презентації
Категорії