Презентація на тему:
Кислоти
Завантажити презентацію
Кислоти
Завантажити презентаціюПрезентація по слайдам:
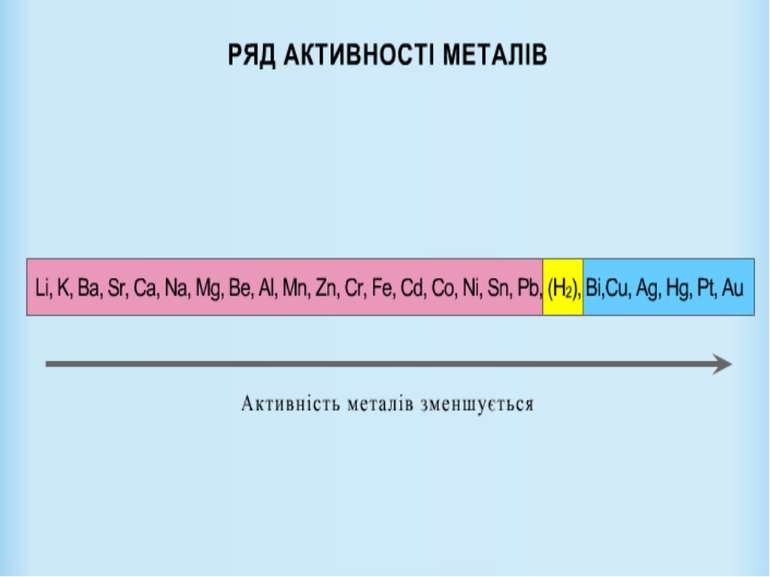
Сторінка перша “Очікувані результати” закріпити знання про хімічні властивості кислот; удосконалити вміння використовувати ряд напруг металів, складаючи хімічні реакції, що відбуваються за участі металів; - розвивати навички складання хімічних реакції; знати правила техніки безпеки під час роботи з кислотами.
Сторінка друга « Увага! Це повинен знати кожен» Проблема. Як правильно змішати дані речовини?
1. Під час роботи з кислотами слід бути обережним. Особливо слід берегти очі. У разі потрапляння кислоти на руки необхідно негайно змити її великою кількістю води. Правила техніки безпеки під час роботи з кислотами.
Правила техніки безпеки під час роботи з кислотами. 2. Уважно читайте етикетку на банці з речовиною, яку берете для досліду. 3. Відкривши банку, не кладіть пробку на лабораторний стіл, а поставте її.
Правила техніки безпеки під час роботи з кислотами. 4. Наливаючи рідини, посудину з реактивом беріть так, щоб етикетка була направлена в бік долоні, знімайте краплю з краю шийки, інакше рідина стікатиме по склу та псуватиме етикетку, може пошкодити шкіру рук.
Правила техніки безпеки під час роботи з кислотами. 5. Посудину, з якої взяли реактив, відразу ж закрийте та поставте на місце. 6.У разі потрапляння кислоти на руки або лице, шкіру необхідно промити водою, 3% соди.
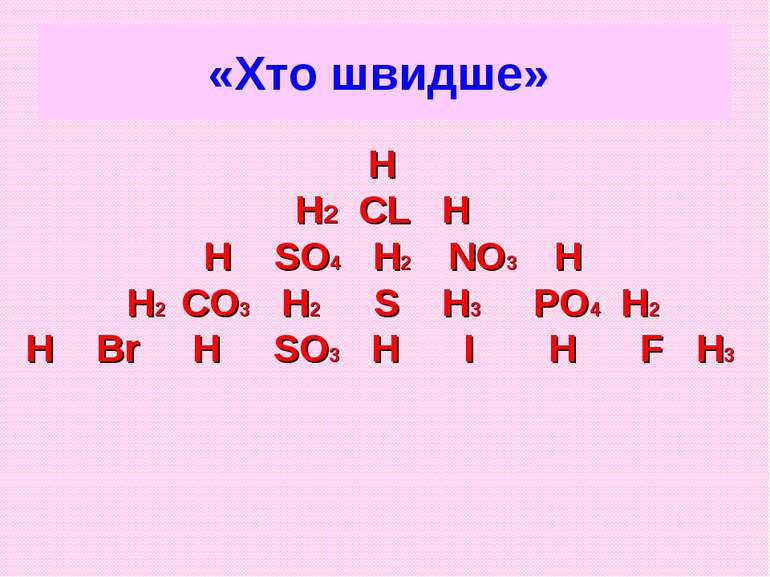
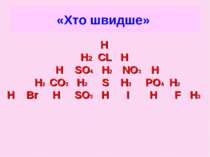
Правильні відповіді З оксигеновмісних кислот: H2CO3, H2SO4, H2SO3, HNO3, H3PO4, H2SiO3, З одноосновних кислот: HCl, HI, HF, HBr, HNO3. З двоосновних кислот: H2CO3, H2SO4, H2SO3, H2SiO3, H2S. З безоксигеновмісних кислот: HCl, HI, HF, HBr, H2S.
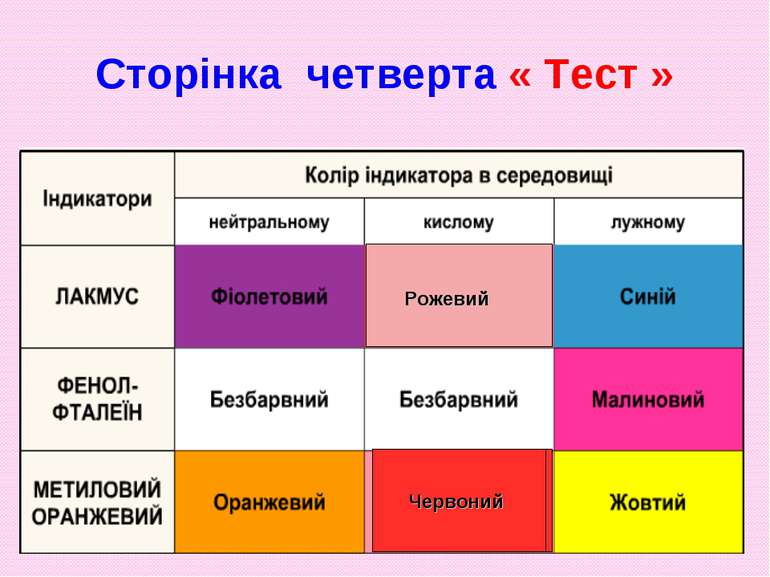
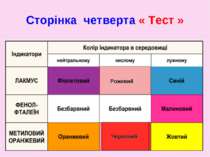
Допоможіть встановити ! Жовту смужку паперу занурюємо в рідину. Посиніє — маємо …, почервоніє — … Колір не змінює в середовищі …. І за ці підказки усі кличуть її …
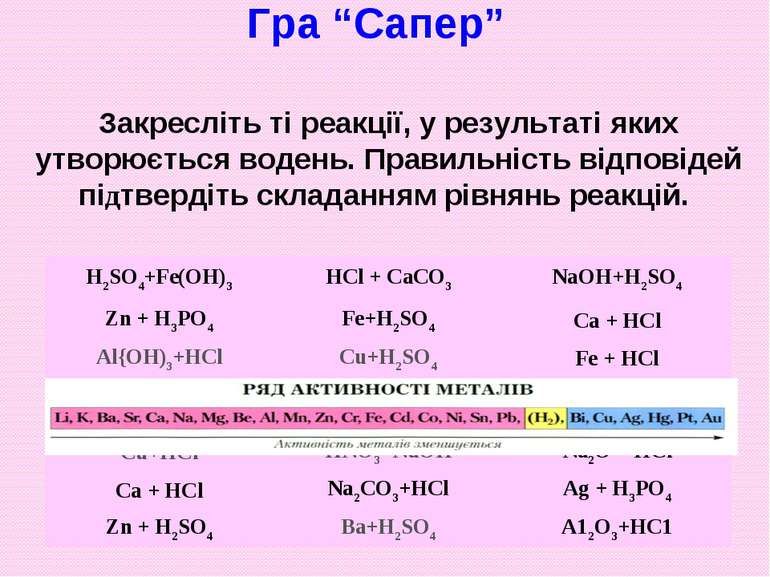
Гра “Сапер” Закресліть ті реакції, у результаті яких утворюється водень. Правильність відповідей підтвердіть складанням рівнянь реакцій. H2SO4+Fe(OH)3 HCl + CaCO3 NaОН+H2SO4 Zn + H3PO4 Fe+H2SO4 Ca + HCl Al{OH)3+HCl Cu+H2SO4 Fe + HCl 2 варіант Cu+HCl HNO3+NaOH Na2O + HCl Ca + HCl Na2CO3+HCl Ag + H3PO4 Zn + H2SO4 Ba+H2SO4 A12O3+HC1
Рецепти коктелів: 1) «Полуничний коктейль» Рецепт: кислота + метиловий оран жевий. 2) «Молочний» коктейль Рецепт: HCl + AgNO3 3) «Ягідка» ' Рецепт: кислота + лакмус. 4) «Блакить» Рецепт: CuO + H2SO4 5) «Содовий» Рецепт: СаСО3+НС1 6) «Шипучка» Рецепт: Zn + HCl
“Хімічне печиво” Заповнити пропуски в таблиці «Формули солей». Формула кислоти Na Mg Fe(III) H2S04 HCl Формула кислоти Ag(I) Cu(II) Fe(III) НІ H3P04
Гра “Один, два, три” 1).Запишіть три засвоєні вами поняття, правила. 2).Запишіть два поняття або правила, які ви успішно застосовуєте на практиці. 3).Запишіть одне поняття або правило, яке вам необхідно відпрацювати.
Схожі презентації
Категорії