Презентація на тему:
Кількісний склад розчину. Масова частка розчиненої речовини. Приготування розчинів
Завантажити презентацію
Кількісний склад розчину. Масова частка розчиненої речовини. Приготування розчинів
Завантажити презентаціюПрезентація по слайдам:
Запитання Чим відрізняється розчин від механічної суміші? Чим відрізняється розчин від хімічної сполуки? Чи є склад розчину постійним? Які розчини називаються насиченими? Які розчини називаються ненасиченими? Які розчини називаються концентрованими?
Які розчини називаються розведеними? Запропонуйте способи перетворення насиченого розчину на ненасичений. Запропонуйте способи перетворення ненасиченого розчину на насичений. Що станеться, якщо помістити кристалик твердої речовини в ненасичений розчин? Що станеться, якщо помістити кристалик твердої речовини в насичений розчин? Що станеться, якщо помістити кристалик твердої речовини в пересичений розчин?
Скільки кристалізаційної води міститься в 1 кг мідного купоросу CuSO4·7H2O? Розв’язання M (CuSO4·7H2O) = 160 + 7·18 = 286 (г/моль) M (H2O) = 18 г/моль 286 — 7·18 1000 — х х = 440,6 н (H2O) Як приготувати розчин? Як визначити склад розчину?
Способи вираження складу розчинів ω = m (речовини)/ m (розчину)·100%, де m(речовини) — маса розчиненої речовини, г; m (розчину) = m (речовини) + m (розчинника) — маса розчину, г. Використовуючи цю формулу, можна обчислити масу речовини й розчину: m (реч.) = m (розч.) · ω/100% m (розч.) = m (реч.) · ω/100% Масова частка розчиненої речовини — безрозмірна величина, виражається в частках від одиниці або відсотках.
Виконання тренувальних вправ Задача 1 Обчисліть масову частку розчиненої речовини в розчині, одержаному в результаті змішування 20 г цукру і 130 г води.
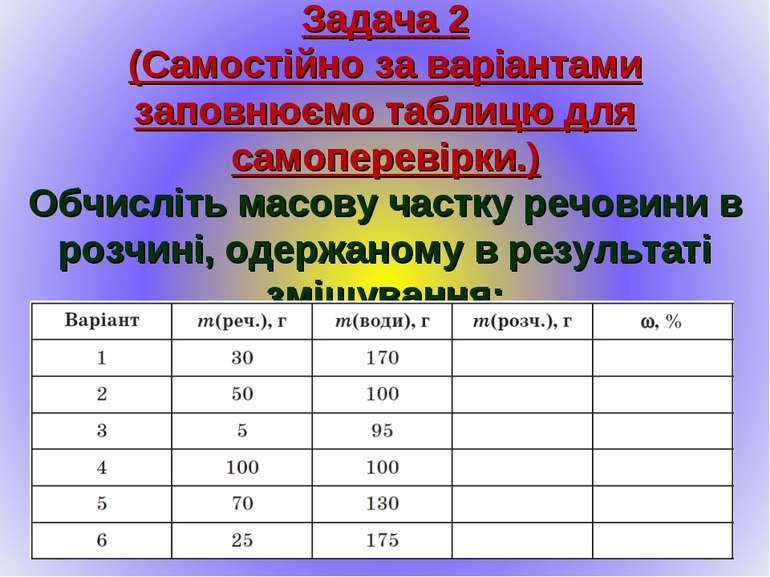
Задача 2 (Самостійно за варіантами заповнюємо таблицю для самоперевірки.) Обчисліть масову частку речовини в розчині, одержаному в результаті змішування:
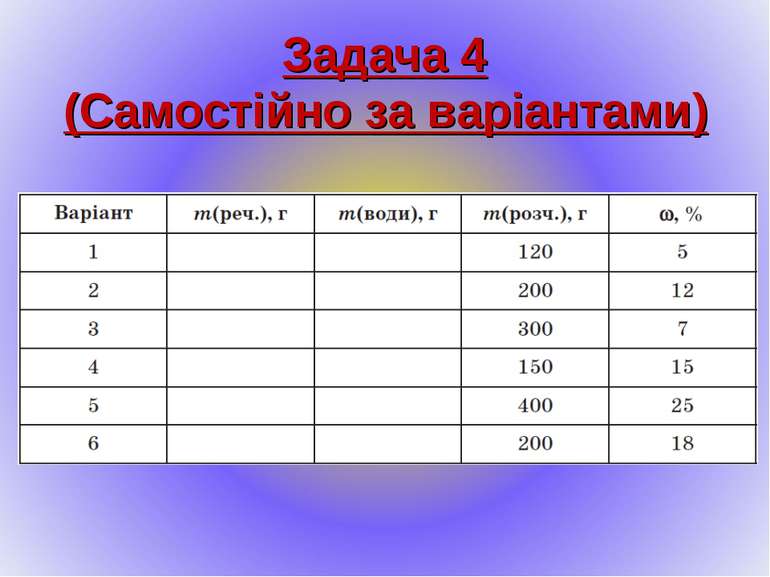
Задача 3 Обчисліть, яку масу натрій хлориду й води необхідно взяти для приготування 200 г розчину з масовою часткою розчиненої речовини 10 %.
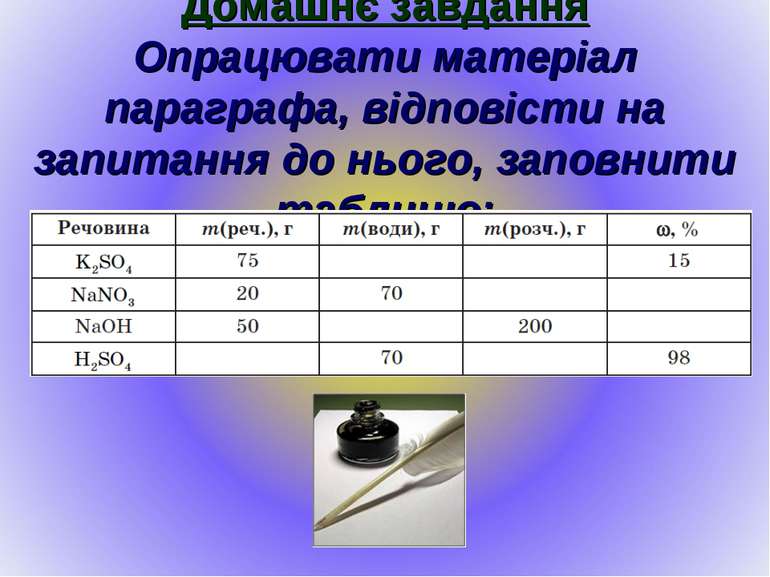
Домашнє завдання Опрацювати матеріал параграфа, відповісти на запитання до нього, заповнити таблицю:
Схожі презентації
Категорії