Презентація на тему:
Хімічний склад атмосферного повітря та його гігієнічне значення. Денатурація повітряного середов приміщень, шляхи та засоби її профілактики.
Завантажити презентацію
Хімічний склад атмосферного повітря та його гігієнічне значення. Денатурація повітряного середов приміщень, шляхи та засоби її профілактики.
Завантажити презентаціюПрезентація по слайдам:
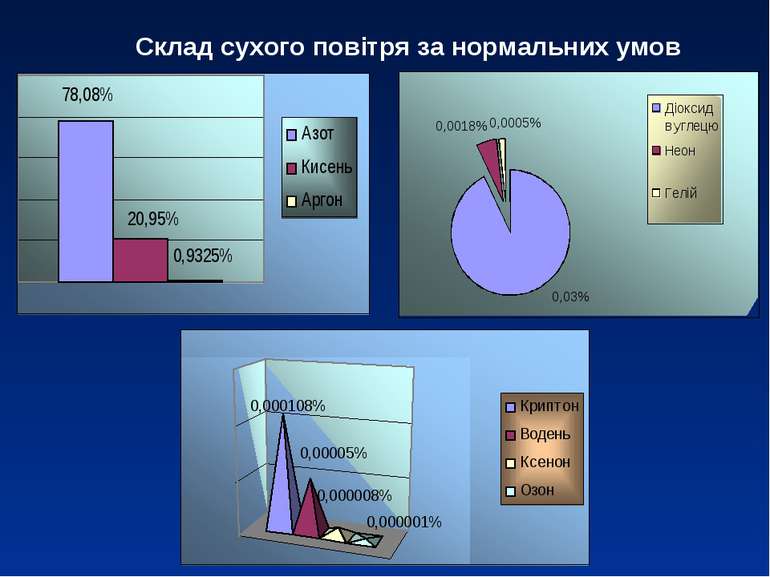
Хімічний склад атмосферного повітря та його гігієнічне значення. Денатурація повітряного середовища приміщень, шляхи та засоби її профілактики.
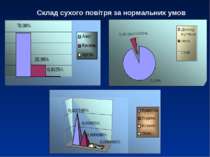
Основний склад атмосферного повітря: кисень (О2) азот (N) діоксид вуглецю (CO2) А також до складу атмосферного повітря входять: водень (Н2) метан (СН4) аміак (NH4) сірководень (SH4) перекис водню (Н2О2)
Повітря N О2 СО2 Атмосферне 78,97 20,7-20,9 0,03-0,04 Води від 1 до 30 г в 1 мз Те, що видихається 79,2 15,4-16 3,4-4,7 Насичене
Чистий кисень важчий за повітря: 1 л О2 при 0° і 760 мм рт.ст. важить 1,429 г. Повітря за тих же умов важить 1,293 г. Кількість кисню в атмосферному повітрі біля земної поверхні коливається в невеликих межах - 20,7-20,9%
При зменшенні вмісту кисню нижче 16% прискорюється дихання і збільшується кількість серцевих ударів. При 7-8% кисню ці компенсаторні явища не допомагають, настає асфіксія, зниження температури тіла, анурія або сеча з кров'ю, знепритомнення і смерть. Під час розтину спостерігається жирове переродження внутрішніх органів. Треновані люди, наприклад, пілоти, можуть протягом деякого часу витримувати концентрації кисню 10% і нижче. Водолази без шкідливих наслідків дихають повітрям, що містить 50% кисню. Так само нешкідливе дихання 30-50% киснем для хворих.
Водень (Н) Утворюється у високих шарах атмосфери в результаті фотохімічного розкладання молекул води на кисень і водень. Метан (СН4) виділяється при анаеробному гнитті органічних сполук як складова природного газу. Концентрація його в атмосферному повітрі не перевищує 0,00022% (Не підтримує дихання. При накопиченні його в повітрі у великих концентраціях можлива смерть від асфіксії.)
Аміак (NH4) Його концентрація залежить від ступеня забрудненості даної території: в чистому повітрі (вдалині від населених пунктів) – 0,003-0,005 мг/м3 Перекис водню (Н2О2) Утворюється внаслідок взаємодії ультрафіолетових променів із молекулами повітря і разом з озоном сприяє окисленню органічних речовин в атмосфері
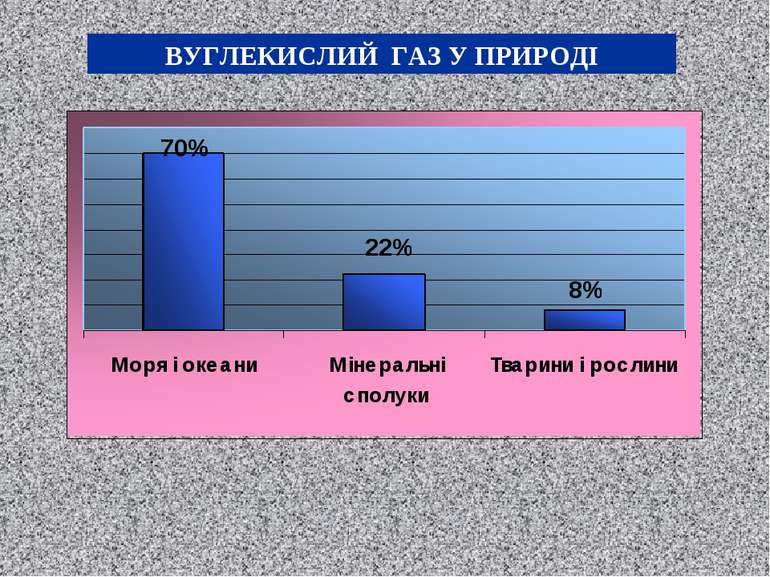
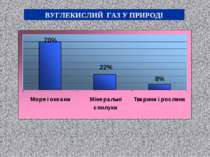
Вміст вуглекислоти в зовнішній атмосфері коливається від 0,03 до 0,04%. Джерела її: дихання людей, тварин, горіння, гниття, виділення з ґрунту, рудників, вулканів, деяких мінеральних джерел. Поряд з утворенням відбувається витрачання вуглекислоти. Рослини, споживаючи вуглекислоту, утворюють у своїх тканинах вуглеводи, а за наявності азоту і білки. Великі кількості вуглекислоти виносяться з атмосфери з дощами. Підвищені концентрації вуглекислоти негативно впливають на організм людини: а) при 3% спостерігається прискорення і поглиблення дихання; б) при 4%, окрім цього, з'являється відчуття стиснення голови, головний біль, шум у вухах, психічне збудження, серцебиття, сповільнення пульсу, іноді блювання і непритомність; в) при 6-8% – перелічені явища посилюються; г) при 10% настає швидке знепритомнення і зупинка дихання, хоча серце ще деякий час продовжує працювати; д) при 20% через декілька секунд настає параліч мозкових центрів і смерть.
Озон при високих концентраціях має запах, подібний до запаху хлору, при помірних - "запах електрики". Виявляється нюхом при концентрації 0,002 мг/л.
Озон постійно міститься в повітрі рентген- і фізіотерапевтичних кабінетів, утворюючись під впливом кварцевих ламп, іскрових розрядів, і іноді викликає у персоналу ряд хворобливих явищ. Великі кількості його діють снодійно. Концентрації 0,002-0,005 мг/л: подразнюють слизові дихальних шляхів, викликають запаморочення, слинотечу, посилене потіння, втому. У дрібних тварин вдихання повітря, що містить 0,01 мг/л озону, через кілька годин викликає смерть.
Озон має дуже сильну окислювальну здатність, яка і забезпечує потужний знезаражувальний ефект. Озон інактивує бактерії та віруси набагато швидше, ніж хлор. Хлору для знищення бактерій та вірусів потрібно декілька годин, а озону – декілька секунд. Озон має ще одну унікальну властивість, яка використовується в так званому процесі "полірування" води. Ця властивість обумовлена здатністю озону флокулювати зважені у воді частинки та освітлювати воду. В результаті процесу "полірування" отримують кришталево-прозору воду блакитного кольору.
Як діє озон? Озон, або трьохатомний кисень, це нестабільний газ, який існує лише протягом декількох хвилин. Озон повинен бути використаний одразу після вироблення, його не можна зберігати через властиву йому хімічну нестабільність. Існує два методи генерування озону – метод ультрафіолетового опромінення та метод коронного розряду. Метод коронного розряду дозволяє отримувати більш високу концентрацію озону, ніж метод ультрафіолетового опромінення, що має значення при знешкодженні комплексних забруднень води. Отриманий озон змішується з потоком води всередині вакуумного інжектора. Чим довше відбувається процес змішування, тим більша кількість озону розсіються у воді. Озон повинен повністю розчинитися у воді, що є дуже важливим моментом у всьому процесі знезараження. Розчинений озон вступає в реакцію з вірусами, бактеріями та іншими забруднювачами у воді і знешкоджує їх. Третій нестабільний атом озону зв‘язує забруднювачі і руйнує їх. У воді після процесу знезараження залишається чистий кисень. Якщо ж у воді залишилась якась кількість невикористаного надлишкового озону, то через 20-30 хвилин він також перетворюється на кисень. Водночас із озонуванням у воду не можна додавати жодних хімікатів, як то хлор, хлордіоксид, перманганат т.ін. Це є важливою умовою для отримання високої якості води.
Азот - газ, мало розчинний у воді. Вважають, що для людини азот індиферентний. Він служить немовби для розбавлення кисню в атмосфері. Під впливом електричних розрядів азот окислюється й у вигляді азотистих сполук з повітря вимивається дощами в ґрунт. Це підвищує врожайність ґрунту. При підвищеному тиску чистий азот діє як наркотик. Спостерігаються: збудження, балакучість, важкість у голові, сплутаність думок, забудькуватість та інші порушення
Окис вуглецю (чадний газ) являє собою безбарвний газ, без смаку, з ледь відчутним запахом, хоч багато дослідників вважають, що він без запаху. Питома вага його менша, ніж повітря,- 0,967. Окис вуглецю є продуктом неповного окислення вуглецю. Окис вуглецю горить синюватим полум'ям. Чадний газ утворюється скрізь, де відбувається горіння при недостатності кисню, бо при достатній кількості кисню вуглець під час горіння окислювався б до вуглекислоти. Окис вуглецю надходить у повітря з топок печей, при курінні, від самоварів, гасових ламп, світильних свічок, при згорянні світильного газу в плитах, з вихлопними газами автомобільних та інших моторів, від олійної фарби в момент її висихання тощо. Максимальні концентрації окису вуглецю для людини 0,02%.
Механізм отруєння полягає в тому, що окис вуглецю зв'язується з гемоглобіном крові, утворюючи карбоксигемоглобін. Окис вуглецю має в 250-300 разів більшу спорідненість до гемоглобіну, ніж кисень. Тому навіть при порівняно дуже незначному парціальному тиску окис вуглецю швидко витісняє кисень з гемоглобіну. В останні роки деякі дослідники пояснюють механізм отруєння не стільки великою спорідненістю CO до гемоглобіну, скільки значно меншою швидкістю розпаду молекул карбоксигемоглобіну. За їх даними, гемоглобін крові насичується окисом вуглецю в 10 разів повільніше, ніж киснем, але зворотна дисоціація карбоксигемоглобіну відбувається в 3600 разів повільніше, ніж оксигемоглобіну.
Картина отруєння: в легких випадках - головний біль, запаморочення, шум у вухах, нудота, рідко блювання, загальна слабість; у тяжких випадках, крім перелічених симптомів, спостерігається розлад свідомості, сонливість, заціп’яніння. Іноді, навіть ще не знепритомнівши, людина не може рухатись. Буває сильне блювання. В подальшому явища наростають, настає непритомність, рухове і психічне збудження, судоми і смерть. Смерть настає від паралічу дихального центру. Лікування: негайно свіже повітря. Для прискорення дисоціації карбоксигемоглобіну дають вдихати кисень з 5-7% вуглекислоти. Вуглекислота збуджує дихальний центр. При зупинці дихання - штучне дихання. Для збудження дихального центру дають лобелін. В усьому іншому застосовують симптоматичні засоби. Профілактика: усунення причин утворення CO, а також провітрювання і вентиляція приміщень, де можна очікувати нагромадження цього газу.
Аміак - газ з лужним смаком і різким специфічним запахом, легко розчинний у воді. В атмосфері населених місць він виділяється з речовин, які гниють а останні в зоні населених місць - це найчастіше нечистоти. У значних концентраціях цей газ є в каналізаційних колекторах. Може бути він і у виробничих умовах при виготовленні коксу, при холодильному виробництві, де застосовується аміак. Людина відчуває присутність досить малих концентрацій аміаку в повітрі. При концентраціях 0,1 мг/л аміак викликає подразнення дихальних шляхів, при концентраціях більш високих (0,15-0,25 мг/л) спостерігається сильне подразнення кон'юнктиви очей, слизової носа, чхання, слинотеча, головний біль, потіння. При великих концентраціях (від 3,5 до 7,0 мг/л) настає смерть від набряку легень. У зовнішньому повітрі населених місць звичайно зустрічаються дуже незначні кількості аміаку - до 0,0025 мг/л. Ці концентрації нешкідливі, хоч і можуть бути відчутні на запах. При цих концентраціях аміак є показником забруднення повітря.
Сірководень - безбарвний газ із запахом тухлих яєць. Густина його- 1,19, тобто він важчий за повітря. Тому в колодязях і ямах, де він утворюється при гнитті, сірководень накопичується в нижніх шарах повітря. При малих концентраціях сірководень відчутний на запах, а при великих концентраціях запах майже не відчувається внаслідок ураження закінчень нюхових нервів у дихальних шляхах. Сірководень зустрічається й як продукт гниття в каналізаційних каналах, ямах, тунелях, а також на ряді виробництв, у лабораторіях, при сірчистому фарбуванні, де сірка може виділятися в повітря, відновлюючись до H2S, у виробництві шкіри, при видобуванні деяких сортів нафти, при виготовленні ультрамарину і в багатьох інших виробництвах, де застосовується сірка. При концентраціях більших за 1 мг/л настає блискавичне отруєння, людина відразу непритомніє і падає, як підкошена, може настати і смерть. Трохи менші концентрації (від 1 до 0,7 мг/л) теж небезпечні, однак при тривалішому вдиханні (близько години). Нюхом виявляються дуже малі концентрації-до 0,0028 мг/л. Санітарні норми обмежують концентрацію сірководню в повітрі населених місць у кількості 0,00015 мг/л.
Сірчистий газ (сірчистий ангідрид), SO2 ― безбарвний газ із різким задушливим запахом, добре розчиняється у воді, утворюючи сірчисту та сірчану кислоти. Належить до подразнюючих газів. Осаджуючись, пил і SO2, діють на людей, рослини, одяг і т. ін. Рослини можуть загинути навіть під дією незначних концентрацій сірчистого газу. Тому в повітрі міст не допускається більше за 0,25 мг/м3 сірчистого газу. Концентрації 20- 50 мг/м3 подразнюють гортань і кон'юнктиву ока. При деяких метеорологічних умовах сірчистий газ може завдавати великої шкоди людині і викликати масові захворювання і навіть смерть. Особливо сприяють нагромадженню в атмосфері шкідливих промислових газів, і зокрема SO2, тумани. Збільшення концентрації SO2 за наявності туманів призводить до підвищеної захворюваності і навіть смертності, особливо в людей із захворюваннями легень і серцево-судинної і системи, а також серед осіб літнього віку.
Концентрація пилу в атмосферному повітрі На неї впливають: метеорологічні процеси умови і характер викидів дисперсність пилового аерозолю Великодисперсний пил із частинками діаметром більшим за 10 мкм випадає швидко. Дрібнодисперсний пил із частинками діаметром меншим за 0,1 мкм практично не випадає.
Речовини, що містяться в атмосферному повітрі представлені: природним пилом штучним пилом Види природного пилу: космічний вулканічний земний морський пил лісових пожеж
Космічний пил Утворюється у світовому просторі в результаті згорання метеоритів. Вулканічний пил Здатний поширюватись на великі відстані, довго утримується у завислому стані, що може призвести до інтенсивного запилення атмосфери Морський пил Представлений кристалами солей, які утворюються внаслідок випаровування крапель води
Дослідженнями виявлено, що в 1 мл гірського і морського повітря міститься близько 1300-1800 пилинок, а в повітрі великого міста - до 130000. Пил зменшує прозорість атмосфери, особливо для ультрафіолетової частини сонячного спектру, змінює її здатність до розсіювання для сонячного проміння. Так, якщо прозорість атмосфери сільської місцевості Англії прийняти за 100%, то прозорість її в містах становить лише 25%. Пил сприяє утворенню хмарних днів, туманів і атмосферних опадів, бо кожна пилинка являє собою центр конденсації для водяної пари повітря.
При вибуху вулканів, особливо великих, з їх кратерів викидається (іноді на висоту 40-50 км) величезна кількість вулканічного пилу. Завдяки високому ступеню дисперсності цей пил надовго затримується в атмосфері і розвіюється на великі відстані. Вулканічний пил значно знижує прозорість атмосфери.
Морський (сольовий) пил утворюється в результаті випаровування краплинок морської води, що їх піднімають вітри. Тому не випадково морський вітер солоного присмаку.
Наземний пил може бути найрізноманітнішого походження, інтенсивності і шкідливості для організму. 1. Ґрунтовий, піщаний пил приноситься вітрами з пустель, степів та інших бідних на вологу місцевостей. Прикладом цього виду пилу можуть бути так звані "чорні бурі" на півдні України, яскраво описані в "Таврії" Олеся Гончара. До цього виду пилу належить і ліс о в и й пил або імла азіатських пустель і степів. 2. Пил від лісових і степових пожеж, коли як буревій мчать величезні маси попелу. 3. До наземного пилу належить і міський пил, що утворюється від руху транспорту по невпорядкованих вулицях, від вітрів, але особливо - від промислових підприємств, які викидають в атмосферу значні забруднення (теплоелектроцентралі, підприємства хімічної промисловості, заводи: коксохімічні, нафтоперегонні, цементні, гіпсові, вапняні, металургійні, особливо кольорової металургії). Значна кількість пилу утворюється і від залізничного транспорту.
Дисперсність пилу визначають за: його стійкістю до повітря фізико-хімічною активністю адсорбційною здатністю здатністю дифундувати чи затримуватись захисними мембранами
Власне пил (розмір частинок від 10 до 100 і більше мікрон). Такий пил не дифундує в повітрі та осаджується із зростаючою швидкістю, бо сила падіння частинок більша, ніж сила опору повітря. Цей пил видно неозброєним оком. Хмари і тумани (розмір частинок від 10 до 0,1 мікрона). Для цих пилинок сила падіння дорівнює силі опору повітря. Ці пилинки майже не дифундують у повітрі, осідають повільно і, в нерухомому повітрі, - з постійною швидкістю. Наприклад, якщо частинка сажі розміром в 1 мікрон буде викинута з димаря на висоту 30 м, то їй потрібно буде при повному безвітрі 11 -19 днів, щоб досягти поверхні землі. Такий пил можна спостерігати в прохідному сонячному світлі. В залі кінотеатру, який погано прибирають, завжди видно сніп світла від кінопроектора. Чим яскравіший цей сніп, тим більше пилу в залі. Дими - це пилинки завбільшки від 0,1 до 0,001 мікрона. Для таких пилинок сила падіння менша, ніж сила опору повітря, тому вони протягом тривалого часу лишаються завислими в повітрі. Вони здатні розсіюватися і дифундувати навіть у нерухомому повітрі, перебувають у стані броунівського руху.
За своєю природою пил може бути органічний (рослинний і тваринний), неорганічний (металевий, мінеральний) і мішаний. За місцем утворення розрізняють пил виробничий (промисловий і сільськогосподарський), ґрунтовий (в тому числі і вуличний пил міст) і побутовий (пил житлових і громадських приміщень). За формою пилових частинок пил поділяють на гострокінцевий (скляний, металевий), пил з тупими краями (цементний, крейдяний тощо), пил волокнистий ( пил від ганчір'я, бавовняний). За консистенцією розрізняють пил м'який (гіпс, сажа та ін.) і твердий (металевий, піщаний). За розчинністю пил поділяють на добре розчинний (цементний, борошняний, цукровий), слабо розчинний (глинистий, цегляний) і нерозчинний (вугільний, смолистий, кварцевий і ін.). За аналогією з колоїдними розчинами (золями) повітря із завислими в ньому частинками пилу розглядають як аерозоль, де повітря є дисперсним середовищем, а частинки пилу – дисперсною фазою.
Леткість пилу під впливом руху повітря прямо пропорційна квадрату радіусу пилинок. Чим більша питома вага пилу (при однаковому об'ємі пилинок), тим менша її леткість. Осадження пилу залежить ще від однієї його властивості - питомої поверхні пилу. Питома поверхня пилу - це відношення його поверхні до маси. З подрібненням пилу питома поверхня значно зростає. Чим більше роздроблення пилинки, тим більше звільняється міжмолекулярних сил і тим більша поверхнева активність пилу. Оскільки вільна поверхнева енергія прагне набути меншого значення, то частинки пилу виявляють здатність адсорбуватися одна на одній, що приводить їх до з'єднання в більші частинки, здатні до осідання (звичайно, коли відсутні інші фактори, які зберігають пил у стані дрібної дисперсності). З іншого боку, чим більша ця поверхнева енергія, тим більше виражена здатність частинок адсорбувати на собі гази, пару та іони.
Здатність пилу осідати з повітря залежить і від електричного заряду частинок, що його набувають вони або при роздрібненні і дробленні твердої речовини, або при стиканні пилу з якими-небудь поверхнями. Пилинки можуть набувати заряд також при стиканні їх між собою або під дією ультрафіолетового і космічного проміння. Завдяки заряду частинки можуть адсорбувати з повітря іони. Якщо частинки пилу адсорбують іони однойменного заряду, то їх стійкість у повітрі збільшується. Якщо ж частинки пилу адсорбують іони різного заряду, заряд самої пилинки зменшується, пилинки з'єднуються в більші частинки й осідають. Цілком очевидно, що частинки пилу, заряджені різнойменними зарядами, випадають швидше, ніж заряджені однойменними.
Дія пилу на організм може бути: а) механічною - поранення слизових очей, дихальних шляхів, епідермісу, закупорка вивідних протоків потових і сальних залоз шкіри тощо; б) загальнотоксичною - свинцевий, фтористий, миш'яковий; в) викликати місцеве подразнення - цементний, тютюновий пил; г) алергічною - прядив'яний, сінний, борошняний, урсоловий пил; д) канцерогенною - хромовий пил; е) інфікуючою - пил, що містить мікроорганізми (сибірка, туберкульоз); є) іонізуючою - радіоактивний пил.
Деяка кількість пилу (частинки розміром від 50 до мікрона проходить верхні дихальні шляхи і потрапляє у просвіт бронхів, де затримується на слизовій. Частинки діаметром менші за 0,3 мікрони потрапляють із вдихуваним повітрям у бронхіоли і альвеоли. Вказують, що пилові частинки розміром менші за 0,2 мікрона внаслідок своєї дуже незначної величини й інерції, яка дорівнює інерції молекул повітря, поводяться як молекули повітря, тому можуть видихатися назад. Однак, на думку М. А. Вігдорчика, такий пил також може частково затримуватися в легенях. Вважають, що пил з розміром частинок порядку 0,2-1 мікрон найбільше затримується в легенях і тому є найнебезпечнішим.
Залежно від природи пилу, що вдихають розрізняють такі види пневмоконіозів: а) силікоз – фіброз легень, викликаний пилом, що містить S02; б) антракоз, що спричиняється вугільним пилом; в) сидероз, що викликається вдиханням пилу, який містить окис заліза; г) азбестоз - азбестовим пилом; д) табакоз - тютюновим пилом; е) амілоз - борошняним пилом і т. ін.
Механізм розвитку силікозу можна уявити собі так. Проникаючи в легеню, пилинки спочатку викликають реактивний процес – пиловий альвеоліт. Вони фагоцитуються лейкоцитами, гістіоцитами. Частина пилинок і клітин з ними проникають у лімфатичні шляхи, де розвиваються запальні явища – відповіді у вигляді невеликих гранулем і деякого розростання фібробластичних сполучнотканинних елементів. Місцевий фіброз викликає порушення відтікання лімфи і стиснення альвеол, що призводить до їх ателектазу, до руйнування стінок і до виключення дихальної функції ділянок легеневої тканини. Подальше рубцювання призводить до утворення фіброзних або силікотичних вузликів у тканині легені. Зливаючись, ці вузлики утворюють пухлиноподібні ущільнення, в яких у дальшому розвиваються деструктивні зміни, розпад, що призводить до утворення порожнин, які нагадують туберкульозні каверни. При розпаданні вузликів вивільнюються кварцеві пилинки, які знову можуть бути захоплені новими клітинами, і процес відновлюється. Таким чином, розпочавшись, захворювання вже не припиняється, тобто є незворотним.
Різко зменшує запиленість зволоження матеріалу, що спричиняє пил (вологе буріння, обробка каменю). Величезне значення має раціонально влаштована вентиляція в цехах. Однак, зважаючи на неможливість 100% вловлювання промислових відходів, передбачено ряд заходів планувального характеру: 1) врахування рози вітрів (домінуючих вітрів) при плануванні міст і промислових підприємств; 2) влаштування санітарно-захисних зон - розривів між підприємствами і житловою зоною міста – протяжністю від 100 м до 1 км залежно від ступеня шкідливості відходів; 3) обов'язкове озеленення як санітарно-захисних зон, так і територій підприємств, вулиць, кварталів, дворів. Необхідно, щоб кожна ділянка вільної землі була вкрита зеленими насадженнями – деревами, кущами, травою. Величезна поверхня листя є природним фільтром, що затримує переважну частину пилу і газів із повітря. Це відбувається внаслідок фільтрації повітря через листя, а також через сповільнення його руху. Повітря зелених масивів багате на озон, що сприяє окисленню ряду газів (H2S, SO2, NH3). При озелененні необхідно висаджувати найбільш стійкі до пилу і газів зелені насадження (дуб, американський клен, білу акацію). Такі дерева як хвойні (ялина, сосна) і фруктові, дуже чутливі до пилу й газів і швидко уражаються; 4) обов'язковою умовою успішної боротьби з запиленістю повітря населених місць є брукування шляхів, вулиць і дворів, своєчасне й регулярне вологе прибирання та поливання вулиць і зелених насаджень в місті; 5) захист повітря закритих приміщень (житлових і громадських) від запиленості складається з проведення вологого прибирання, натирання підлог пилофіксуючими мастиками, регулярного провітрювання приміщень, особливо наскрізного, влаштування вентиляції і кондиціонування повітря, використання пилососів для видалення пилу з одягу, м'яких меблів, килимів, книжок та ін.
Основні токсичні речовини Оксиди сірки Оксиди азоту Оксиди вуглецю Оксиди і пил різного складу На процеси окислення впливають: ультрафіолетові промені присутність озону вологість повітря
Основні забруднювачі атмосферного повітря: промислові підприємства автотранспорт великі теплоелектростанції електростанції
Викиди автотранспорту містять: оксиди вуглецю озон оксиданти свинець сажу Концентрація оксиду вуглецю в атмосферному повітрі великих міст залежить від: інтенсивності руху ширини вулиць озеленення плану міста та ін.
Об’єми викидів в атмосферу промисловість чорної металургії – 24% промисловість кольорової металургії – 10% теплоелектростанції та електростанції – 27% У результаті згорання палива в повітря викидаються: летуча зола сажа різноманітні газоподібні продукти
Викиди в атмосферу СРСР США промисловість транспорт енергетика інше 60% 17% 13% 60% 27% 14% 9% 1989 рік
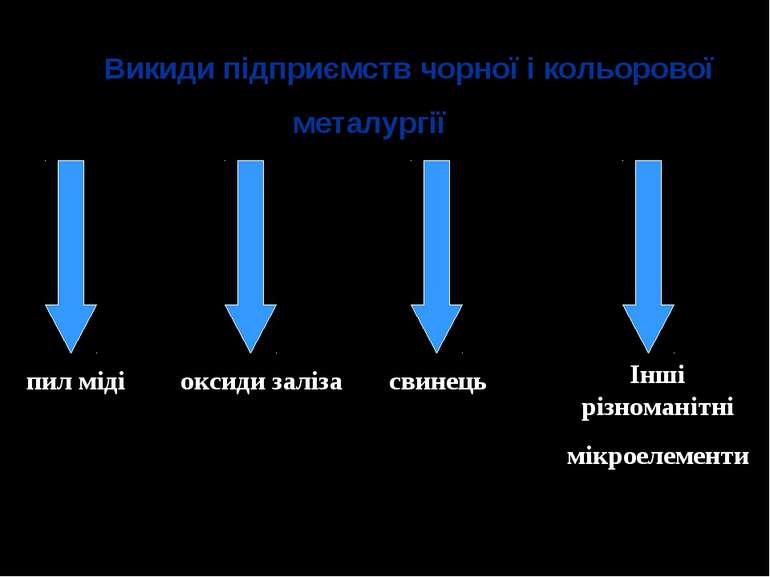
Викиди підприємств чорної і кольорової металургії пил міді оксиди заліза свинець Інші різноманітні мікроелементи
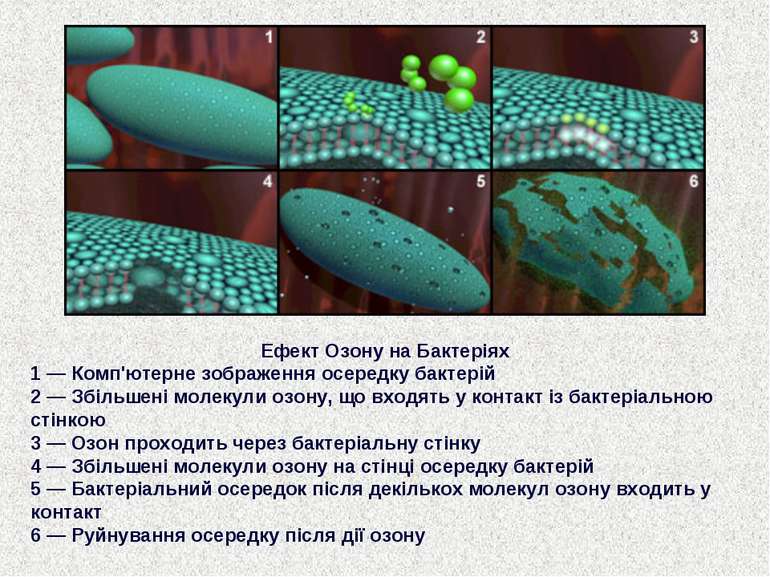
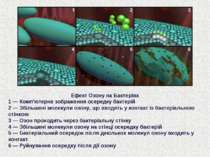
Ефект Озону на Бактеріях 1 ― Комп'ютерне зображення осередку бактерій 2 ― Збільшені молекули озону, що входять у контакт із бактеріальною стінкою 3 ― Озон проходить через бактеріальну стінку 4 ― Збільшені молекули озону на стінці осередку бактерій 5 ― Бактеріальний осередок після декількох молекул озону входить у контакт 6 ― Руйнування осередку після дії озону
Схожі презентації
Категорії