Презентація на тему:
Фізико-хімічна сутність процесу розчинення. Теплові явища, що супроводжують розчинення речовин
Завантажити презентацію
Фізико-хімічна сутність процесу розчинення. Теплові явища, що супроводжують розчинення речовин
Завантажити презентаціюПрезентація по слайдам:
Фізико-хімічна сутність процесу розчинення. Теплові явища, що супроводжують розчинення речовин
Запитання: Назвіть компоненти розчину. На які групи поділяються розчини за розміром часток розчиненої речовини? Який із компонентів розчину прийнято вважати розчинником для істинних розчинів? Що таке розчинність?
Які розчини називаються насиченими? Які розчини називаються ненасиченими? Які фактори впливають на процес розчинення? Подумайте й зі свого досвіду наведіть явища, що супроводжують процес розчинення.
Розчинення — фізико-хімічний процес. Демонстрація 1а У склянку з водою зануримо кілька кристалів калій перманганату. Розглянемо, що відбувається з кристалами. Які явища супроводжують цей процес? Відбувається руйнування кристалічної ґратки твердих речовин до молекул. Відбувається процес розподілу молекул розчиненої речовини між молекулами розчинника (дифузія).
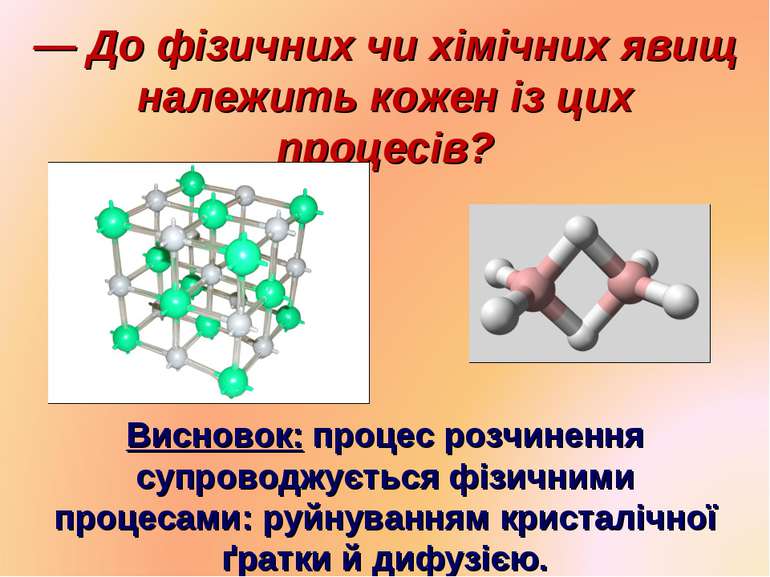
— До фізичних чи хімічних явищ належить кожен із цих процесів? Висновок: процес розчинення супроводжується фізичними процесами: руйнуванням кристалічної ґратки й дифузією.
Як прискорити цей процес? підігріти розчин (прискорюється руйнування й рух молекул); перемішати (прискорюється дифузія, молекули розчинника змивають з поверхні молекули розчинної речовини, відкривається доступ до наступних шарів).
Демонстрація 1б. Теплові явища під час розчинення У три хімічні склянки наливаємо приблизно по 25 мл води, у кожну занурюємо термометр і записуємо температуру. Потім у першу склянку додаємо приблизно 2,5 г натрій хлориду, акуратно перемішуємо, вимірюємо температуру.
У другу склянку додаємо приблизно 2,5 г амоній нітрату, перемішуємо, вимірюємо температуру. У третю склянку акуратно доливаємо приблизно 2,5 г концентрованої сульфатної кислоти, перемішуємо, нагадуємо учням правила роботи з кислотами, вимірюємо температуру.
— Чому змінилася температура розчину? Розчинення речовини супроводжується утворенням сполук між молекулами розчиненої речовини й розчинника. Цей процес називається сольватацією, якщо розчинником є вода — гідратацією. Висновок: розчинення — це складний фізико-хімічний процес.
Отже, які найпоширеніші процеси супроводжують розчинення? Чи можна вважати гідрати хімічними сполуками?
Кристалогідрати: CuSO4 ·5H2O — мідний купорос, CuSO4 — безводний; FeSO4 ·7H2O — залізний купорос, FeSO4 — безводний.
Солі деяких металів утворюють стійкі хімічні сполуки з певною кількістю молекул води — кристалогідрати. Гідратовані йони Cu2+, Fe2+, Na2+ та інші мають забарвлення. Кристалізаційну воду можна видалити з таких сполук лише тривалим прожарюванням за високих температур.
Кристалогідрати: Na2SO4·10H2O — глауберова сіль Na2CO3·10H2O — каустична сода CaCl2 ·6H2O MgSO4·7H2O ZnSO4·7H2O
Запитання: Чи можна стверджувати, що розчинення є лише фізичним або лише хімічним процесом? Які факти доводять, що розчинення — складний фізико-хімічний процес? Багато безводних солей, зокрема перелічені вище, з часом збіль-шуються в масі. Чому? Чи можна використовувати кристалогідрати для приготування розчинів?
Домашнє завдання Опрацювати матеріал параграфа, відповісти на запитання до нього, виконати вправи.
Схожі презентації
Категорії