Презентація на тему:
Предмет органічної хімії
Завантажити презентацію
Предмет органічної хімії
Завантажити презентаціюПрезентація по слайдам:
Презентація в 9 му класі учителя хімії КЗ Верхівцевського НВК Кукси Наталії Миколаївни. Предмет органічної хімії L/O/G/O
Мета: Дати загальну характеристику з основних питань: Органічні речовини Походження речовин Найважливіші характеристики ОС Основні положення теорії будови хімічних сполук. Класифікація ОС L/O/G/O
Блок №1 Цілі: Органічні речовини Походження речовин Найважливіші характеристики ОС Основні положення теорії будови хімічних сполук. Класифікація ОС L/O/G/O
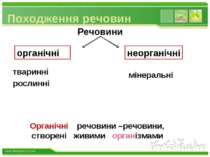
Походження речовин Речовини рослинні мінеральні органічні неорганічні речовини –речовини, створені живими організмами Органічні тваринні www.themegallery.com
Найважливіші характеристики ОС 1) Багатоманітністьсть ( близько 27 млн.) 2)До складу обов’язково входять (С) і (Н) – вуглеводні (ВВ) 3) Атоми в молекулі зв’язані ковалентним в’язком 4) Неелектроліти www.themegallery.com
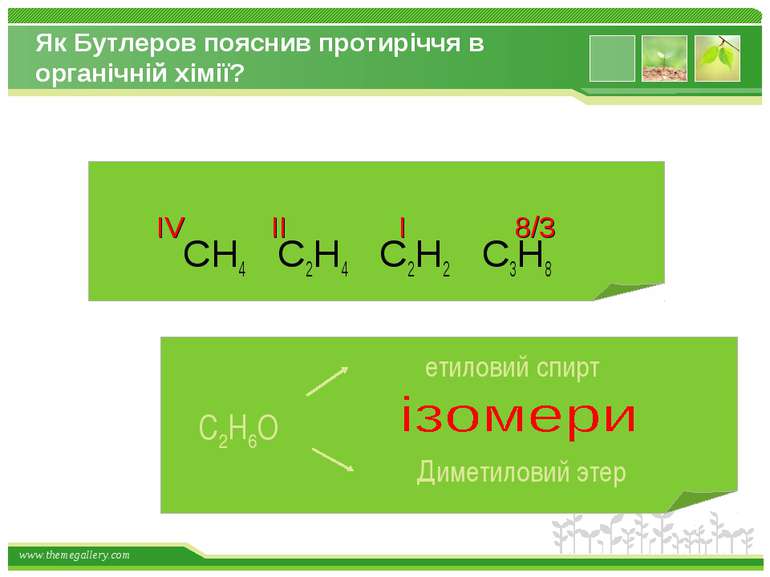
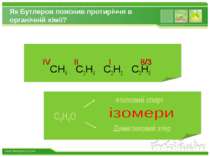
Як Бутлеров пояснив протиріччя в органічній хімії? CH4 C2H4 C2H2 C3H8 IV II I 8/3 www.themegallery.com
Бутлеров Олександр Михайлович (1828-1886) Російський хімік, академік Петербурзької АН (з 1874 р.). Творець теорії хімічної будови органічних сполук, що лежить в основі сучасної хімії. www.themegallery.com
Основні положення теорії будови хімічних сполук. 1. Атоми в молекулах з'єднуються в певному порядку відповідно до їх валентністю. (Carbon чотирьохвалентний). а) атоми чотиривалентного вуглецю можуть з'єднуватися один з одним, утворюючи різні ланцюги: відкриті нерозгалужені Відкриті розгалужені замкнуті б) порядок з'єднання атомів вуглецю в молекулах може бути різним і залежить від виду ковалентного хімічного зв'язку між атомами вуглецю - одинарним або кратним (подвійним і потрійним ): www.themegallery.com
Друге положення Властивості речовин залежать не тільки від їх якісного і кількісного складу, але і від їхньої будови молекул. Це положення пояснює явище ізомерії. Речовини, які мають однаковий склад, але різну хімічну або просторову будову, а отже, і різні властивості, називають ізомерами www.themegallery.com
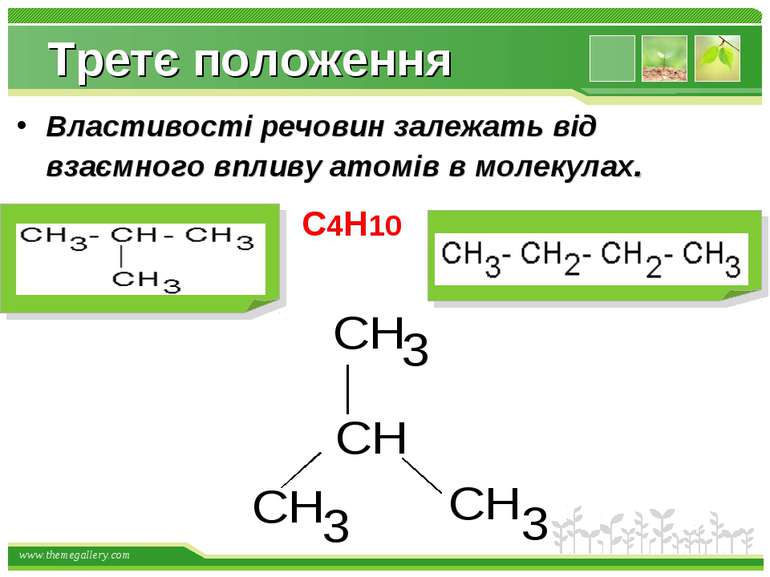
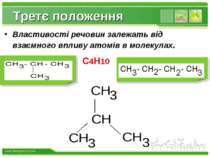
Третє положення Властивості речовин залежать від взаємного впливу атомів в молекулах. С4Н10 www.themegallery.com
Класифікація ОС Природні – утворені природнім шляхом, без втручання людини. мед нафта бавовна www.themegallery.com
Класифікація ОС Штучні – створює людина в лаборатортних умовах, схожі на природні речовини. хутро бензин шовк www.themegallery.com
Класифікація ОС Синтетичні –створює людина в лаборатортних умовах, подібних речовин в природі немає пральні порошки ліки пластмаса www.themegallery.com
Вуглеводні Цілі: Классифікація вуглеводнів Види сполучень атомів Карбону між собою Структурні формули органічних речовин Будова молекул Фізичні властивості Хімічні властивості Добування Застосування. www.themegallery.com
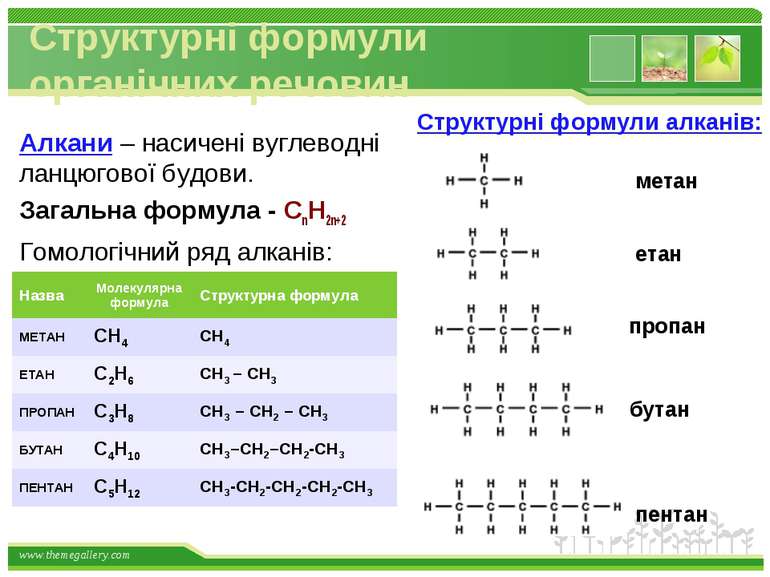
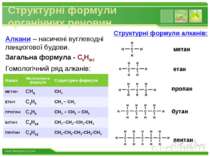
Структурні формули органічних речовин Алкани – насичені вуглеводні ланцюгової будови. Загальна формула - СnH2n+2 Гомологічний ряд алканів: метан етан пропан бутан пентан Структурні формули алканів: www.themegallery.com
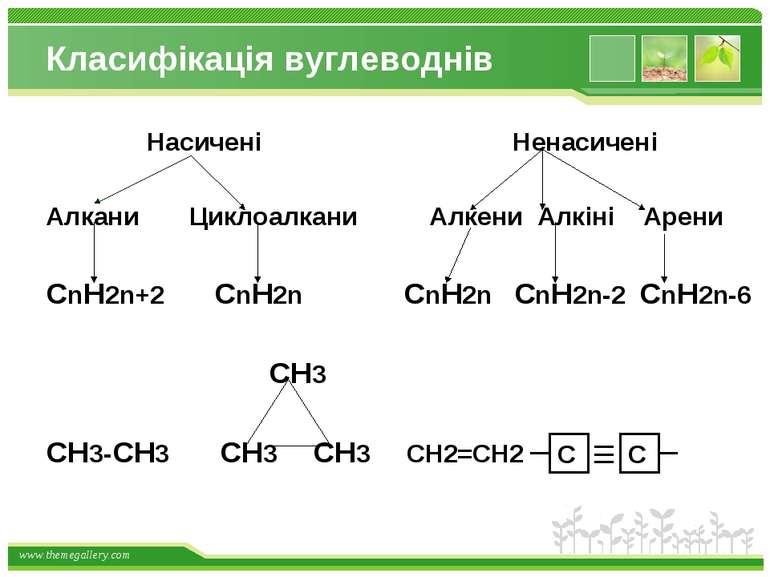
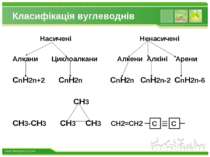
Класифікація вуглеводнів Насичені Ненасичені Алкани Циклоалкани Алкени Алкіні Арени CnH2n+2 CnH2n CnH2n CnH2n-2 CnH2n-6 CH3 CH3-CH3 CH3 CH3 CH2=CH2 www.themegallery.com
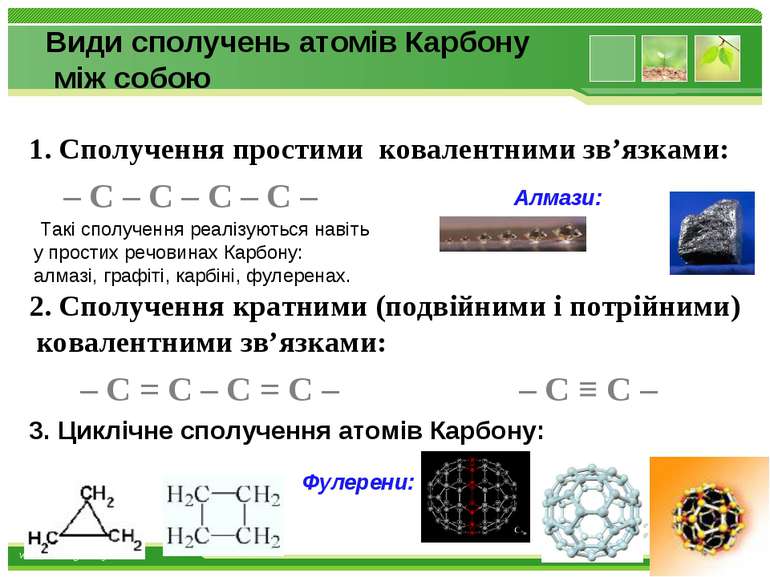
Види сполучень атомів Карбону між собою 1. Сполучення простими ковалентними зв’язками: – С – С – С – С – Такі сполучення реалізуються навіть у простих речовинах Карбону: алмазі, графіті, карбіні, фулеренах. 2. Сполучення кратними (подвійними і потрійними) ковалентними зв’язками: – С = С – С = С – – С ≡ С – 3. Циклічне сполучення атомів Карбону: Алмази: Фулерени: www.themegallery.com
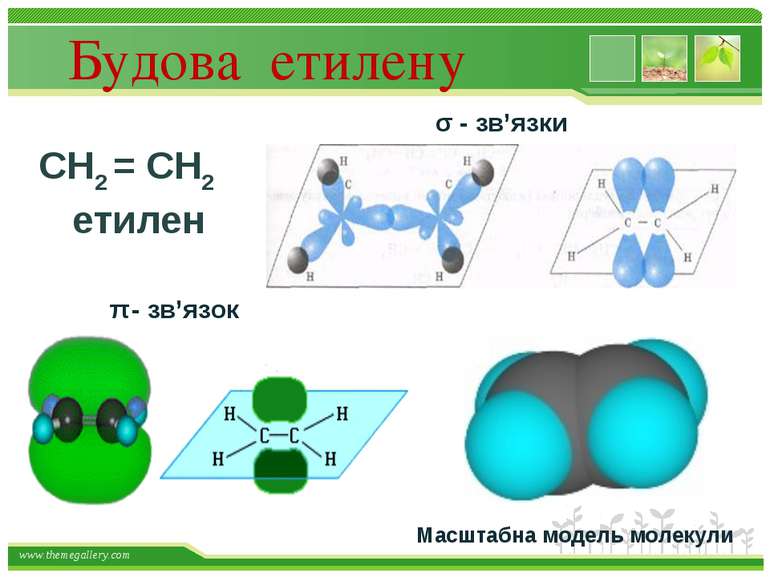
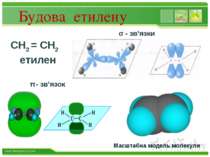
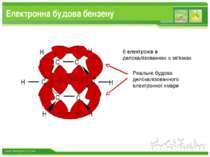
Будова етилену СН2 = СН2 етилен σ - зв’язки π - зв’язок Масштабна модель молекули www.themegallery.com
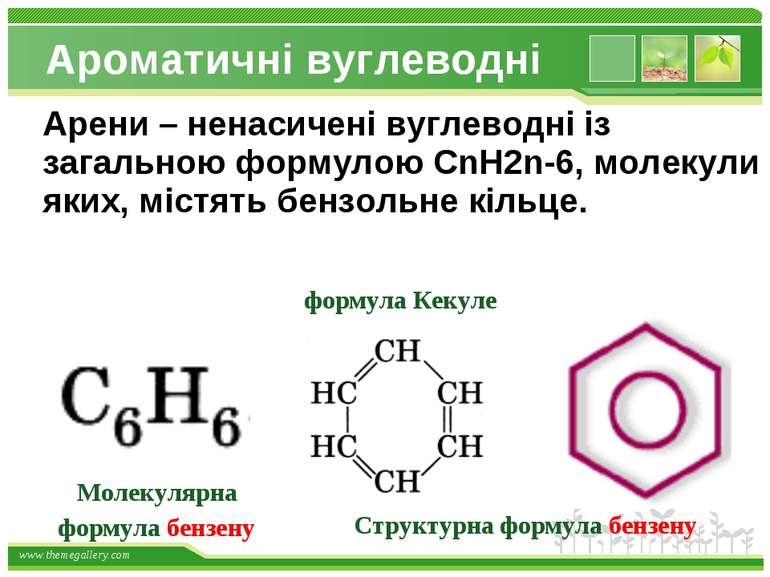
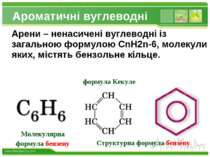
Ароматичні вуглеводні Структурна формула бензену Арени – ненасичені вуглеводні із загальною формулою CnH2n-6, молекули яких, містять бензольне кільце. Молекулярна формула бензену формула Кекуле www.themegallery.com
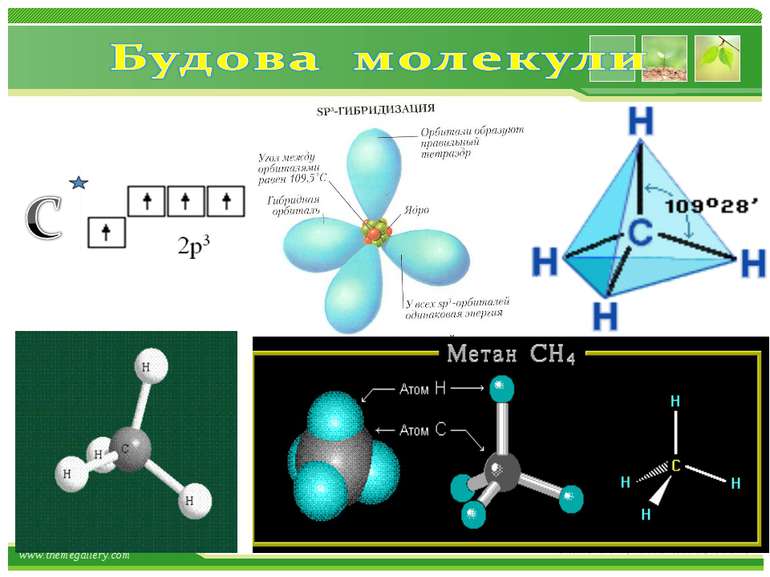
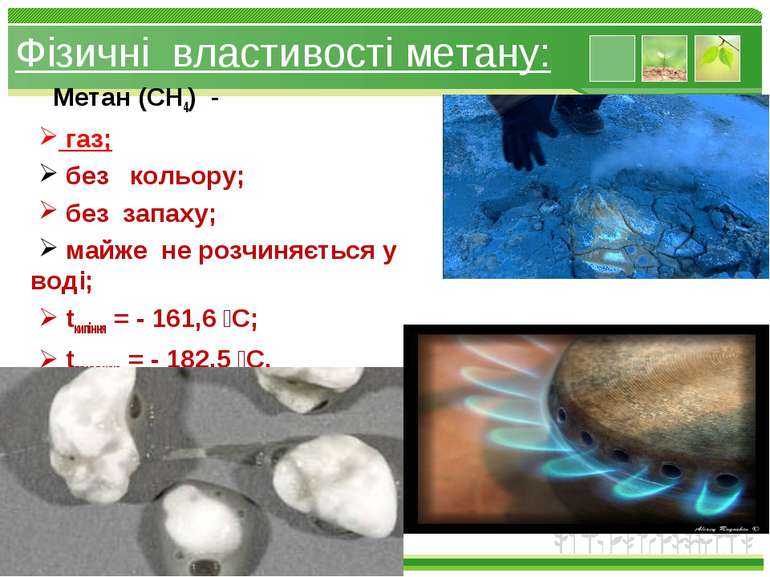
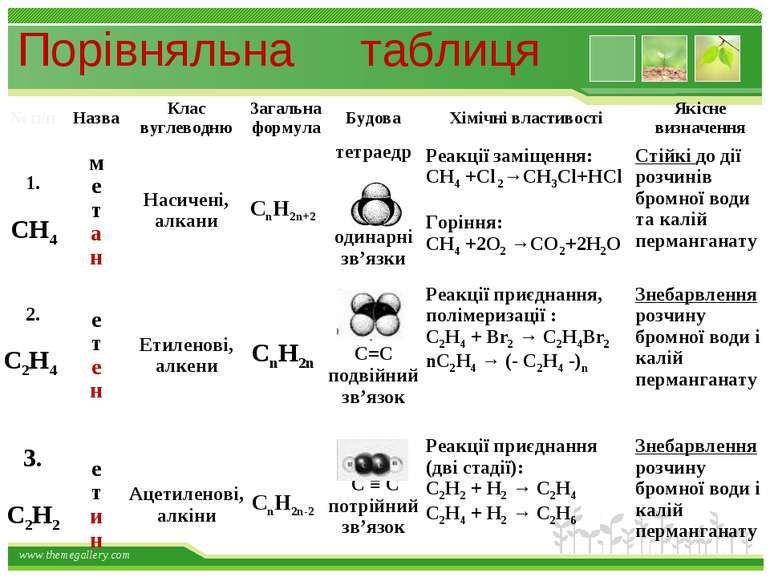
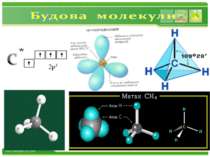
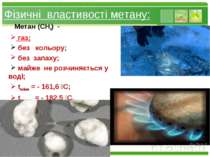
Фізичні властивості метану: Метан (СН4) - газ; без кольору; без запаху; майже не розчиняється у воді; tкипіння = - 161,6 С; tплавлення = - 182,5 С. www.themegallery.com
Фізичні властивості етилену С2Н4 безбарвний газ; добре розчинний в органічних розчинниках; tплавл = - 169,2 С; вибухонебезпечний www.themegallery.com
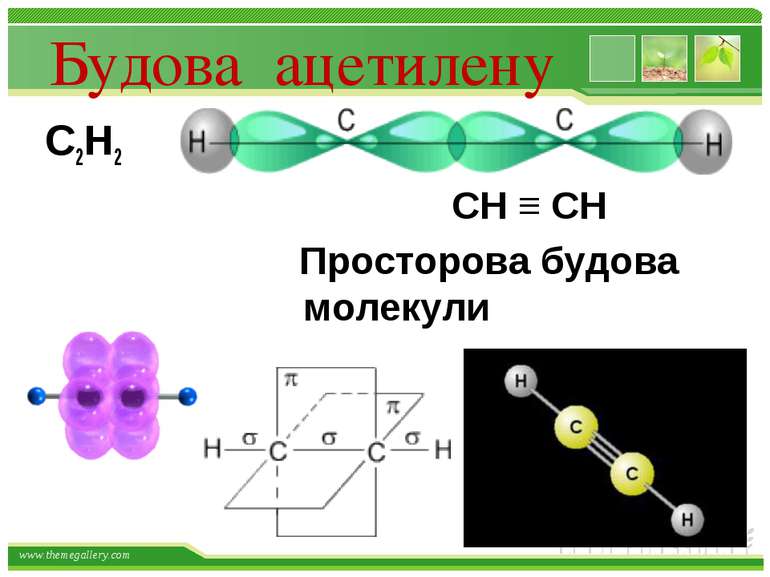
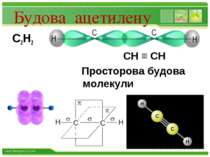
Фізичні властивості С2Н2 безбарвний газ; майже без запаху; малорозчинний у воді, але під тиском добре розчиняється у ацетоні; tкип = - 84 С; легший за повітря; вибухонебезпечний www.themegallery.com
Фізичні властивості бензену. безбарвна рідина, з різким характерним запахом, легше води, розчиняється у воді, розчинний в органічних розчинниках. Бензен токсичний, тому робота з ним в умовах школи неприпустима. www.themegallery.com
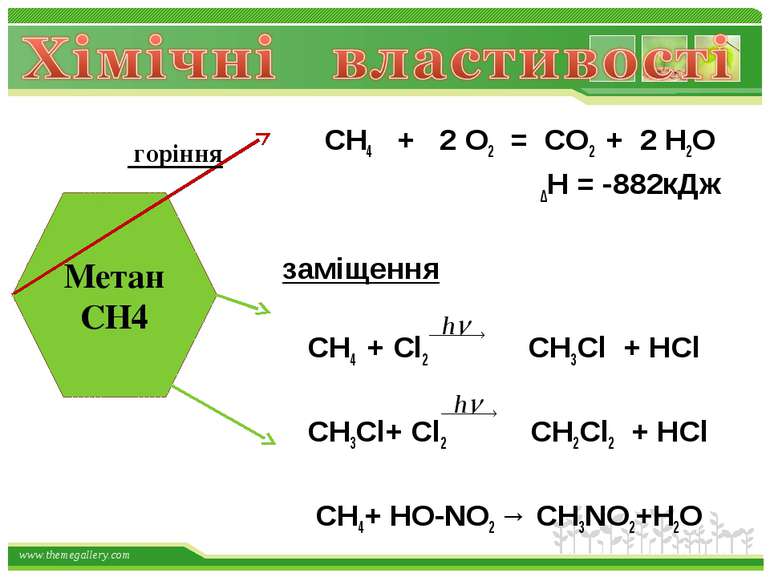
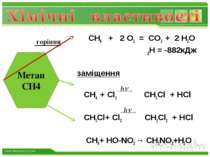
СН4 + 2 О2 = СО2 + 2 Н2О ∆Н = -882кДж заміщення СН4 + Cl2 СН3Cl + HCl СН3Cl+ Cl2 СН2Cl2 + HCl СН4+ HO-NO2 → СН3NO2+Н2О Метан СН4 горіння www.themegallery.com
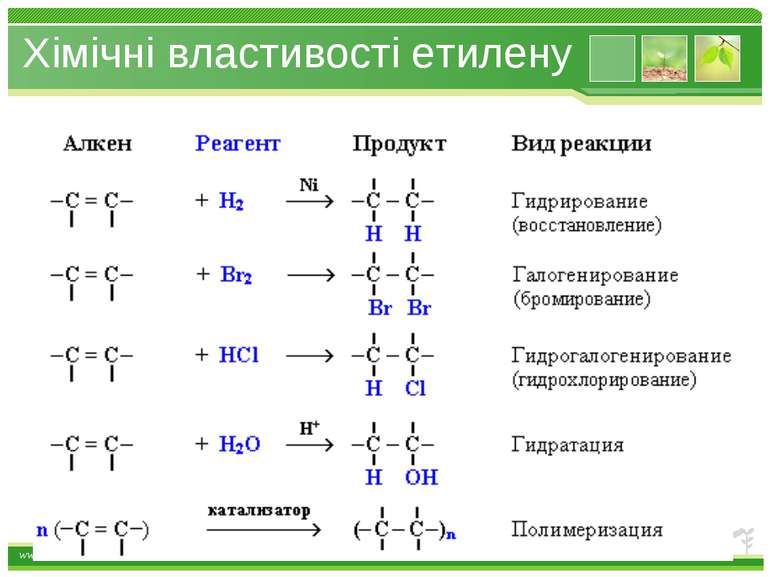
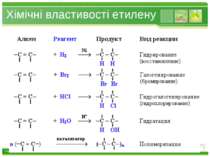
Хімічні властивості етилену Горіння (з виділенням великої кількості теплоти): С2Н4 + 3O2 → 2СО2 +2Н2О 2. Реакції приєднання по місцю розриву π - зв’язку: СН2 = СН2 а) гідрування - приєднання водню: С2Н4 + Н2→ С2Н6 б) галогенування - приєднання галогенів: С2Н4 + Br2 →С2Н4Br2 Якісне визначення ненасичених вуглеводнів - знебарвлення розчину калій перманганату і бромної води www.themegallery.com
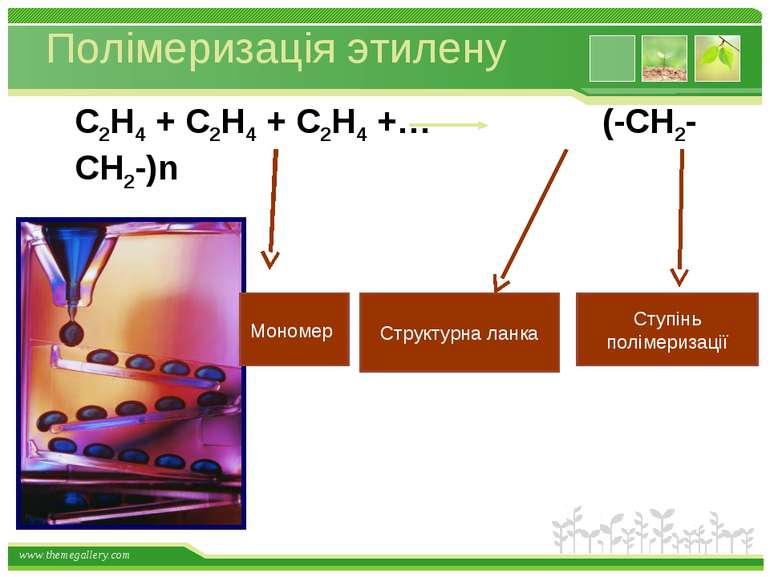
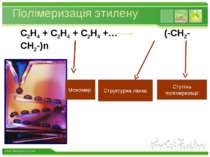
Полімеризація этилену С2Н4 + С2Н4 + С2Н4 +… (-СН2-СН2-)n Структурна ланка Ступінь полімеризації Мономер www.themegallery.com
Хімічні властивості ацетилену Горіння (яскравим кіптявим полум’ям): 2С2Н2 + 5O2 → 4СО2 +2Н2О 2. Реакції приєднання по місцю розриву π - зв’язків відбуваються у дві стадії а) гідрування (каталітичне): kat С2Н2 + Н2→ С2Н4 С2Н4 + Н2→ С2Н6 б) галогенування: С2Н2 + Cl2 → С2Н2 Cl2 (дихлороетен) С2Н2Cl 2 + Cl2 →С2Н2Cl4 (дихлороетан) Якісне визначення ненасичених вуглеводнів - знебарвлення бромної води та розчину калій перманганату. www.themegallery.com
Хімічні властивості бензену Бензен горить. Полум'я бензену кіптяве з за високого вмісту карбону в молекулі. Через особливсті будови молекули, бензен займає проміжне положення між алканами і алкенами, тобто може вступати в реакції приєднання і в реакції заміщення. www.themegallery.com
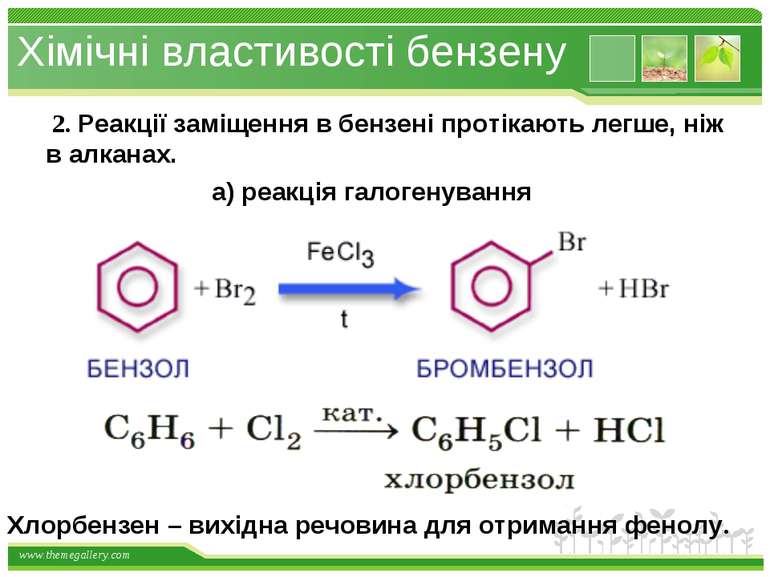
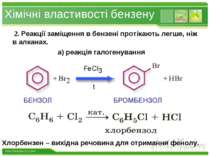
Хімічні властивості бензену 2. Реакції заміщення в бензені протікають легше, ніж в алканах. а) реакція галогенування Хлорбензен – вихідна речовина для отримання фенолу. www.themegallery.com
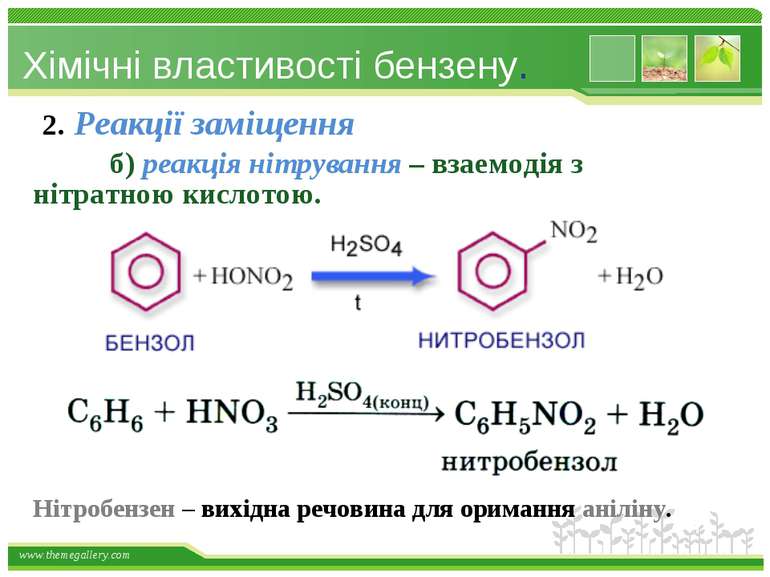
Хімічні властивості бензену. 2. Реакції заміщення б) реакція нітрування – взаемодія з нітратною кислотою. Нітробензен – вихідна речовина для оримання аніліну. www.themegallery.com
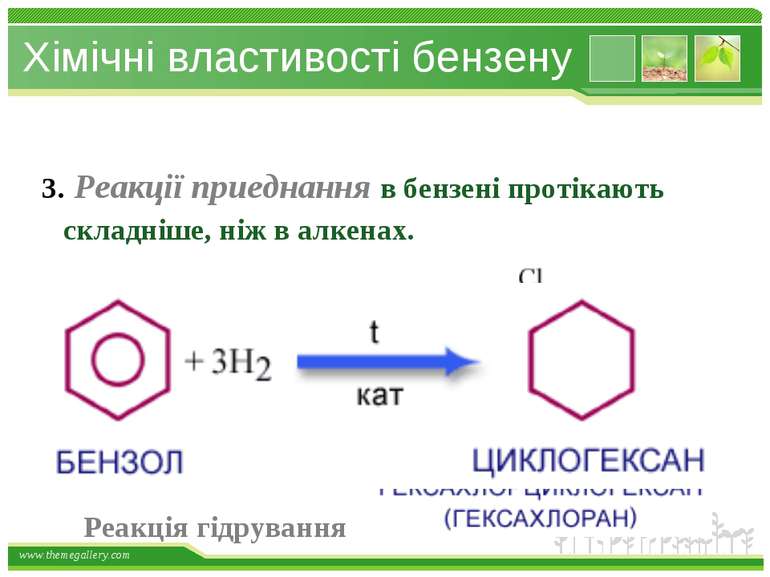
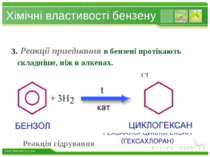
Хімічні властивості бензену 3. Реакції приеднання в бензені протікають складніше, ніж в алкенах. Реакція гідрування www.themegallery.com
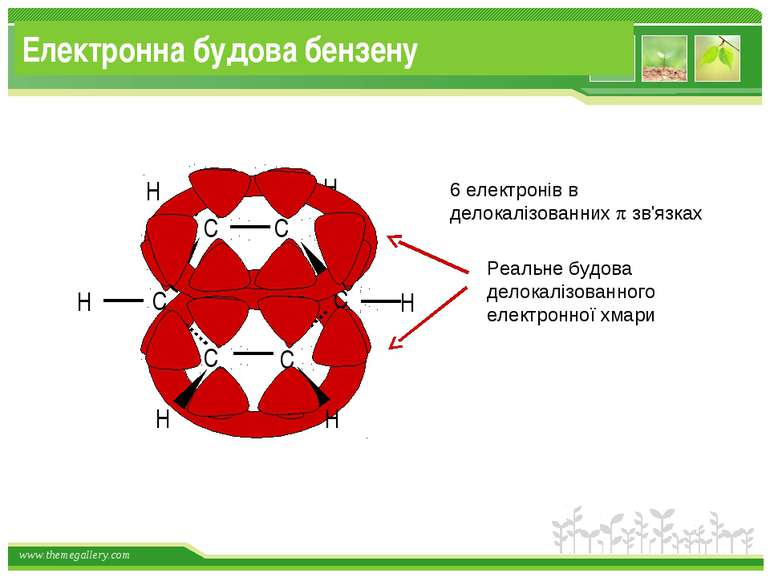
Хімічні властивості бензену Незважаючи на високу ненасиченість молекули бензену (за складом), він не дає характерних, якісних реакцій для ненасичених вуглеводнів: не знебарвлює бромну воду і розчин перманганату калію. Це пов'язано з особливою будовою молекули бензену. www.themegallery.com
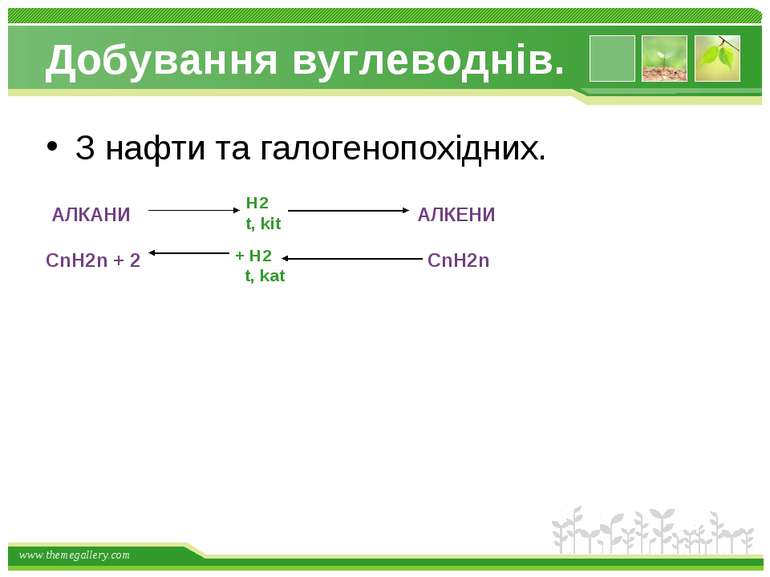
Добування вуглеводнів. З нафти та галогенопохідних. АЛКАНИ CnH2n + 2 АЛКЕНИ CnH2n H2 t, kit + H2 t, kat www.themegallery.com
Добування вуглеводнів. АЛКЕНИ - H2 t, kat АЛКІНИ СnH2n + H2 t, kat СnH2n-2 www.themegallery.com
Дбування бензену. Бензен є першим представником аренів. Його можна отримати трімерізаціей ацетилену. Бензен отримують при переробці кам'яного вугілля, а також при риформінгу бензинів з низьким октановим числом. www.themegallery.com
Застосування бензену 1-добавка до бензину; виробництво 2-розчинників; 3-ацетону; 4-аніліну; 5-фенолу; 6-пестицидів; 7-ліків; 8-фенолформальдегідних пластмас. www.themegallery.com
Схожі презентації
Категорії