Презентація на тему:
Бензен як представник ароматичних вуглеводнів
Завантажити презентацію
Бензен як представник ароматичних вуглеводнів
Завантажити презентаціюПрезентація по слайдам:
Запитання Опишіть, чим відрізняються sp3, sp2, sp-гібридизації. Дайте визначення: ковалентний зв’язок, σ-зв’язок, π-зв’язок.
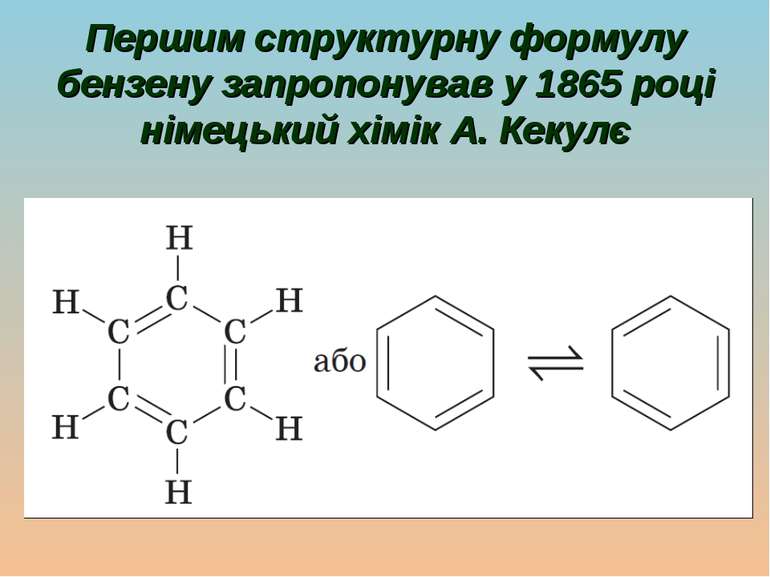
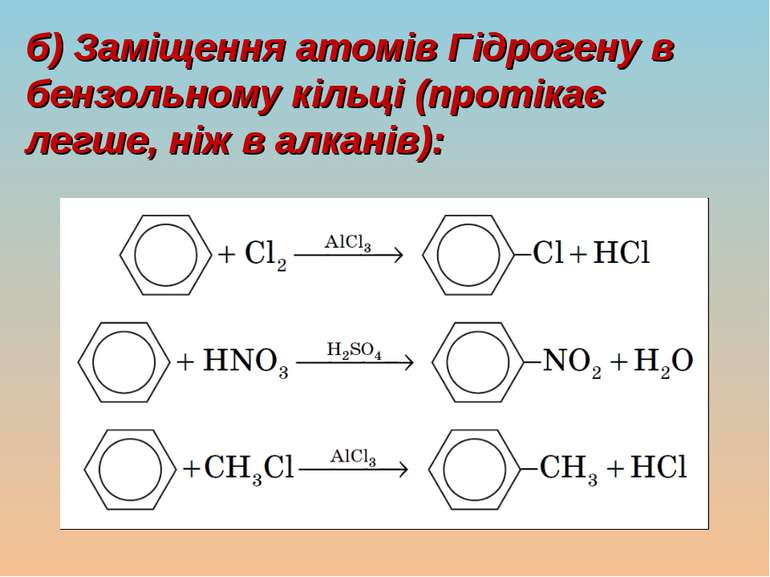
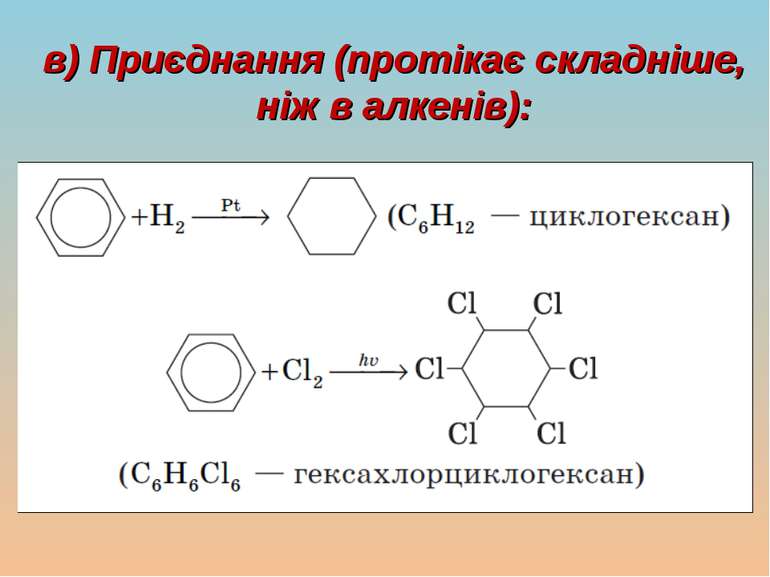
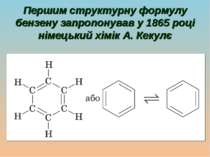
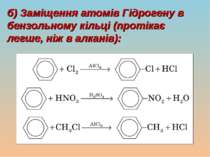
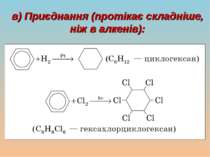
Молекулярна формула бензену — C6H6 Бензен мав своєрідний запах і проявляв дивні хімічні властивості. Незважаючи на свою «ненасиченість», бензен важко вступав у реакції приєднання, але легко давав реакції заміщення атомів Гідрогену. Тому бензен та його похідні виділили в спеціальний клас, якому дали назву «ароматичні вуглеводні», або «арени»
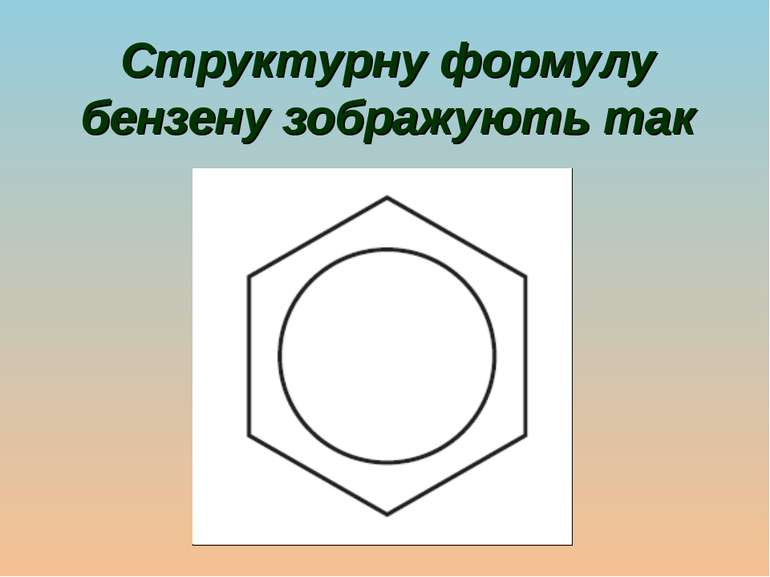
Молекула являє собою правильний плаский шестикутник. Усі зв’язки C − C однакові, а їх довжина не відповідає ні ординарному, ні подвійному зв’язку. Кути між зв’язками дорівнюють 120°. Атоми Карбону в молекулі бензену знаходяться у стані sp2-гібридизації, кожен атом утворює три σ-зв’язки й надає одну р-орбіталь для утворення сполученої системи із шести π-електронів.
Фізичні властивості бензену Рідина, без кольору, із запахом, tпл=5,5°С, tкип = 80°С, не розчиняється у воді, сам є чудовим неполярним розчинником.
Застосування бензену та його гомологів Отрутохімікати Розчинники Вибухові речовини Добавки до пального Органічний синтез, наприклад, одержання аніліну, фенолу, стиролу й полістиролу, лікарських препаратів
Домашнє завдання Повторити матеріал про вуглеводні, їх властивості, способи одержання, сфери використання.
Схожі презентації
Категорії