Презентація на тему:
"Молекулярна фізика"
Завантажити презентацію
"Молекулярна фізика"
Завантажити презентаціюПрезентація по слайдам:
Питання для опрацювання матеріалу Основні положення MKT та їх дослідне підтвердження. Що таке атом (молекула)? Що називається молярною масою? Що таке кількість речовини (одиниці виміру)? Дати визначення поняття концентрації; назвати числове значення сталої Авогадро. Що називається дифузією; броунівським рухом? Агрегатні стани речовини та їх пояснення з точки зору MKT (основні властивості). Швидкість молекул, дослід Штерна. Основне рівняння MKT; фізичний смисл рівняння. Температура, теплова рівновага; абсолютний нуль. Ідеальний газ; параметри, що характеризують ідеальний газ. Стала Больцмана; універсальна газова стала. Рівняння стану ідеального газу (Менделєєва-Клапейрона). Газові закони (ізопроцеси в газах); графіки, що характеризують закони. Прилади, що вимірюють параметри газів.
ОСНОВИ МОЛЕКУЛЯРНО-КІНЕТИЧНОЇ ТЕОРІЇ (MKT) Молекулярна фізика — розділ фізики, в якому вивчають фізичні властивості тіл у різних агрегатних станах на основі розгляду їх мікроскопічної (молекулярної) будови. Для опису використовують два основні методи: молекулярно-кінетичний (статистичний) і термодинамічний. Молекулярно-кінетичний метод ґрунтується на основі уявлень про частинки речовини, їх рух і взаємодію. Вчення називається MKT.
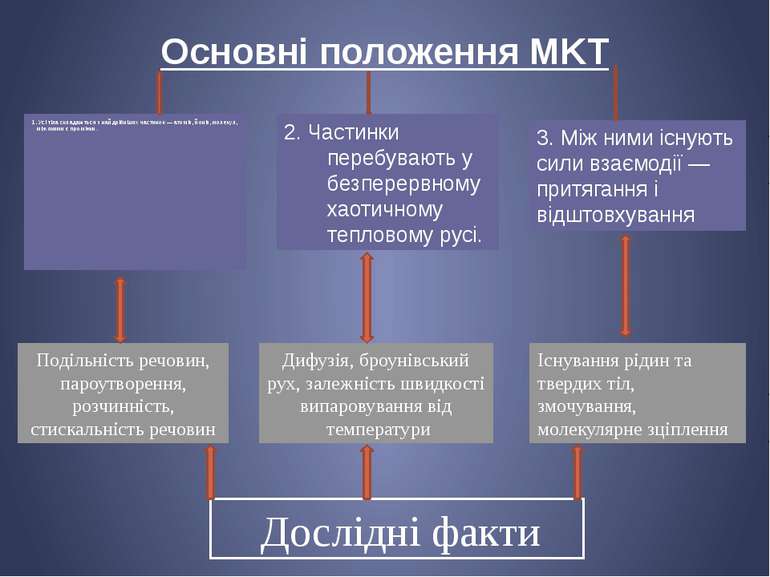
Основні положення MKT 1. Усі тіла складаються з найдрібніших частинок — атомів, йонів, молекул, між якими є проміжки. 2. Частинки перебувають у безперервному хаотичному тепловому русі. 3. Між ними існують сили взаємодії — притягання і відштовхування Подільність речовин, пароутворення, розчинність, стискальність речовин Дифузія, броунівський рух, залежність швидкості випаровування від температури Існування рідин та твердих тіл, змочування, молекулярне зціплення Дослідні факти
Дослідні обгрунтування положень MKT 1. а) молекули і атоми можна бачити в електронний та тунельний мікроскопи; б) наявність межі подрібнення речовини послідовним розведенням розчинів, при якій неможливо встановити наявність розчиненої речовини; в) утворення мономолекулярних плівок; г) змішування рідин, газів (1 л води + 1 л спирту < 2 л розчину); 2. а) Дифузія — явище проникнення молекул однієї речовини в міжмолекулярні проміжки іншої (підтверджує хаотичний рух молекул); б) броунівський рух — хаотичний рух макроскопічних частинок, завислих у рідині чи газі, зумовлений ударами з боку молекул («танець» пилинок в сонячному світлі); в) осмос — проникнення речовин через пористі перегородки (корені рослин, легені (100 м2 ), кишечник (5 м2)). 3. а) збереження форми та об'єму твердим тілом, об'єму — рідиною; б) виготовлення деталей методом порошкової металургії; в) для стискання чи пресування потрібна велика сила.
Агрегатні стани речовини та їх пояснення з точки зору MKT . Критерії Порівняння Речовини гази рідкі тверді Характер упакування частинок Частинкирозподілені повсьому наданому їм об'єму Дещобільш крихке упакування, ніжу кристалах Частинкищільно упаковані (кристалічнаґратка) Середнявідстань між молекулами Велика(-3,3нм) Мала(0,2-0,3нм) Дужемала (0,1нм) Сили зчеплення Дужемалі Дещоменші, ніжу твердому тілі Великі Основні властивості речовини а)Повністю заповнюють надані їм об'єми; б) легко змінюють свої об'єми та форму; в) легко перемішуються між собою в будь-яких пропорціях а) Заповнюютьлише нижню частину наданого їм об'єму; Б) текучі, тобто не зберігають свою форму; В) невсі рідини змішуються в будь-яких пропорціях а)Характерні стійкість форми та міцність; Б) незмінюють об'єм, але внаслідок деформації можуть змінити форму та об'єм; в) самовільно не перемішуються
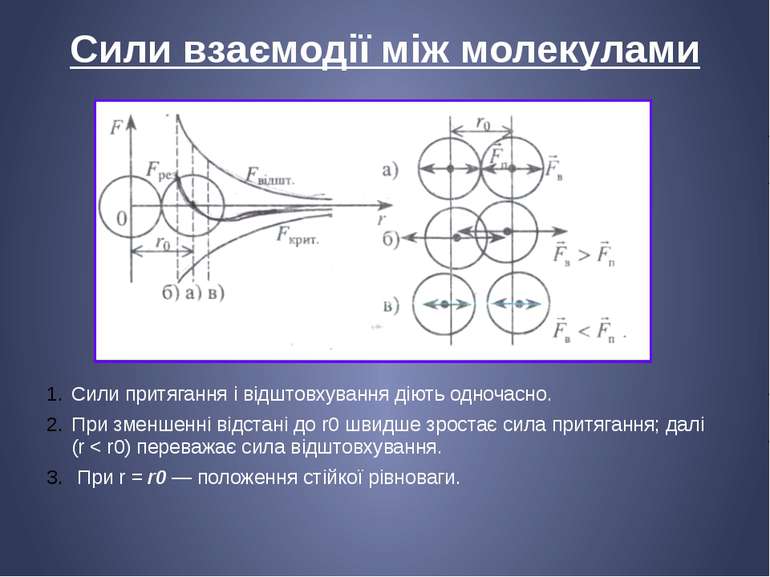
Сили взаємодії між молекулами Сили притягання і відштовхування діють одночасно. При зменшенні відстані до r0 швидше зростає сила притягання; далі (r < r0) переважає сила відштовхування. При r = r0 — положення стійкої рівноваги.
Основні поняття MKT Атом — це найменша частина хімічного елемента, яка є носієм його властивостей та не ділиться в процесі хімічних реакцій Молекула — це найменша стійка частинка речовини, яка має її основні хімічні властивості та складається з атомів одного (проста речовина) або кількох (складна речовина) хімічних елементів Примітка. Атоми можна розглядати як одноатомні молекули
3. Маси молекул і атомів (виражені в одиницях СІ) дуже маленькі, а тому незручні для користування. їх порівнюють з 1/12 тос = 1а.о.м. = 1,66∙10-27кг. Відносною молекулярною (або атомною масою) речовини називають відношення маси молекули (або атома) т0 даної речовини до 1/12маси атома вуглецю тос.
4. Розмір молекул дуже малий, тому їх кількість у макроскопічому тілі велика, що незручно. Тому використовують відносну кількість молекул, порівнюючи з 1 молем. Моль — це кількість речовини, в якій міститься стільки молекул чи атомів, скільки є атомів в 0,012 кг вуглецю. Незалежно від агрегатного стану, моль речовини містить одне і те ж число молекул N А = 6,02 • 1023 моль -1 (стала Авогадро). 5. Кількість речовини ν — це кількість молей, тобто відношення числа молекул (чи атомів) N у даному тілі до числа молекул (чи атомів) NА в 1 молі.
6. Молярна маса — фізична величина, що дорівнює відношенню маси речовини т до кількості речовини V. . Іншими словами, це маса речовини, взятої в кількості одного моля. Оскільки в 1 молі є NА молекул, то М = т0NА , M = Mr ∙10-3 кг/моль Авогадро встановив, що моль газу за нормальних умов займає об'єм
Схожі презентації
Категорії











![Концентрація молекул (n) — число молекул в одиниці об'єму. [n]=м⁻³ Концентрація молекул (n) — число молекул в одиниці об'єму. [n]=м⁻³](https://svitppt.com.ua/images/44/43629/770/img12.jpg)











![Концентрація молекул (n) — число молекул в одиниці об'єму. [n]=м⁻³ Концентрація молекул (n) — число молекул в одиниці об'єму. [n]=м⁻³](https://svitppt.com.ua/images/44/43629/210/img12.jpg)






















