Презентація на тему:
Сілікати
Завантажити презентацію
Сілікати
Завантажити презентаціюПрезентація по слайдам:
Силікатна кислота H2SiO3 - сполука кремнію, назву якої утворено від латинської назви елемента Silicium. Силікатна кислота дуже слабка. Вона слабша навіть за карбонатну кислоту. Силікатну кислоту можна одержати дією будь-якої кислоти на розчини силікату калію або натрію, наприклад: Na2SiO3 + 2HCl = H2SiO3↓ + 2NaCl При цьому вона виділяється у вигляді білого драглистого осаду, який містить значну кількість води. У воді H2SiO3 нерозчинна, але у подрібненому стані має властивість утворювати колоїдний розчин. При нагріванні силікатна кислота поступово зневоднюється, а при прожарюванні повністю втрачає воду і перетворюється на силікатний ангідрид SiO2.
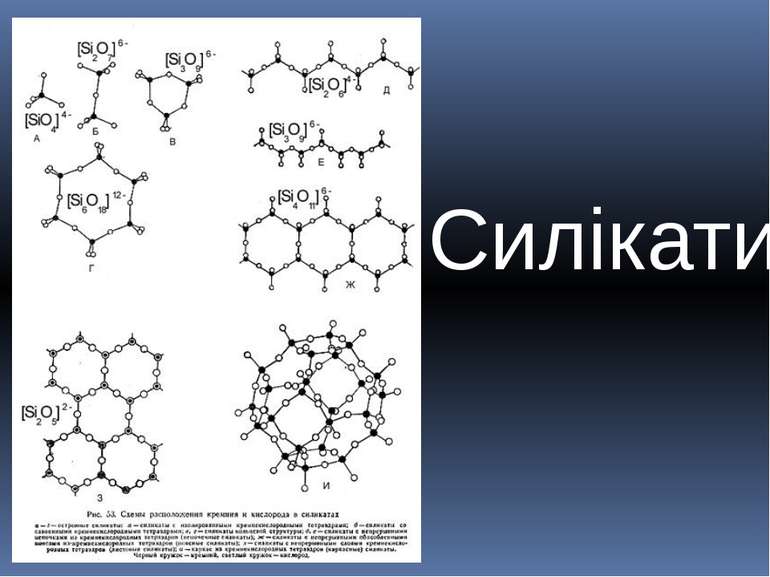
Взагалі силікатних кислот існує багато. Їх формули о записувати як сполуки силікатного ангідриду з водою, зв'язуючи формули крапкою. Наприклад, формулу метасилікатної кислоти H2SiO3 записують так: SiO2 • H2O. Формулу ортосилікатної кислоти H2SiO4 записують: SiO2 • 2H2O. Крім мета- і ортосилікатної кислоти існує багато так званих полісилікатних кислот, в молекулах яких міститься більше одної молекули силікатного ангідриду. Їх позначають такою загальною формулою: (SiO2)n • (H2O)m. Наприклад, H2Si2O5, або 2SiO2•H2O; H4Si3O8, або 3SiO2•2H2O; H2Si4O9, або 4SiO2•H2O і т. д. Солі силікатної кислоти називають силікатами, а полісилікатних - полісилікатами. Їх зазвичай зображують формулами окремих оксидів, що входять до складу полісилікату, зв'язуючи формули оксидів крапками в єдину формулу полісилікату: олівін - MgO•FeO•SiO2.
Силікати (і полісилікати) у воді нерозчинні, за винятком силікатів натрію Na2SiO3 і калію K2SiO3. Розчинне скло Силікати натрію і калію одержують сплавленням кремнезему з твердими лугами або з карбонатами калію і натрію: SiO2 + 2KOH = K2SiO3 + H2O ↑ SiO2 + Na2CO3 = Na2SiO3 + CO2 ↑ Одержувані при цьому сплавлені солі мають вигляд склоподібної маси. Тому силікати натрію і калію називають розчинним склом, а водні їх розчини — рідким склом. Розчинне скло додають до цементу і бетону, щоб зробити їх водонепроникливими. Ним просочують тканини і дерево для надання їм вогнестійкості. З розчинного скла виготовляють вогнестійкі замазки, силікатний клей тощо.
Природні сполуки силіцію Більшість природних сполук силіцію являють собою похідні полісилікатних кислот. Коли до складу полісилікатів входить алюміній, тоді їх називають алюмосилікатами. Більшість гірських порід складаються з алюмосилікатів. До найпростіших полісилікатів і алюмосилікатів належать азбест CaMg3Si4O12, або CaO • 3MgO • 4SiO2; польовий шпат (ортоклаз) K2Al2Si6O16, або K2O • Al2O3 • 6SiO2; каолін H4Al2Si2O9, або Al2O3 • 2SiO2 • 2H2O; калійна слюда H4K2Al6Si6O24, або K2O • 3Al2O3 • 6SiO2 • 2H2O. Природні силікати під впливом вологи і вуглекислого газу повітря повільно руйнуються (вивітрюються). Наприклад, розклад польового шпату (ортоклазу) схематично можна представити таким рівнянням: K2O • Al2O3 • 6SiO2 + CO2 + 2H2O = K2CO3 + Al2O3 • 2SiO2 • 2H2O + 4SiO2 Поташ вимивається водою, а каолін утворює глину з домішками піску. Оскільки польовий шпат у природі дуже поширений, то і глина утворюється в дуже значних кількостях.
Схожі презентації
Категорії