Презентація на тему:
"Галогени"
Завантажити презентацію
"Галогени"
Завантажити презентаціюПрезентація по слайдам:
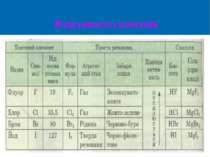
До галогенів належать Флуор F, Хлор СІ, Бром Вr, Йод І і Астат At. Це ще одна природна родина подібних за властивостями хімічних елементів
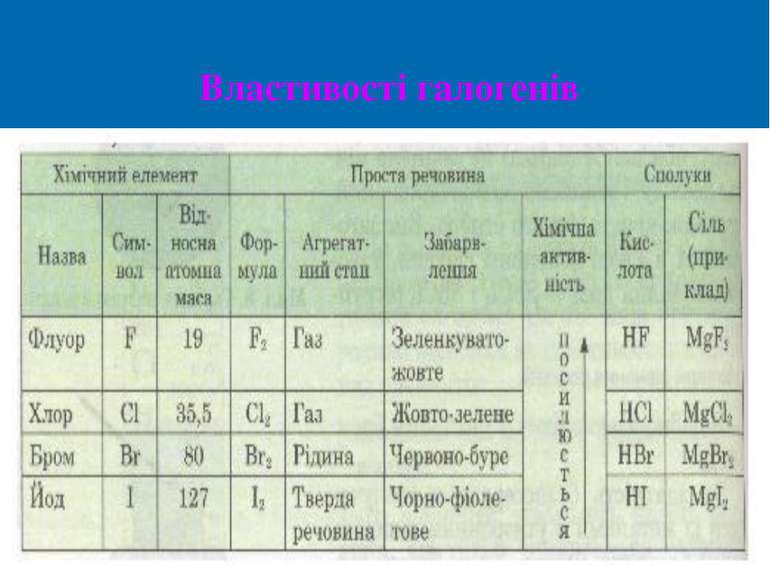
Галогени — найактивніші неметали Ці елементи утворюють прості речовини, які також називаються галогенами. Реагують майже з усіма простими речовинами, крім деяких неметалів. Всі галогени - енергійні окислювачі, тому зустрічаються в природі тільки у вигляді сполук.Вони являють собою типові неметали. За стандартних умов фтор F2 — газ, хлор Сl2 — газ, бром Вr2 — рідина, йод І2 — легкоплавка кристалічна речовина. За здатність безпосередньо сполучатись із металами з утворенням типових солей елементи Флуор, Хлор, Бром, Йод називають галогенами, що з грецької буквально означає «солеродні» (ті, що народжують солі).
Галогени взаємодіють з багатьма неметалами, у тім числі з воднем. Галогени — хімічно активні елементи, тому в природі вони трапляються лише у складі сполук, виявляючи валентність 1.Сполуки Брому та Йоду є у воді бурових свердловин, у воді морів та деяких озер, а також у морських водоростях Хоча активність галогенів при цьому різна, та склад продуктів реакції однаковий: утворюються газуваті сполуки — галогеноводні HF, НСl, НВг, НІ, водні розчини яких є кислотами
Історія відкриття флору У 1886 році французький хімік А. Муассан, використовуючи електроліз рідкого фтороводороду, охолодженого до температури, - 23°C(у рідині повинен міститися трохи фториду калію, який забезпечує її електропровідність), зміг на аноді отримати першу порцію нового, газу. У перших дослідах для Анрі отримання фтору Муассан використав Муассан дуже дорогий (1852 – 1907) електролізер, виготовлений з платини і іридію. При цьому кожен грам отриманого фтору " зїдав" до 6 г платини.
Історія відкриття хлору У 1774 році шведський вчений К. Шееле відкрив хлор, який прийняв за складну речовину і назвав "дефлогістированою соляною кислотою". У 1807 році англійський хімік Гемфрі Деві отримав той же газ. Він дійшов висновку, що отримав новий елемент і назвав його " хлорин"(від " хлорос" – жовто-зелений).У 1812 році Гей-Люсеок дав газу назву хлор.
Історія відкриття брому У 1825 році французький хімік А.Ж.Балар при вивченні маткових розсолів виділив темно-буру рідину, яку він назвав - " мурид"(від латинського слова muria, що означає " розсіл"). Комісія Академії, перевіривши це повідомлення, підтвердила відкриття Балара і запропонувала назвати елемент Антуан Жером бромом(від " бромос", з грецького " Балар смердючий"). (1802 – 1876)
Історія відкриття йоду У 1811 році французький хімік Бернар Куртуа відкрив йод шляхом перегонки маткових розчинів від свого азотнокислого кальцію з сірчаною кислотою. Щоб інші хіміки могли вивчати нову речовину, Б. Куртуа подарував його (правда, дуже невелику кількість) фармацевтичній фірмі в Дижоне.Бернар Куртуа У 1813 році він вивчив цей елемент і дав йому сучасну назву. Назва "йод" походить від грецького слова "йодес" - " фіолетовий" (за кольором).
Історія відкриття астату У 1869 р Д.І.Менделєєв передбачив його існування і можливість відкриття в майбутньому (як «ека-іод"). Вперше астат був отриманий штучно в 1940 р відкритий Д.Корсоном, К.Маккензі і Е.Сегре (Каліфорнійський університет у Берклі) . Для синтезу ізотопу 211At вони опромінювали вісмут альфа-частками. У 1943-1946 роках ізотопи астату були виявлені у складі природних радіоактивних рядів. Астат є найбільш рідкісним елементом серед усіх, виявлених в природі. У поверхневому шарі земної кори завтовшки 1,6 км міститься всього 70 мг астату.
Схожі презентації
Категорії