Презентація на тему:
Дослід Резерфорда. Ядерна модель атома
Завантажити презентацію
Дослід Резерфорда. Ядерна модель атома
Завантажити презентаціюПрезентація по слайдам:
Дослід Резерфорда. Ядерна модель атома Розділ V. АТОМНА І ЯДЕРНА ФІЗИКА Розробив викладач вищої категорії Старовижівського професійного ліцею Барчук Віктор Степанович
Джо зеф Джон То мсон (1856-1940) Англійський фізик, лауреат Нобелівської премії (1906) за заслуги в області теоретичних й експериментальних досліджень провідності електрики в газах, серед яких найважливіша — відкриття електрона, ізотопів і винаходу мас-спектрометра. Запропонував одну з перших моделей атома (пудинг з ізюмом). Позитивний заряд як би розмазаний всередині всього об'єму атома. В атом вкраплені окремі електрони, що нейтралізують позитивний заряд.
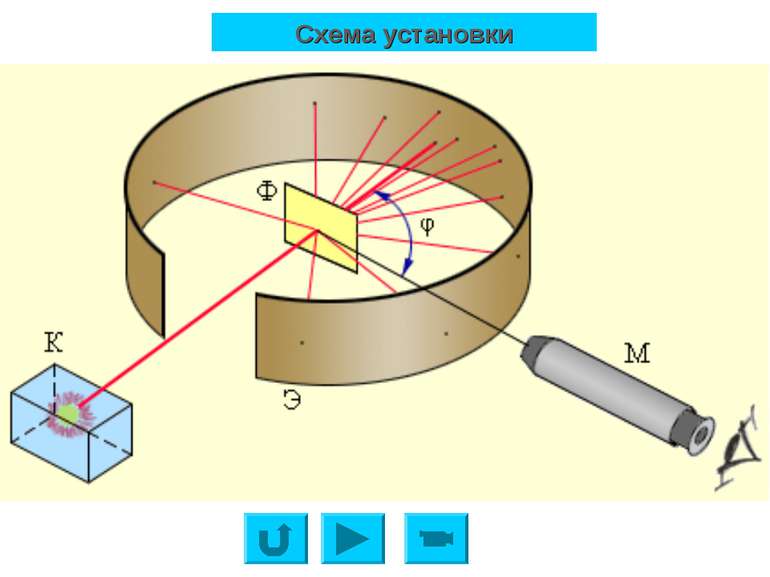
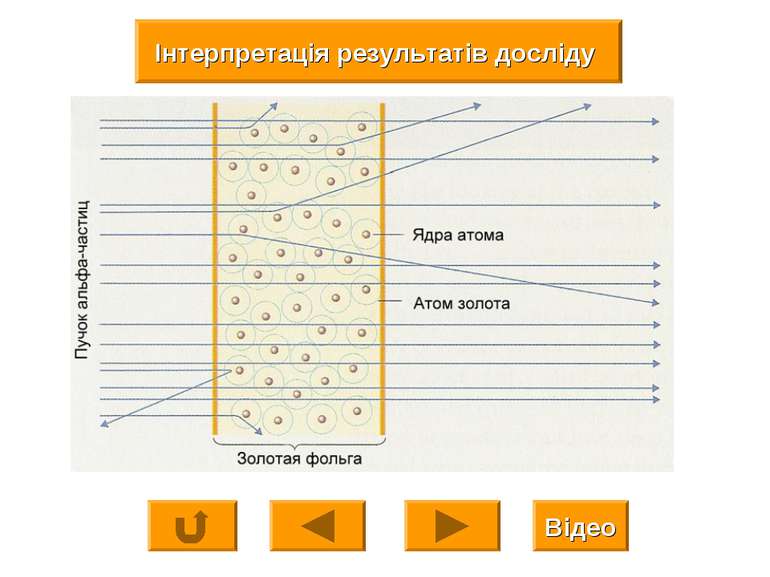
Ернест Резерфорд (1871-1937) Ерне ст Ре зерфорд британський фізик, лауреат Нобелівської премії з хімії (1908). Резерфорд відомий перед усім експериментами з розсіювання альфа-частинок (Резерфордівське розсіювання), завдяки якому він встановив структуру атома, як системи, що складається із малого за розмірами позитивно зарядженого ядра й електронів.
Демокріт Абдерський (грецькою: Δημόκριτος) (приблизно 460—370 pоки до н. е.) Давньогрецький філософ-матеріаліст, засновник атомістичної гіпотези пояснення світу. Демокріт розвинув вчення про атоми свого вчителя філософа Левкіппа, що є головним досягненням демокрітової філософії. Демокріт приходить до ідеї неподільних атомів, які можуть бути різної конфігурації: гачкоподібні, якореподібні, кутасті, вигнуті тощо. За Демокрітом фізичні атоми неподільні, але подумки в них можна виділити певні частини – точки, які не мають ваги і які не можна від атомів відторгнути. Це – уявна частина атома – „амера” (та, що не має частин).
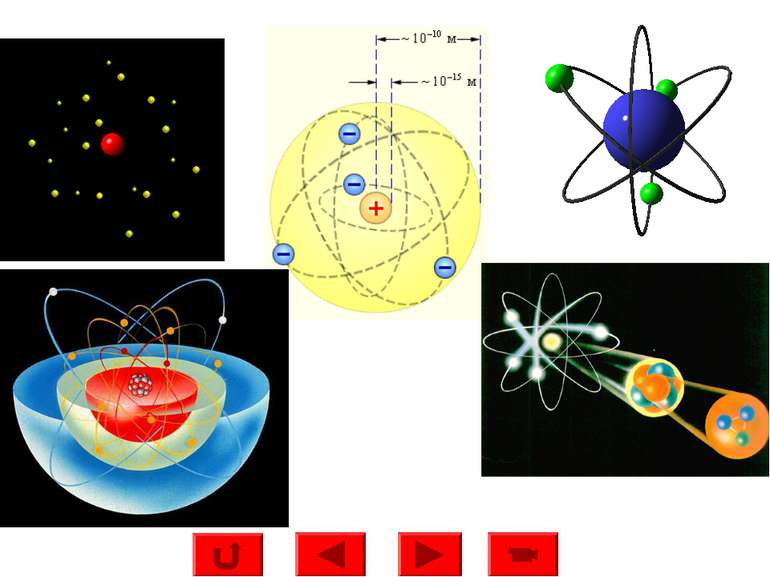
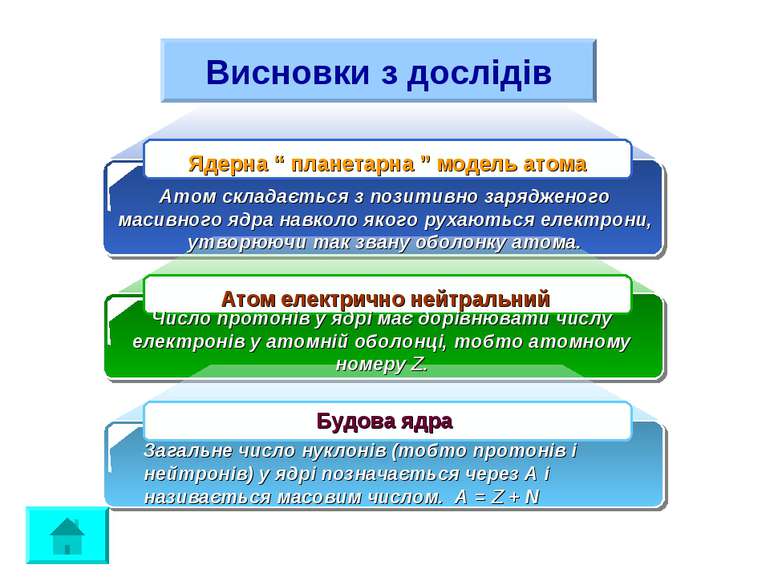
Атом складається з позитивно зарядженого масивного ядра навколо якого рухаються електрони, утворюючи так звану оболонку атома. Число протонів у ядрі має дорівнювати числу електронів у атомній оболонці, тобто атомному номеру Z. Загальне число нуклонів (тобто протонів і нейтронів) у ядрі позначається через А і називається масовим числом. А = Z + N Ядерна “ планетарна ” модель атома Атом електрично нейтральний Будова ядра Висновки з дослідів
Схожі презентації
Категорії