Презентація на тему:
"Вуглеводні"
Завантажити презентацію
"Вуглеводні"
Завантажити презентаціюПрезентація по слайдам:
Вуглеводні. Насичені, ненасичені та ароматичні вуглеводні: їх склад, будова, фізичні та хімічні властивості.
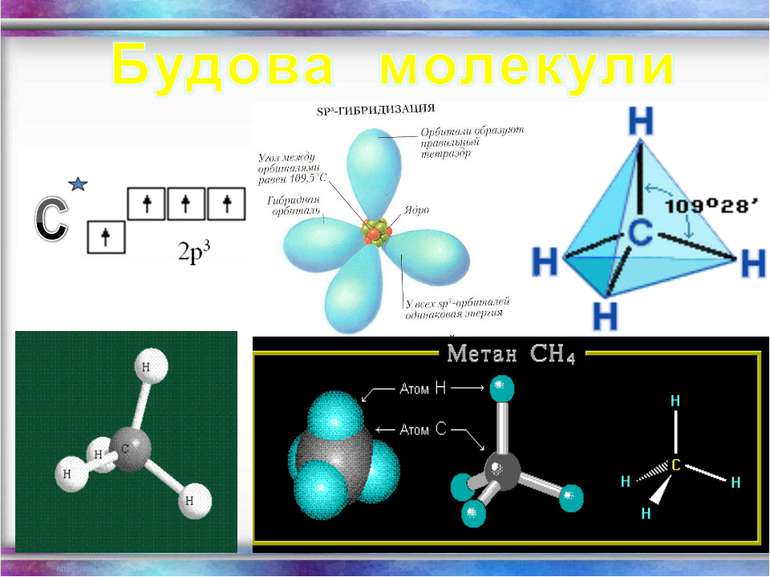
Види сполучень атомів Карбону між собою 1. Сполучення простими ковалентними зв’язками: – С – С – С – С – Такі сполучення реалізуються навіть у простих речовинах Карбону: алмазі, графіті, карбіні, фулеренах. 2. Сполучення кратними (подвійними і потрійними) ковалентними зв’язками: – С = С – С = С – – С ≡ С – 3. Циклічне сполучення атомів Карбону: Алмази: Фулерени:
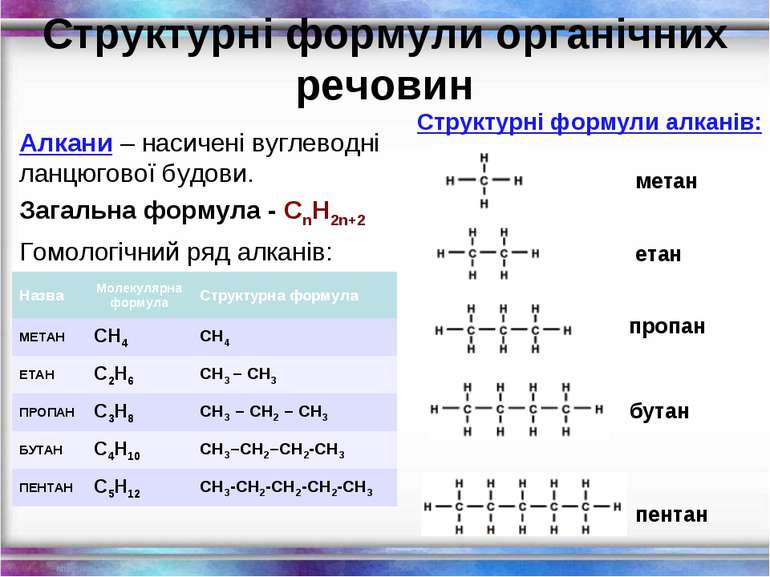
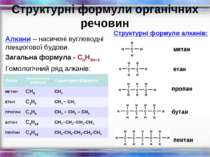
Структурні формули органічних речовин Алкани – насичені вуглеводні ланцюгової будови. Загальна формула - СnH2n+2 Гомологічний ряд алканів: метан етан пропан бутан пентан Структурні формули алканів: Назва Молекулярна формула Структурна формула МЕТАН СН4 СН4 ЕТАН С2Н6 СН3 – СН3 ПРОПАН С3Н8 СН3 – СН2 – СН3 БУТАН С4Н10 СН3–СН2–СН2-СН3 ПЕНТАН С5Н12 СН3-СН2-СН2-СН2-СН3
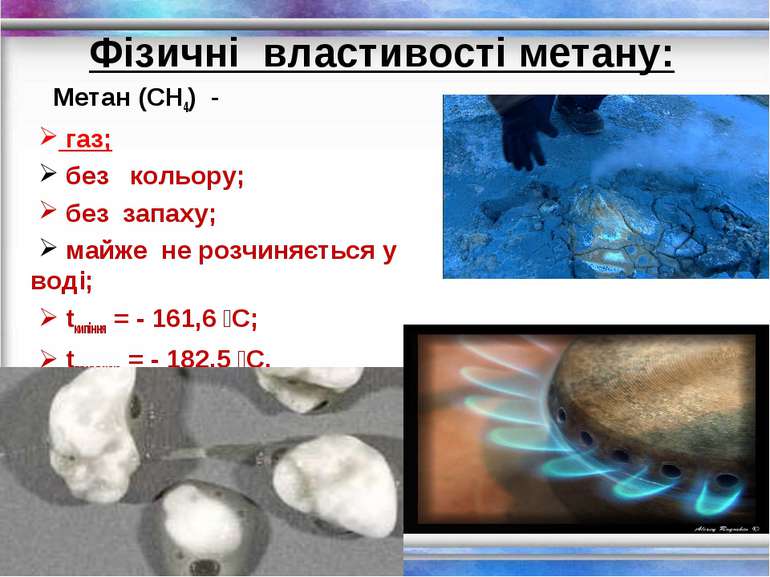
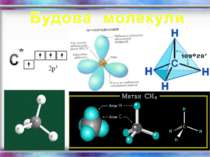
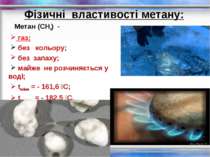
Фізичні властивості метану: Метан (СН4) - газ; без кольору; без запаху; майже не розчиняється у воді; tкипіння = - 161,6 С; tплавлення = - 182,5 С.
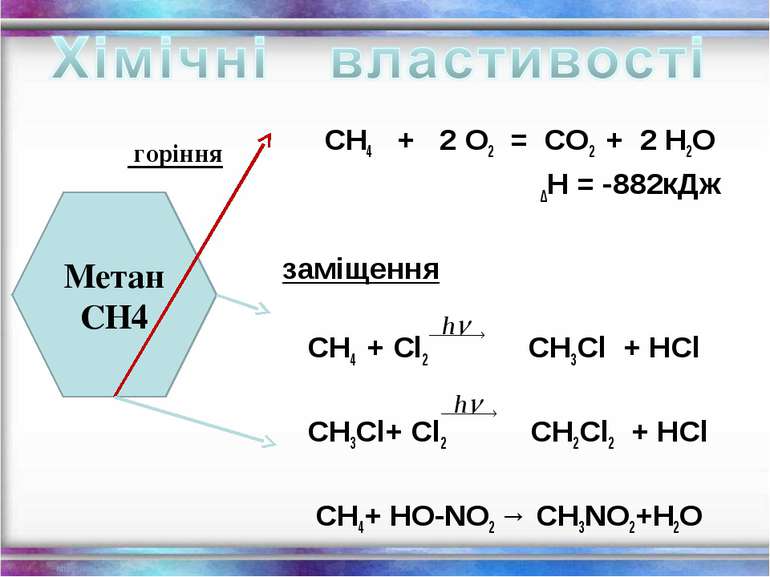
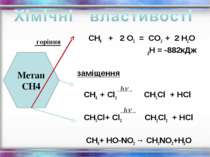
СН4 + 2 О2 = СО2 + 2 Н2О ∆Н = -882кДж заміщення СН4 + Cl2 СН3Cl + HCl СН3Cl+ Cl2 СН2Cl2 + HCl СН4+ HO-NO2 → СН3NO2+Н2О Метан СН4 горіння
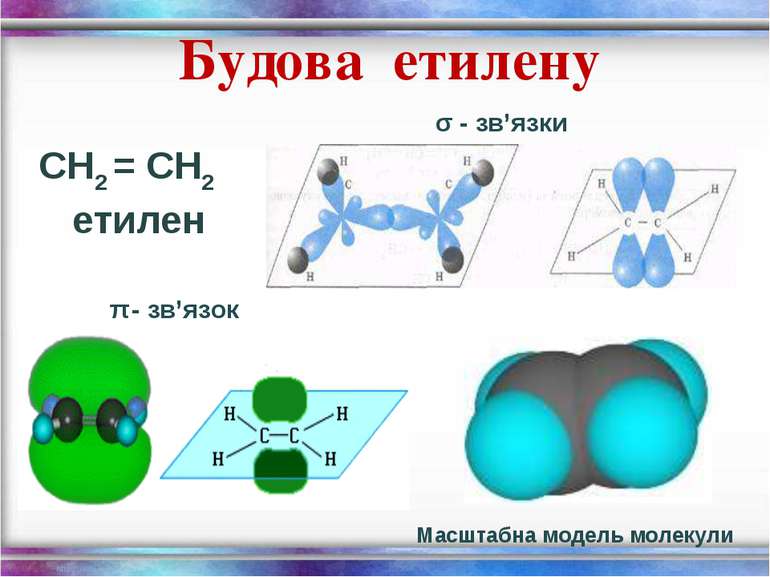
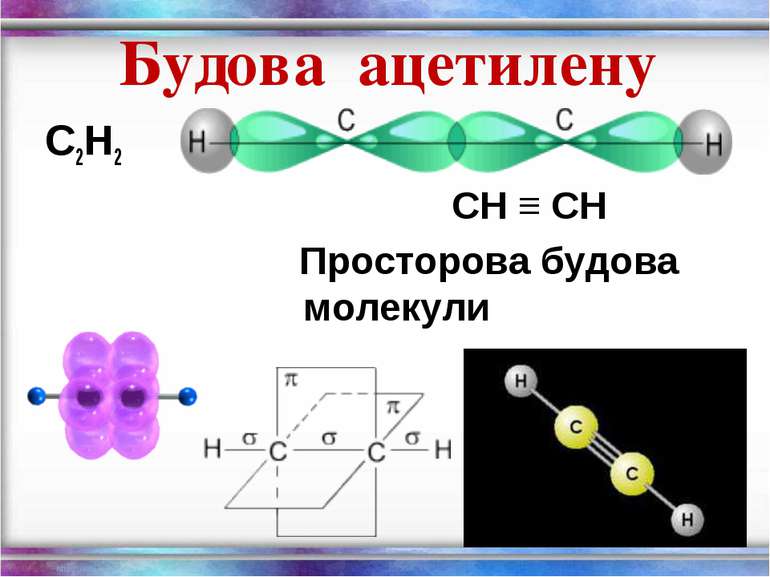
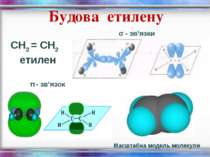
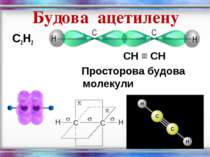
Ненасичені вуглеводні – органічні сполуки, що мають кратні зв’язки між атомами Карбону (подвійні – С = С – або потрійні – С Ξ С – ) Етиленові вуглеводні - органічні сполуки, що мають один подвійний зв’язок між атомами Карбону. Загальна формула СnH2n С2Н4 - етен (етилен) С3Н6 - пропен С4Н8 - бутен Ацетиленові вуглеводні - органічні сполуки, що мають один потрійний зв’язок між атомами Карбону. Загальна формула - СnH2n - 2 С2Н2 - етин (ацетилен) С3Н4 - пропін С4Н6 - бутин
Фізичні властивості етилену С2Н4 безбарвний газ; добре розчинний в органічних розчинниках; tплавл = - 169,2 С; вибухонебезпечний
Хімічні властивості етилену Горіння (з виділенням великої кількості теплоти): С2Н4 + 3O2 → 2СО2 +2Н2О 2. Реакції приєднання по місцю розриву π - зв’язку: СН2 = СН2 а) гідрування - приєднання водню: С2Н4 + Н2→ С2Н6 б) галогенування - приєднання галогенів: С2Н4 + Br2 →С2Н4Br2 Якісне визначення ненасичених вуглеводнів - знебарвлення розчину калій перманганату і бромної води
Фізичні властивості С2Н2 безбарвний газ; майже без запаху; малорозчинний у воді, але під тиском добре розчиняється у ацетоні; tкип = - 84 С; легший за повітря; вибухонебезпечний
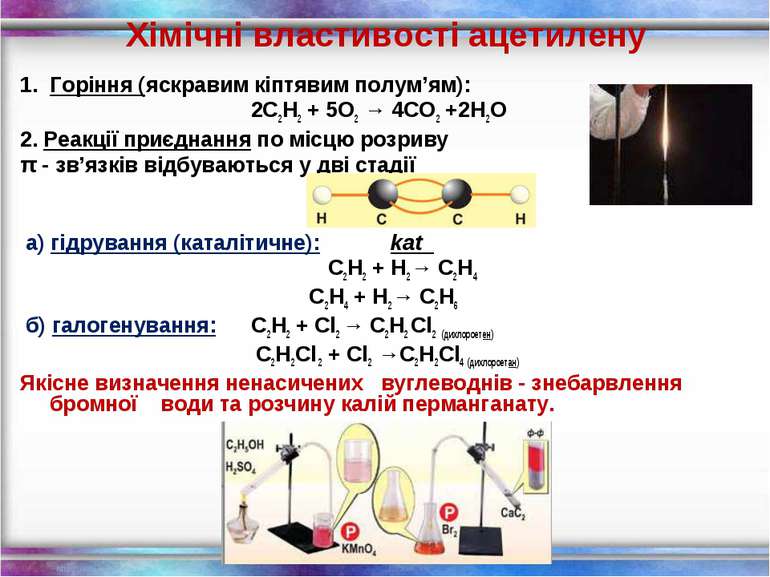
Хімічні властивості ацетилену Горіння (яскравим кіптявим полум’ям): 2С2Н2 + 5O2 → 4СО2 +2Н2О 2. Реакції приєднання по місцю розриву π - зв’язків відбуваються у дві стадії а) гідрування (каталітичне): kat С2Н2 + Н2→ С2Н4 С2Н4 + Н2→ С2Н6 б) галогенування: С2Н2 + Cl2 → С2Н2 Cl2 (дихлороетен) С2Н2Cl 2 + Cl2 →С2Н2Cl4 (дихлороетан) Якісне визначення ненасичених вуглеводнів - знебарвлення бромної води та розчину калій перманганату.
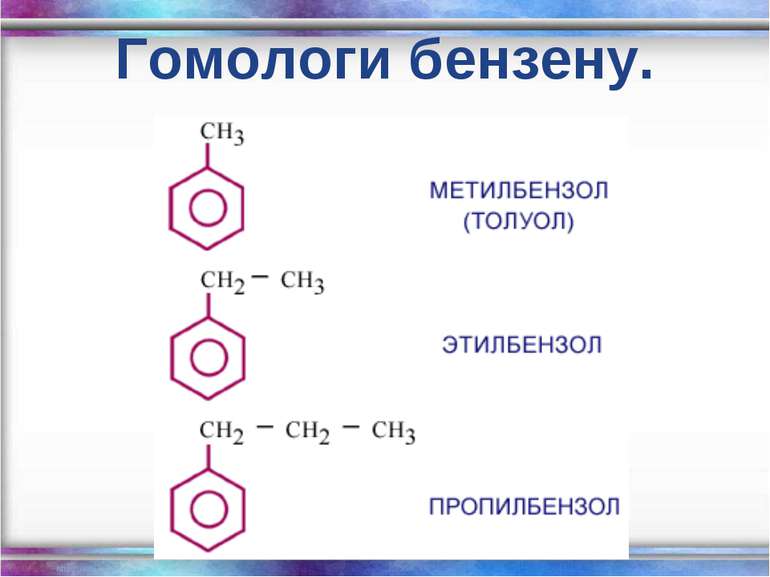
Структурна формула бензену Арени – ненасичені вуглеводні із загальною формулою CnH2n-6, молекули яких, містять бензольне кільце. Молекулярна формула бензену формула Кекуле Ароматичні вуглеводні
Фізичні властивості бензена. Бензен: безбарвна рідина, з різким характерним запахом, легше води, розчиняється у воді, розчинний в органічних розчинниках. Бензен токсичний, тому робота з ним в умовах школи неприпустима.
Бензол горить. Полум'я бензолу кіптяве з-за високого вмісту карбону в молекулі. Хімічні особливості бензолу Через особливого будови молекули, бензен займає проміжне положення між алканами і алкенами, тобто може вступати в реакції приєднання і в реакції заміщення.
Застосування бензену 1-добавка до бензину; виробництво 2-розчинників; 3-ацетону; 4-аніліну; 5-фенолу; 6-пестицидів; 7-ліків; 8-фенолформальдегідних пластмас. Поліщук Михайло
Схожі презентації
Категорії