Презентація на тему:
Сприйняття кольору, світла
Завантажити презентацію
Сприйняття кольору, світла
Завантажити презентаціюПрезентація по слайдам:
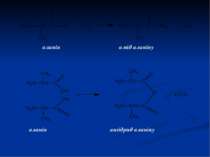
Амінокислоти – гетерофункціональні сполуки, молекули яких містять одночасно аміногрупу і карбоксильну. Загальна формула амінокислот:
Різноманітні пептиди і білки складаються із залишків α-амінокислот. Частіше за все термін "амінокислота" застосовують для позначення карбонових кислот, аміногрупа яких знаходиться в α- положенні, тобто для α-амінокислот.
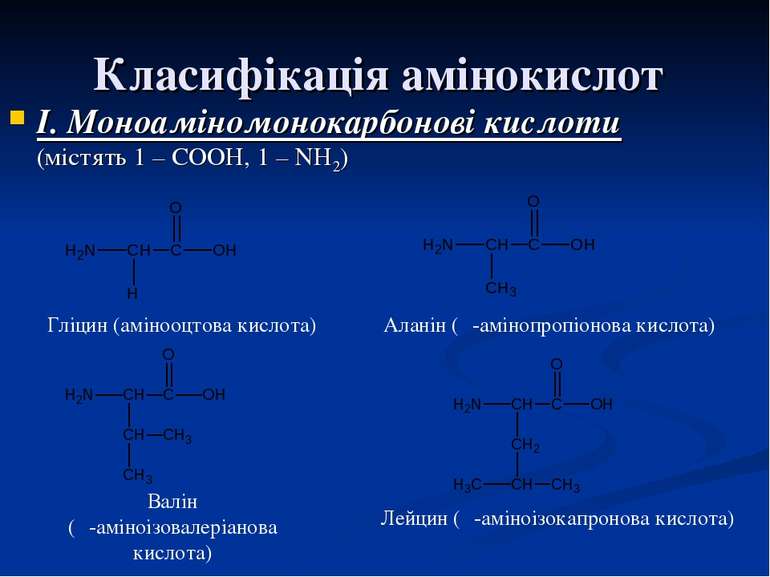
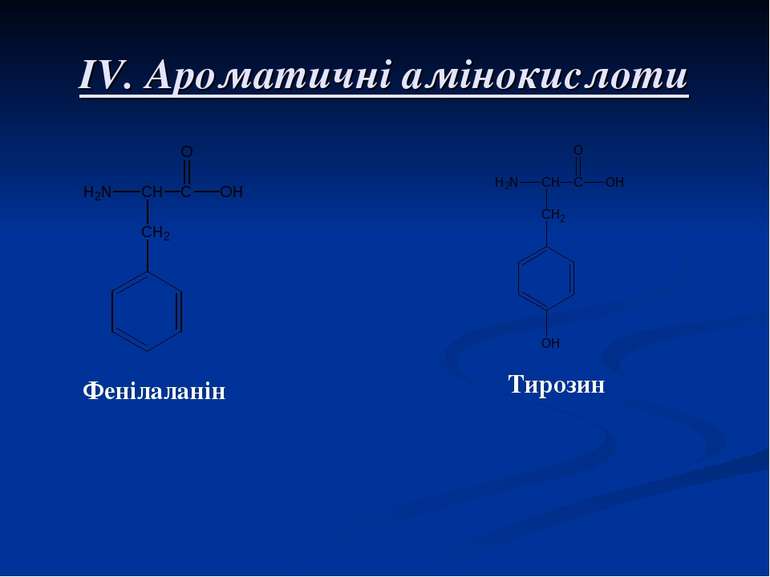
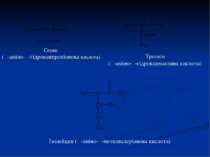
Класифікація амінокислот I. Моноаміномонокарбонові кислоти (містять 1 – СООН, 1 – NH2) Гліцин (амінооцтова кислота) Аланін (α-амінопропіонова кислота) Валін (α-аміноізовалеріанова кислота) Лейцин (α-аміноізокапронова кислота)
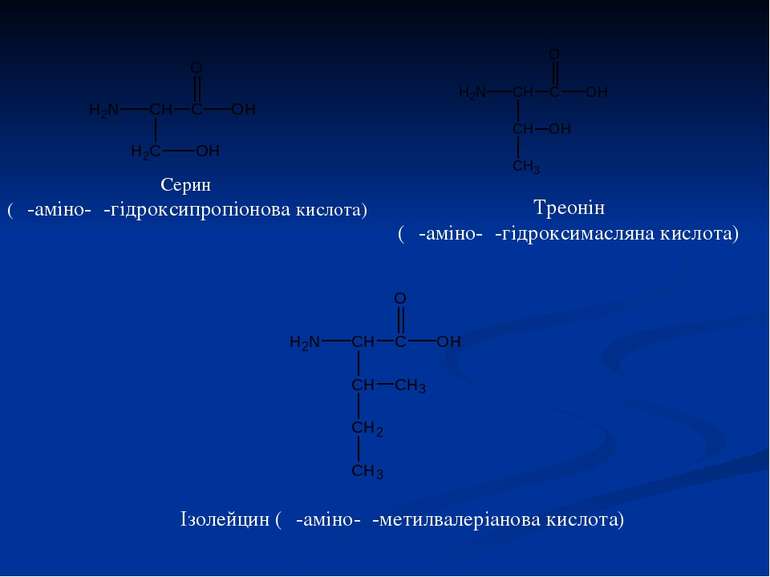
Треонін (α-аміно-β-гідроксимасляна кислота) Серин (α-аміно-β-гідроксипропіонова кислота) Ізолейцин (α-аміно-β-метилвалеріанова кислота)
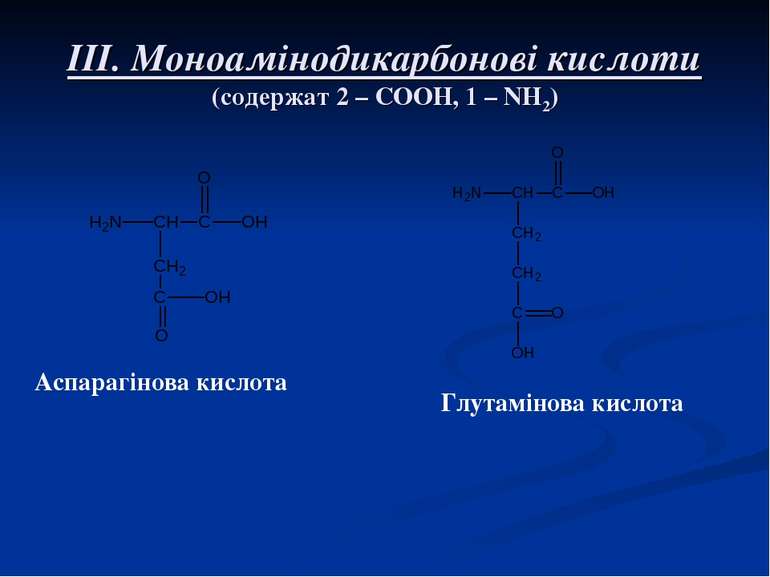
III. Моноамінодикарбонові кислоти (содержат 2 – СООН, 1 – NH2) Аспарагінова кислота Глутамінова кислота
Амінокислоти Замінні Гліцин Аланін Серин Цистеїн Аспарагінова кислота Глутамінова кислота Тирозин Пролін Аспарагін Глутамін Незамінні Треонін Метионін Валін Лейцин Ізолейцин Лізин Аргінін Фенілаланін Гістидин Триптофан
Ізомерія Разом з ізомерією, що обумовлена будовою вуглецевого скелету та положенням функціональних груп, для α-амінокислот характерна оптична (дзеркальна) ізомерія. Всі α-амінокислоти, крім гліцину, оптично активні. Наприклад, аланін має один асиметричний атом Карбону, а значить, існує у вигляді оптично активних енантіомерів: Д-аланін L-аланін Всі природні - амінокислоти відносяться до L– ряду.
Фізичні властивості Амінокислоти представляють собою кристалічні речовини з високими (вище 250 С) температурами плавлення, які мало відрізняються в індивідуальних амінокислот і тому не є характерними. Амінокислоти добре розчинні в воді і нерозчинні в органічних розчинниках, чим вони схожі на неорганічні сполуки. Більшість амінокислот мають солодкий смак. Амінокислоти, за винятком гліцину, оптично активні. В організмі всі α-амінокислоти L-ряду. Д-амінокислоти отримують синтетичним шляхом, вони зустрічаються в небілкових компонентах грибів, синтезуються мікроорганізмами. В організмі знезаражуються і виводяться з нього. На ці амінокислоті не діють ферменти.
Хімічні властивості 1. Дисоціація амінокислот: а) Моноаміномонокарбонові кислоти гліцин Білки, в складі яких переважає такий тип кислот, називаються нейтральними, рН розчинів яких ≈7
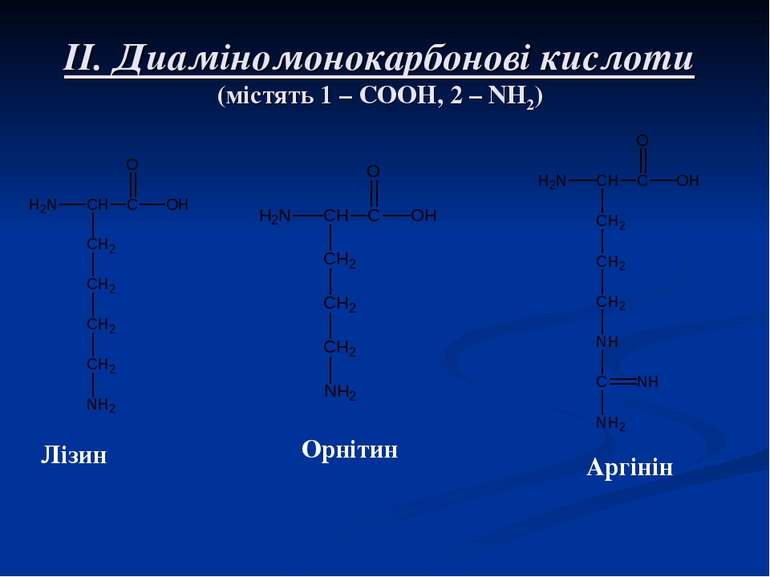
б) Диаміномонокарбонові кислоти лізин в) Моноамінодикарбонові кислоти Аспарагінова кислота Білки, в складі яких переважає такий тип кислот, називаються лужними, середовище лужне, рН>7. Білки, в складі яких переважно знаходяться дикарбонові кислоти, називаються кислими, середовище кисле, рН
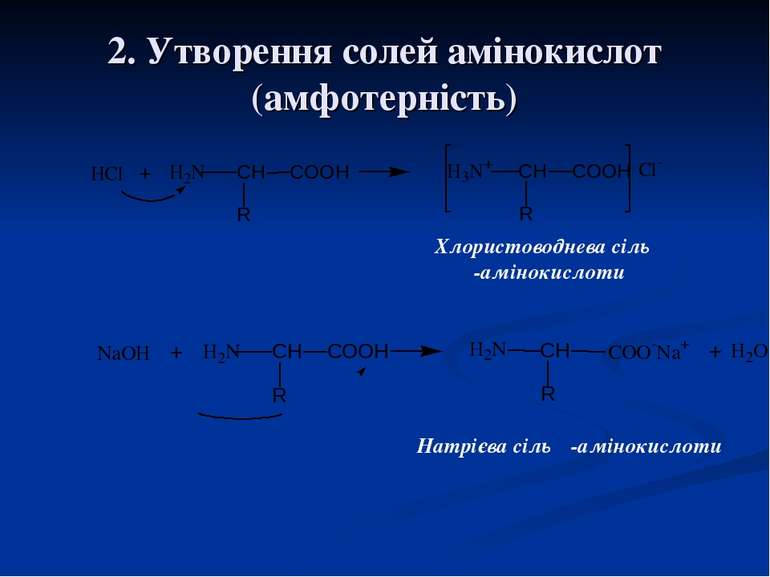
2. Утворення солей амінокислот (амфотерність) Хлористоводнева сіль α-амінокислоти Натрієва сіль α-амінокислоти
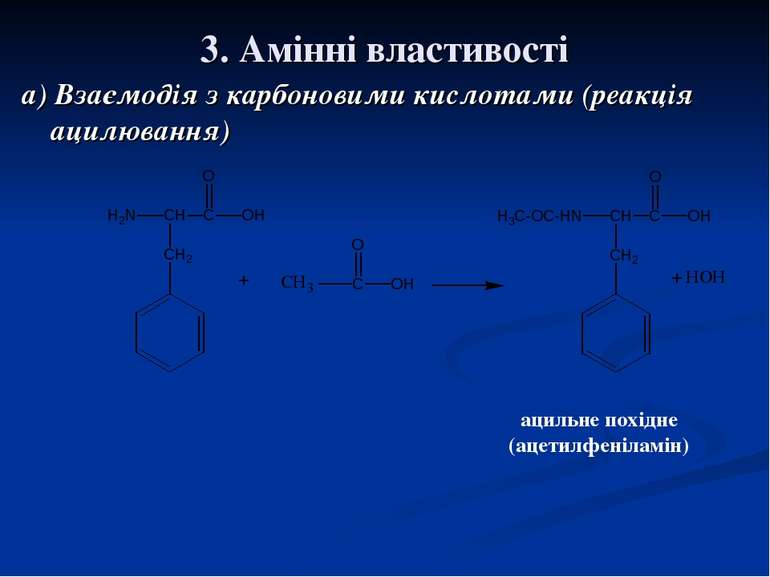
3. Амінні властивості а) Взаємодія з карбоновими кислотами (реакція ацилювання) ацильне похідне (ацетилфеніламін)
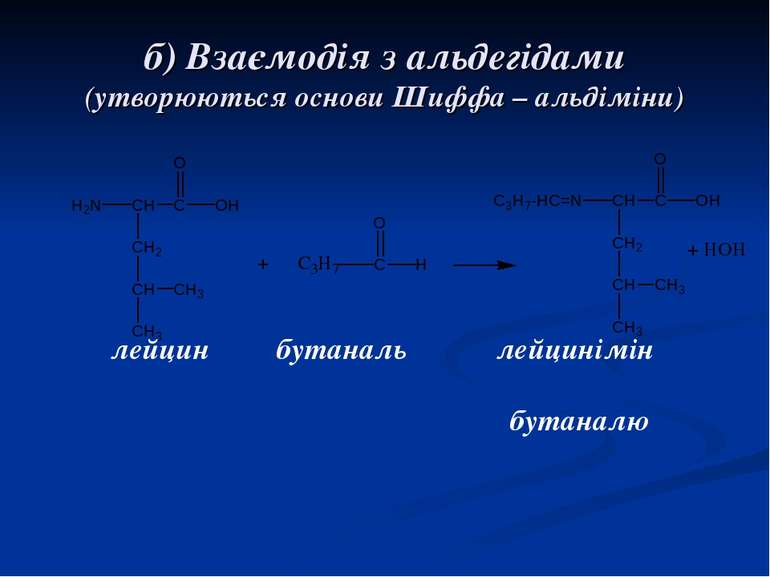
б) Взаємодія з альдегідами (утворюються основи Шиффа – альдіміни) лейцин бутаналь лейцинімін бутаналю
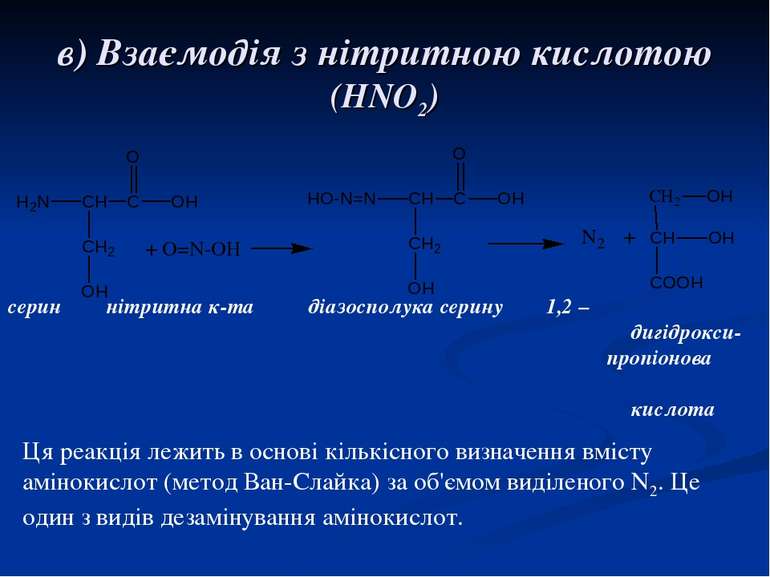
в) Взаємодія з нітритною кислотою (HNO2) серин нітритна к-та діазосполука серину 1,2 – дигідрокси- пропіонова кислота Ця реакція лежить в основі кількісного визначення вмісту амінокислот (метод Ван-Слайка) за об'ємом виділеного N2. Це один з видів дезамінування амінокислот.
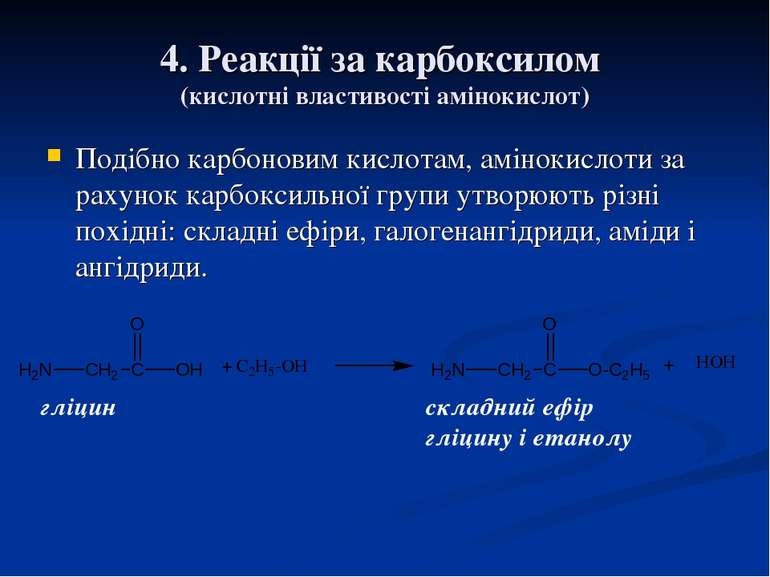
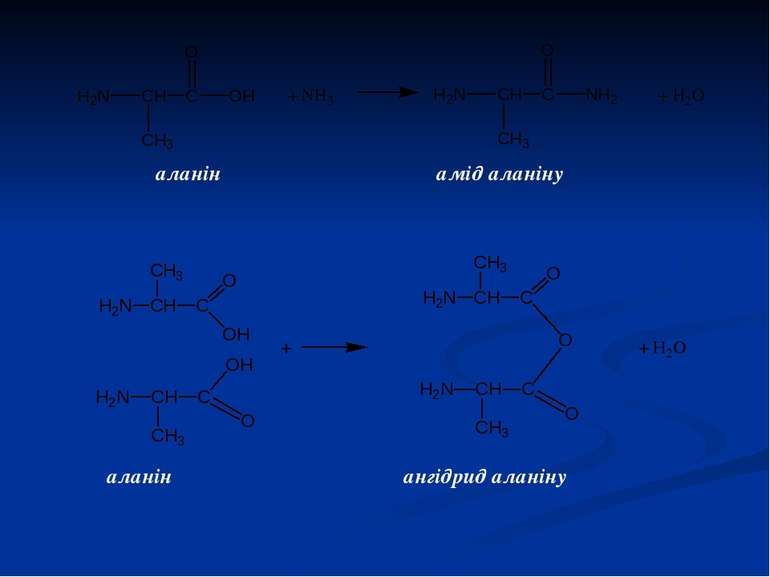
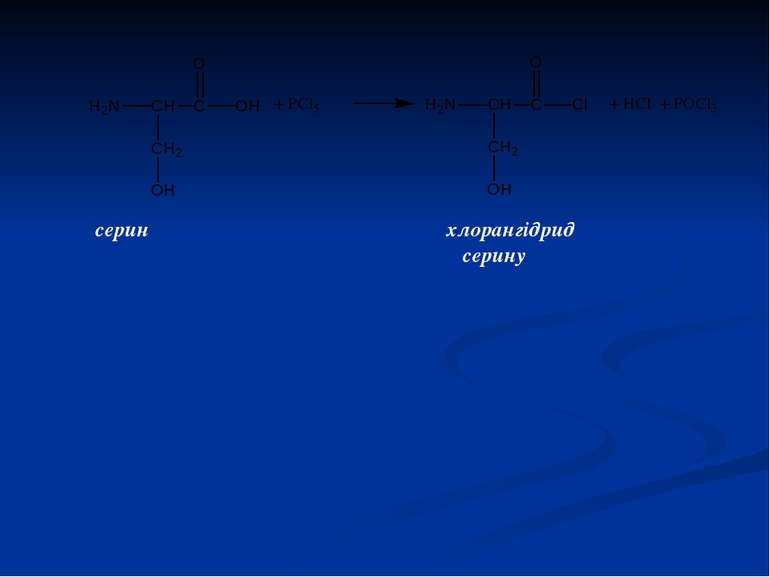
4. Реакції за карбоксилом (кислотні властивості амінокислот) Подібно карбоновим кислотам, амінокислоти за рахунок карбоксильної групи утворюють різні похідні: складні ефіри, галогенангідриди, аміди і ангідриди. гліцин складний ефір гліцину і етанолу
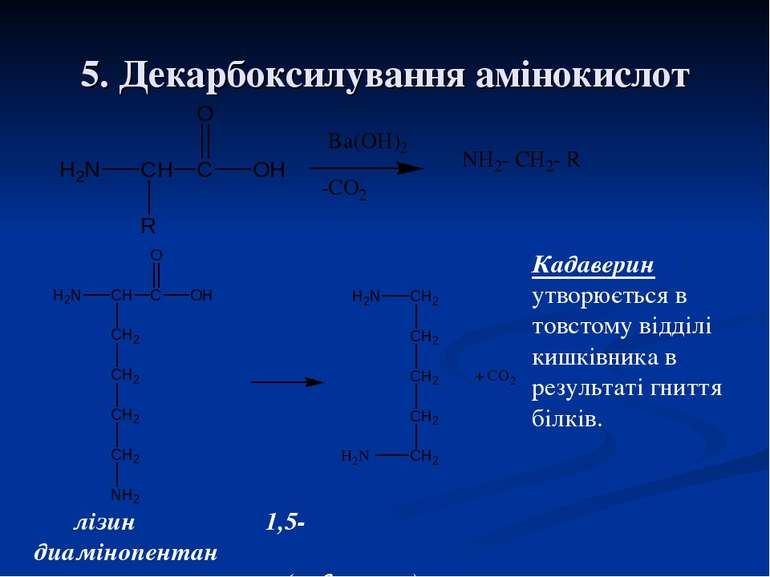
5. Декарбоксилування амінокислот лізин 1,5-диамінопентан (кадаверин) Кадаверин утворюється в товстому відділі кишківника в результаті гниття білків.
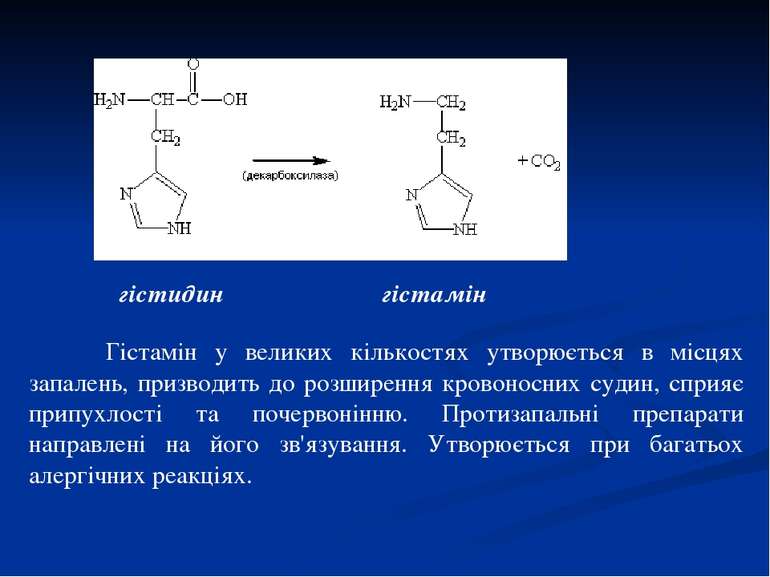
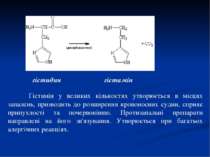
гістидин гістамін Гістамін у великих кількостях утворюється в місцях запалень, призводить до розширення кровоносних судин, сприяє припухлості та почервонінню. Протизапальні препарати направлені на його зв'язування. Утворюється при багатьох алергічних реакціях.
6. Специфічні властивості амінокислот Різне розташування карбоксильних і аміногруп в молекулах амінокислот надає їм деяких відмінних властивостей: в γ- і -амінокислотах можливою є внутрішньомолекулярна взаємодія карбоксилу і аміногрупи з виділенням води (внутрішньомолекулярне ацилювання аміногрупи). При цьому утворюються внутрішні циклічні аміди, що називаються лактами: γ-аміномасляна лактам аміномасляної кислота (ГАМК) кислоти ГАМК – метаболіт, утворюється в нервовій тканині, слугує для регулювання швидкості проведення нервових імпульсів (природний транквілізатор).
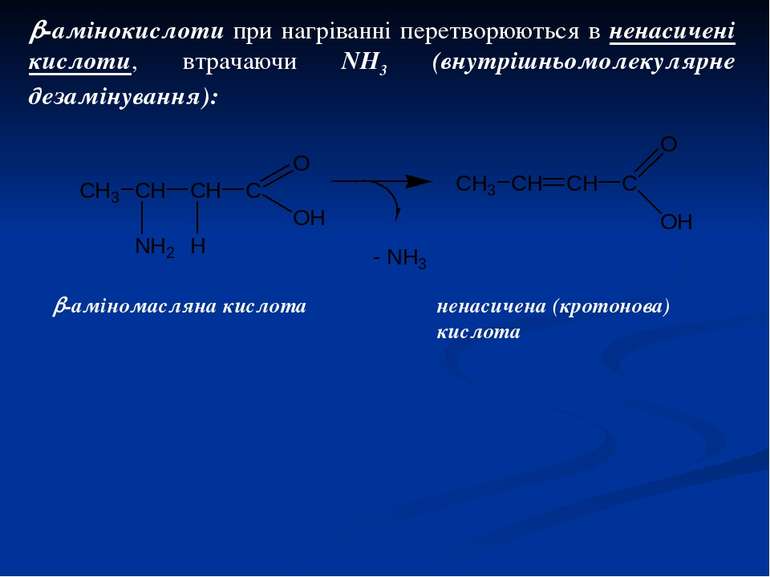
-амінокислоти при нагріванні перетворюються в ненасичені кислоти, втрачаючи NH3 (внутрішньомолекулярне дезамінування): -аміномасляна кислота ненасичена (кротонова) кислота
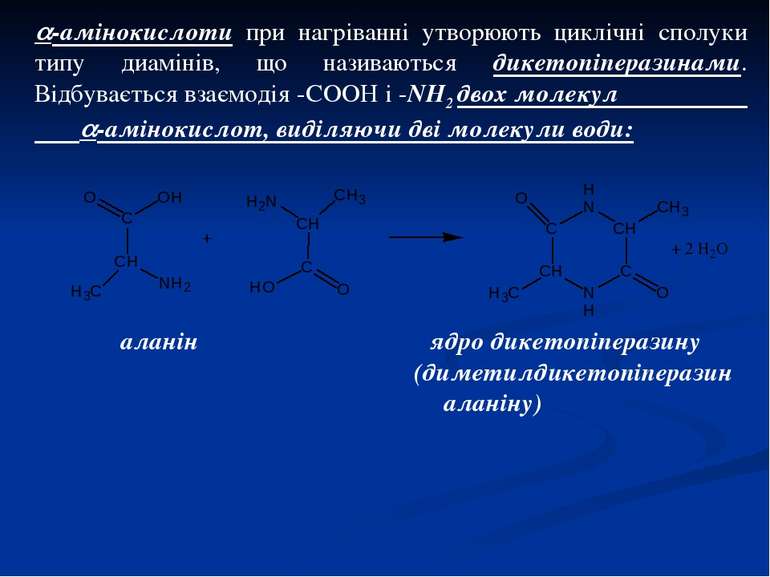
-амінокислоти при нагріванні утворюють циклічні сполуки типу диамінів, що називаються дикетопіперазинами. Відбувається взаємодія -СООН і -NH2 двох молекул -амінокислот, виділяючи дві молекули води: аланін ядро дикетопіперазину (диметилдикетопіперазин аланіну)
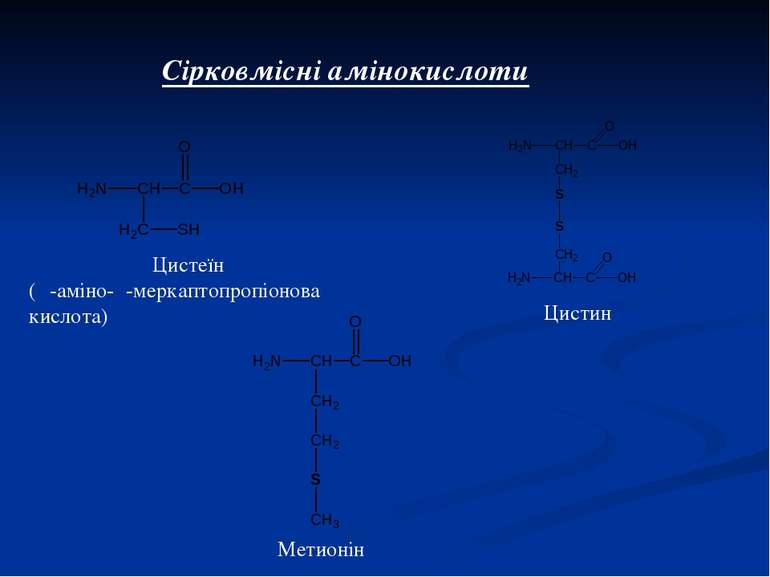
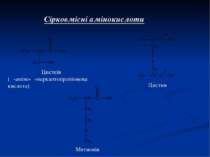
7. Утворення поліпептидів Метионін треонін цистеїн пептидные связи трипептид (метионіл-треоніл-цистеїн, мет-тре-цис)
Біологічна роль амінокислот 1. Амінокислоти називають «цеглинками життя», тобто білки складаються із залишків амінокислот. 2. Амінокислоти обумовлюють ріст і розвиток тварин, рівень їх продуктивності. 3. Синтезуються штучно, використовуються, як кормові і харчові добавки до раціонів людини і тварин. 4. Приймають участь у передаванні нервових імпульсів (гліцин, глутамінова кислота). 5. Утворюють аміни (гістамін, ГАМК), що виконують регуляторну функцію. 6. Кількісні зміни та порушення обміну амінокислот викликають захворювання.
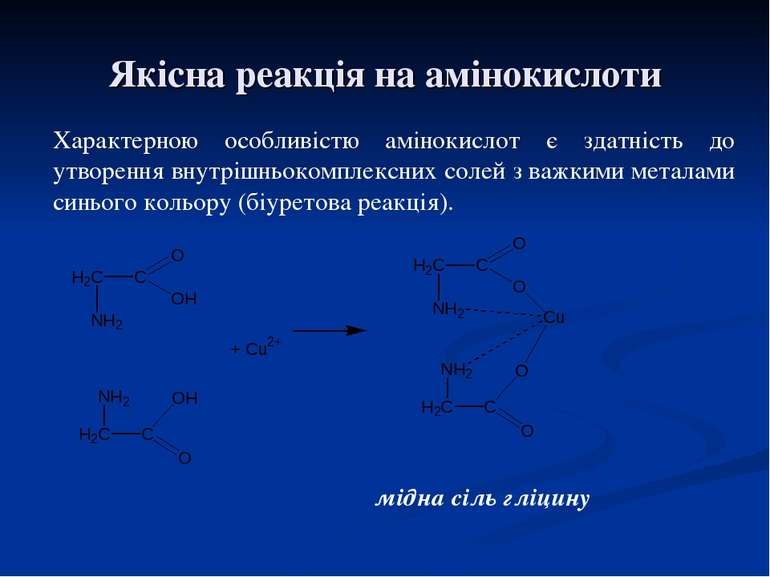
Якісна реакція на амінокислоти мідна сіль гліцину Характерною особливістю амінокислот є здатність до утворення внутрішньокомплексних солей з важкими металами синього кольору (біуретова реакція).
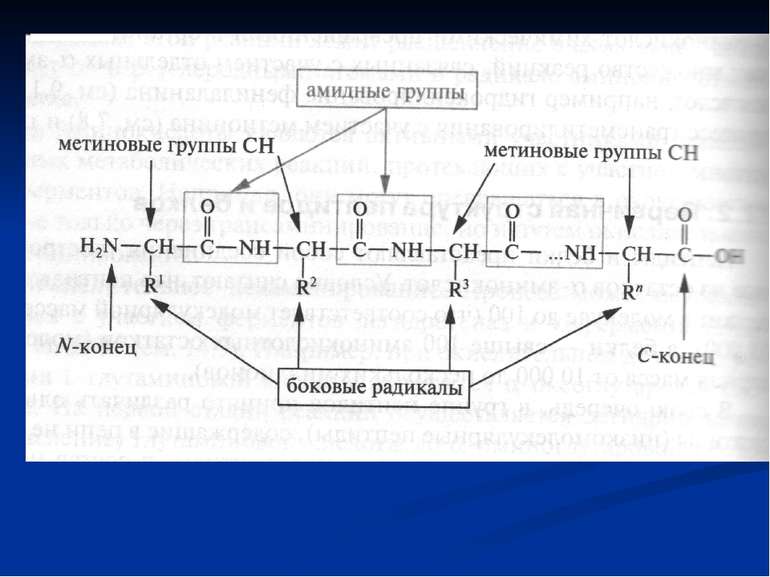
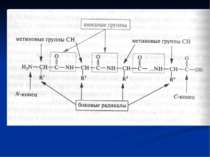
Пептиди і білки Пептиди і білки представляють собою високомолекулярні органічні сполуки, які побудовані із залишків α- амінокислот, з'єднаних між собою пептидними зв'язками.
Пептиди Пептид складається з двох або більшої кількості амінокислотних залишків, сполучених пептидними зв'язками (дипептид, трипептид ….). До 10 залишків – олігопептид, 10 і більше, то це поліпептид. Значення: 1. Деякі гормони (вазопресин, окситоцин, інсулін). 2. Антибіотики (валіноміцин, граміцидин А). 3. Протипухлинні препарати. 4. Фізіологічно активні речовини (брадикінін – розслабляє гладку мускулатуру. Глутатіон – модулятор ферментативної активності, утворює дисульфідні зв'язки). Як і амінокислоти, білки мають амфотерні властивості.
Білки Білки – біологічні полімерні молекули, мономерами яких є амінокислоти, сполучені пептидними зв'язками. Індивідуальність білкових молекул визначається порядком чергування амінокислот і їх кількістю. Білки мають м.м. від 5 тис. Д і більше.
Функції білків Каталітична – ферменти Пластична – структурні білки Регуляторна – гормони, ферменти Скорочувальна – білки м'язів і цитоскелету Захисна – імуноглобуліни Енергетична – використані білки Рецепторна – деякі білки мембран Транспортна – білки крові, білки мембран Гістосумісність – деякі білки мембран В організмі тварин білків - 18-21%, у рослин – 0,01-15%
Схожі презентації
Категорії