Презентація на тему:
Архітектура стародавнього Єгипту
Завантажити презентацію
Архітектура стародавнього Єгипту
Завантажити презентаціюПрезентація по слайдам:
Валентність Сьогодні ми продовжимо знайомство з початковими хімічними поняттями. Наступним таким поняттям є валентність. Що це таке і навіщо воно потрібне, нам і належить дізнатися на цьому уроці. Тема нашого уроку: “Валентність”.
Необхідні терміни: Речовина Складна речовина Проста речовина Молекула Атом Хімічний елемент Хімічна формула Але перш ніж перейти до нового терміну давайте пригадаємо ті, визначення яких ви вже знаєте і які знадобляться для вивчення нового матеріалу
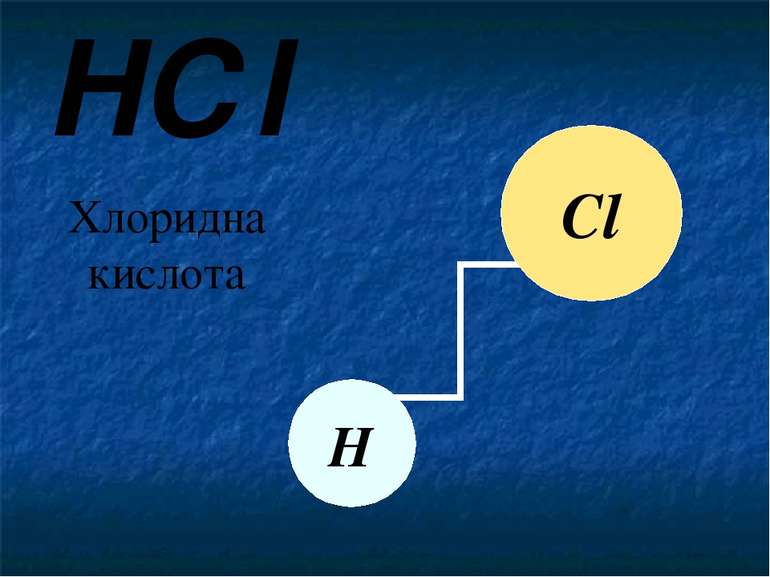
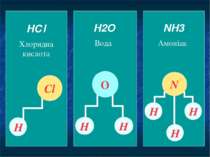
H2O Вода NH3 Амоніак HСl Хлоридна кислота Запишемо кілька хімічних речовин. Розглянемо більш докладно їх формули. Що вони означають?
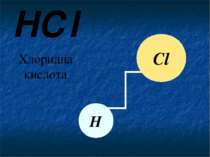
HСl Хлоридна кислота Сl Н Позначимо схематично зв'язок між атомами. Хлоридна кислота складається з одного атому Хлору (позначимо його жовтим колом) та одного атому Гідрогену (позначимо світло блакитним кольором). Між ними утворюється зв’язок (позначимо його прямою, яка зв'язує ці два атоми).
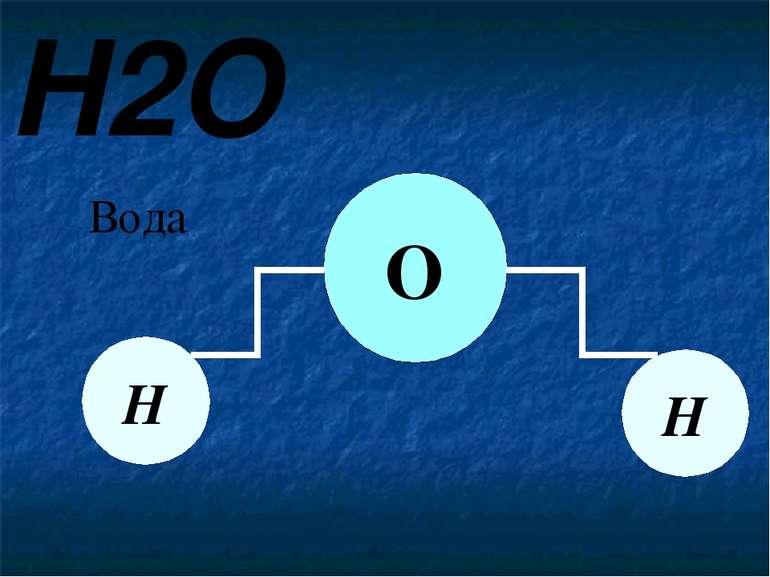
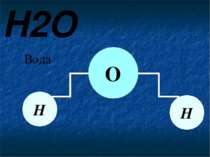
H2O Вода Н Н О Вода складається з двох атомів Гідрогену та одного атому Оксигену. Так схематично виглядає будова молекули води.
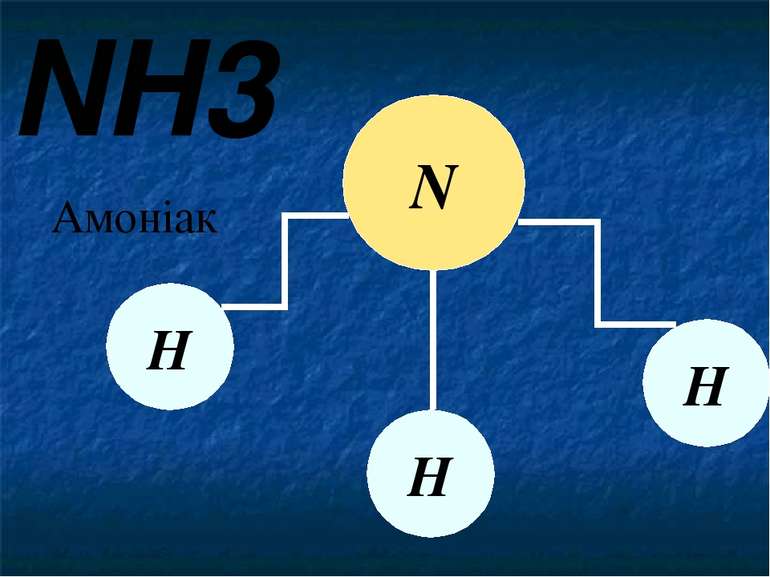
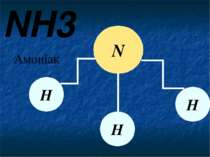
NH3 Амоніак N Н Н Н Молекула амоніаку складається з одного атому Нітрогену та трьох атомів Гідрогену. Ось що отрималось.
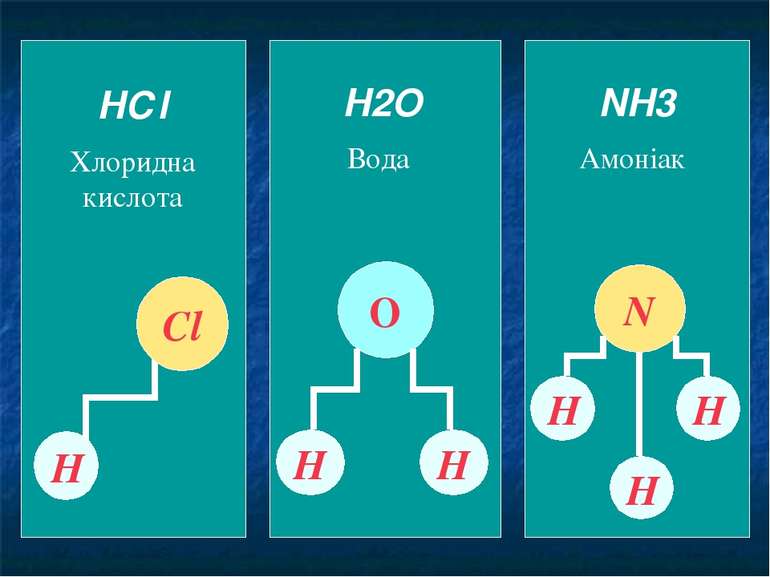
HСl Хлоридна кислота Н Сl H2O Вода Н Н О NH3 Амоніак N Н Н Н Як ви бачите різні атоми можуть утворювати тільки певну кількість зв'язків. Наприклад Гідроген – 1, Хлор – 1, Оксиген – 2, Нітроген - 3
Здатність атомів утворювати певну кількість зв'язків називається ВАЛЕНТНІСТЮ (записують у зошитах)
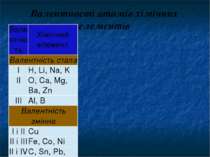
Атоми зі сталою валентністю H2O Вода Н Н О Na2O Натрій оксид Na О Na CaO Кальцій оксид Са О Одні атоми мають постійну валентність. Як, наприклад, Оксиген та Гідроген.
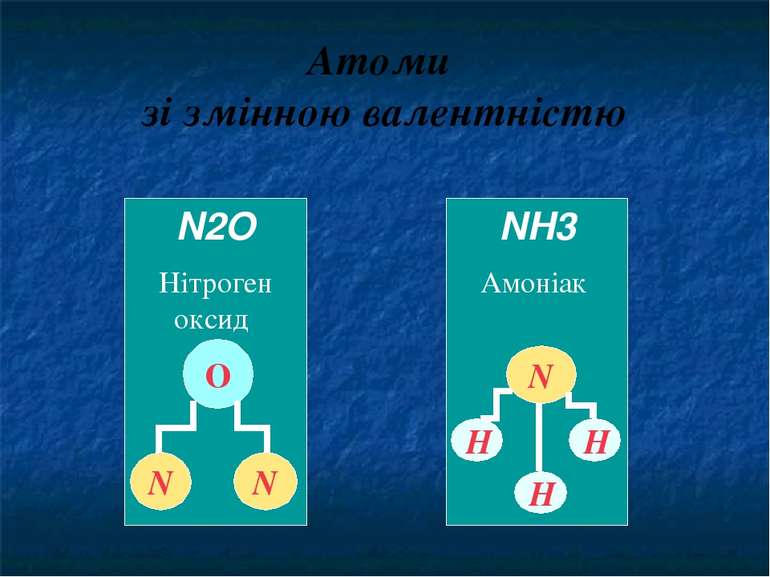
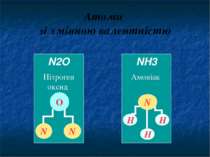
Атоми зі змінною валентністю NH3 Амоніак N Н Н Н N2O Нітроген оксид О N N А інші змінну, наприклад Нітроген. У сполуках Гідрогеном проявляє валентність І, а з Оксигеном може проявляти валентність ІІ.
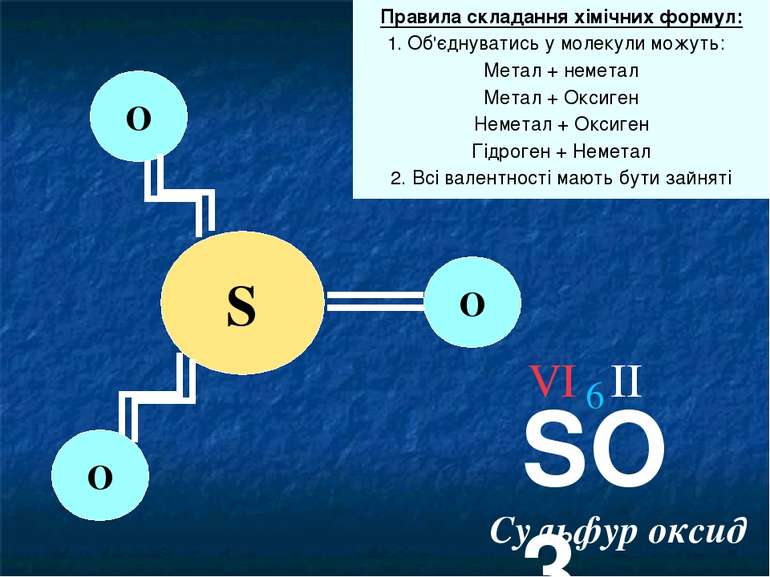
Правила складання хімічних формул: 1. Об'єднуватись у молекули можуть: Метал + неметал Метал + Оксиген Неметал + Оксиген Гідроген + Неметал 2. Всі валентності мають бути зайняті Щоб правильно складати хімічні формули, слід знати кілька правил. Одне з них пригадаємо: які комбінації атомів можуть поєднуватись у молекули? Тепер додамо ще одне не менш важливе: всі валентності мають бути зайняті
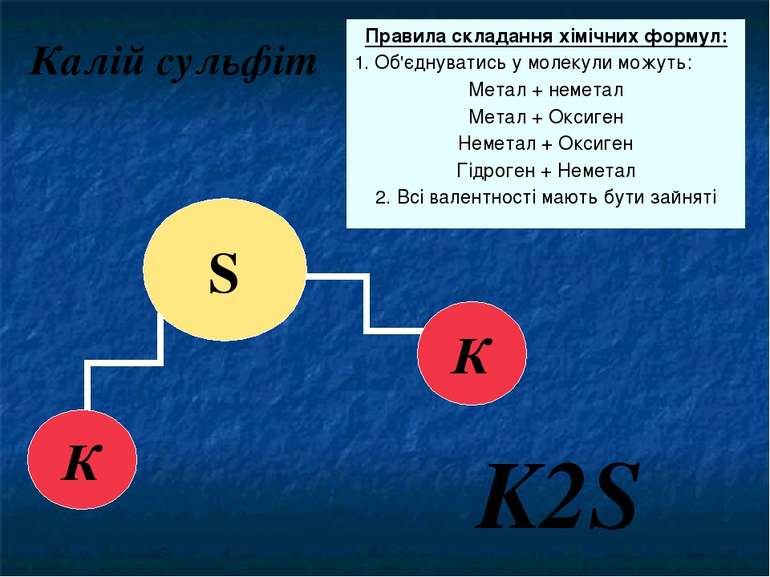
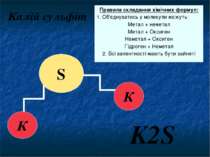
Калій сульфіт К К S K2S Правила складання хімічних формул: 1. Об'єднуватись у молекули можуть: Метал + неметал Метал + Оксиген Неметал + Оксиген Гідроген + Неметал 2. Всі валентності мають бути зайняті Спробуємо скласти формулу Калій сульфіду, якщо відомо що вона складається з К, який має валентність І та Сульфуру з валентністю ІІ. Ось, що тримали. Відповідно формула цієї сполуки К2S. Перевіримо, чи відповідає правилам наша формула.
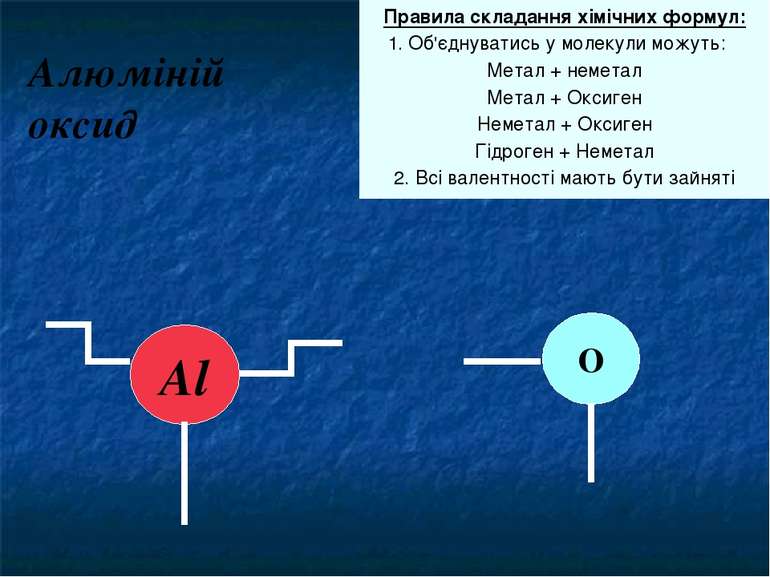
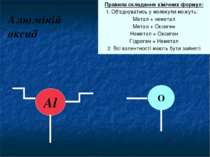
Алюміній оксид Правила складання хімічних формул: 1. Об'єднуватись у молекули можуть: Метал + неметал Метал + Оксиген Неметал + Оксиген Гідроген + Неметал 2. Всі валентності мають бути зайняті Al О Ускладнимо завдання. Спробуємо записати формулу Алюміній оксиду. Яка валентність Алюмінію? Оксигену?
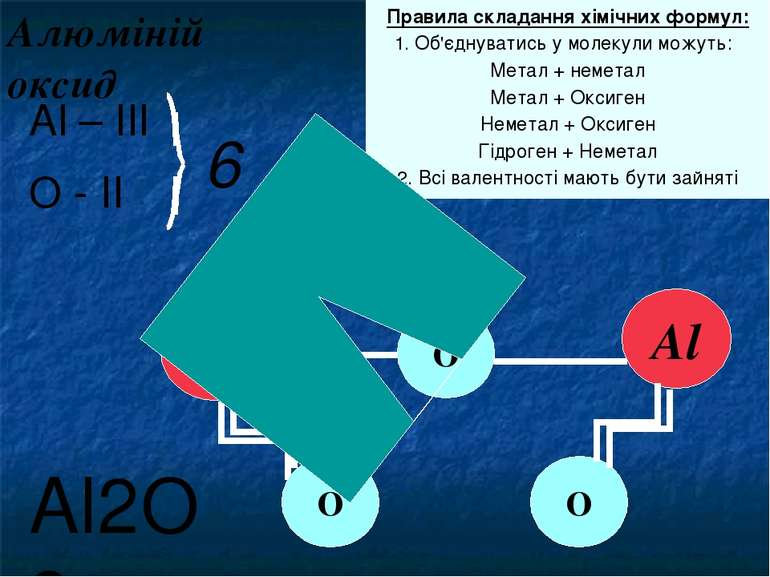
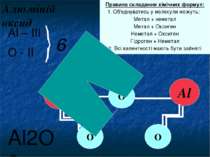
Алюміній оксид Правила складання хімічних формул: 1. Об'єднуватись у молекули можуть: Метал + неметал Метал + Оксиген Неметал + Оксиген Гідроген + Неметал 2. Всі валентності мають бути зайняті Al О О О Al Al – ІІІ О - ІІ 6 Al2O3 Ми визначили, що валентність Алюмінію дорівнює ІІІ, а Оксигену – ІІ. Яке число є спільним кратним для 2 і 3? - 6 Це означає, що до складу цієї сполуки входять 2 атоми Алюмінію і 3 атоми Оксигену Перевіримо!
4. Визначити і записати найменше спільне кратне валентностей для двох елементів 5. Розрахувати валентність невідомого елемента (Найменше спільне кратне / кількість атомів елемента з невідомою валентністю) Сульфур оксид Визначення валентностей хімічних елементів за формулами речовин SO3 Записати формулу речовини Позначити відомі валентності Записати загальну кількість валентностей відомого елемента (число валентностей х кількість атомів відповідного елемента) ІІ 6 VІ ЗКВ (О) = 2 х 3 = 6 В(S) = 6 / 1 = 6 6 Все дуже просто, коли ми можемо малювати, але це дуже довго. Спробуємо визначити валентності хімічних елементів використовуючи формули речовин, валентність одного елементу в якій ми вже знаємо. Для цього складемо алгоритм визначення валентностей хімічних елементів
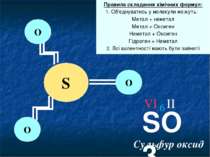
Правила складання хімічних формул: 1. Об'єднуватись у молекули можуть: Метал + неметал Метал + Оксиген Неметал + Оксиген Гідроген + Неметал 2. Всі валентності мають бути зайняті S О О О SO3 Сульфур оксид ІІ VІ 6 Перевіримо, чи відповідає валентність Сульфуру формулі. Чи правильно записана формула. Замалюємо структурну формулу Сульфур оксиду
Фосфор оксид Визначення валентностей хімічних елементів за формулами речовин Записати формулу речовини Позначити відомі валентності Записати загальну кількість валентностей відомого елемента (число валентностей х кількість атомів відповідного елемента) Визначити і записати найменше спільне кратне валентностей для двох елементів Розрахувати валентність невідомого елемента (Спільне кратне валентностей / кількість атомів елемента з невідомою валентністю) Р2О5 ІІ 10 V 10 Користуючись наведеним алгоритмом спробуємо визначити валентність Фосфору у фосфор оксиді
Схожі презентації
Категорії