Презентація на тему:
Марко Кропивницький
Завантажити презентацію
Марко Кропивницький
Завантажити презентаціюПрезентація по слайдам:
Загальна характеристика Причини виникнення кислотних дощів Механізм утворення кислотних опадів Показник кислотності Вплив кислотних дощів на екосистеми Вплив кислотних дощів на тваринний світ Корозія (металів) будинків і пам'ятників. Вплив кислотних дощів на людину Методи боротьби з кислотними опадами
Кислотний дощ утворюється в результаті реакції між водою і такими забруднюючими речовинами, як діоксид сірки (SO2) і різних оксидів азоту (NOx). Ці речовини викидаються в атмосферу автомобільним транспортом, у результаті діяльності металургійних підприємств і електростанцій, а також при спалюванні вугілля і деревини. Вступаючи в реакцію з водою атмосфери, вони перетворюються в розчини кислот: сірчаної, сірчистої, азотистої й азотної. Потім, разом із снігом чи дощем, вони випадають на землю. Природними джерелами надходження діоксиду сірки в атмосферу є головним чином вулкани і лісові пожежі. Тим часом природні надходження в атмосферу оксидів азоту зв'язані головним чином з електричними розрядами, при яких утвориться NO, згодом — NO2. Значна частина оксидів азоту природного походження переробляється в ґрунті мікроорганізмами, тобто включена в біохімічний колообіг.
Діоксид сірки, що потрапив в атмосферу, перетерплює ряд хімічних перетворень, що ведуть до утворення кислот. Частково діоксид сірки в результаті фотохімічного окислювання перетворюється в триоксид сірки (сірчаний ангідрид) SO3: 2SO2 + О2 → 2SO3,який реагує з водяною парою атмосфери, утворюючи аерозолі сірчаної кислоти: SO3 + Н2О → H2SO4.Основна частина діоксиду сірки, що викидається у вологому повітрі утворить аерозоль сірчистої кислоти і зображують умовною формулою Н2SO3: SO2 + H2O → H2SO3.Сірчиста кислота у вологому повітрі поступово окисляється до сірчаної: 2H2SO3 + O2 → 2H2SO4. Аерозолі сірчаної і сірчистої кислот приводять до конденсації водяної пари атмосфери і стають причиною кислотних опадів (дощі, тумани, сніг). При спалюванні палива утворяться тверді мікрочастинки сульфатів металів (в основному при спалюванні вугілля), легко розчинні у воді, що осаджуються на ґрунт і рослини, роблячи кислотними роси. Аерозолі сірчаної і сірчистої кислот складають близько 2/3 кислотних опадів, інше приходиться на частку аерозолів азотної й азотистої кислот, що утворяться при взаємодії діоксиду азоту з водяною парою атмосфери
Ступінь активності іонів водню у воді визначає водневий показник рН і являє собою кількісно виражений коефіцієнт кислотності або лужності води. Цей показник - рівень рН відображає ступінь кислотності або лужності води, а не кількість кислоти або лугу, що міститься в ній. Під зовнішнім впливом (наприклад, під впливом слабкої електрики) молекула води дисоціює на вільні водневі іони (Н +) і гідроксильну групу (ОН-). Підвищений вміст вільних водневих іонів робить воду кислотною, в той час як підвищений вміст групи ОН робить воду лужною. рН нейтральна вода має рівень рН 7, така вода містить рівну кількість Н + і ОН-або не містить їх взагалі. Вода з кислотною реакцією має рН нижче 7, з лужною реакцією - більше 7. Живі середовища організму, здебільшого, мають слаболужну реакцію. Чим нижче значення рН, тим вища кислотність. Якщо кислотність води нижче 5,5, то опади вважаються кислотними. Для визначення показника кислотності використовують різні рН-метри, зокрема дорогі електронні прилади. Простим способом визначення характеру середовища є застосування індикаторів — хімічних речовин, забарвлення яких змінюється в залежності від рН середовища. Найбільш розповсюджені індикатори — фенолфталеїн, метил-оранж, лакмус, а також природні барвники з червоної капусти і чорної смородини.
Об'єкти впливу: люди, тваринний і рослинний світ, водоймища, ґрунт, будівлі, пам'ятки культури, вироби з металу Кислотні дощі впливають на рослини через хвою чи листя та через закислений ґрунт. У дерев сповільнюється швидкість радіального росту, хвоя після первинного пошкодження стає доступною для шкідників, спостерігається хлороз і опадання хвої, відмирання гілок (знизу догори і від стовбура до периферії), повне засихання дерева. Сильне закислення лісових ґрунтів (на 1-1,5 одиниць рН) виникає в результаті вилужування поживних речовин під впливом кислих опадів і озону. Процес супроводжується переведенням нерозчинних сполук алюмінію (він є складовим компонентом глинистих ґрунтів) в розчині. Чим більший вміст розчинних форм алюмінію, тим інтенсивніше зменшується маса кореневої системи і відмирають кореневі волоски. Аналогічний ефект спричиняють і сполуки заліза. З підвищенням кислотності ґрунту і утворенням розчинних форм токсичних металів різко знижується біохімічна роль ґрунтових мікроорганізмів, пригнічується їх мікоризна активність.
У водяних екосистемах кислотні опади викликають загибель риб та інших водяних мешканців. Підкислення води рік і озер серйозно впливає і на сухопутних тварин, тому що багато звірів і птахів входять до складу харчових ланцюгів, що починаються у водяних екосистемах
Причиною руйнування металів є збільшення концентрації іона водню на поверхнях металу, від якої залежить його окислювання. У заміських зонах швидкість корозії металу -— кілька мікрометрів у рік, а в містах —100 мкм у рік і вище. Корозія заподіює збиток конструкціям мостів, резервуарам, лініям електропередач, машинному устаткуванню, транспорту. Кислотні дощі роз'їдають метали, фарби, синтетичні з'єднання, руйнують архітектурні пам'ятники. Багато скульптур і будинки в Римі, Венеції й інших містах, пам'ятники зодчества, такі, як Акрополь в Афінах, Кельнський собор та інші, за кілька останніх десятиліть одержали значно більші ушкодження, чим за весь попередій час. Під погрозою повного руйнування в результаті дії кислотних опадів знаходяться більш 50 тис. скульптур скельного «Міста Будд» під Юньанем у Китаї, побудованого 15 століть назад.
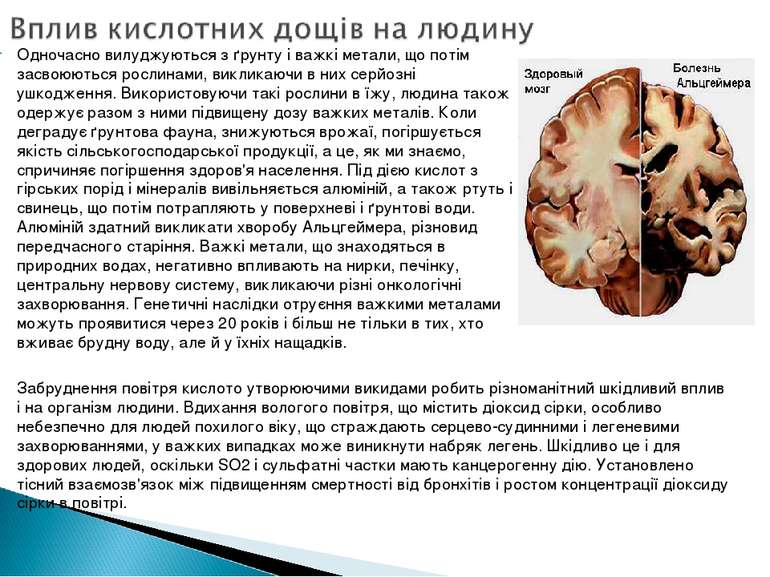
Одночасно вилуджуються з ґрунту і важкі метали, що потім засвоюються рослинами, викликаючи в них серйозні ушкодження. Використовуючи такі рослини в їжу, людина також одержує разом з ними підвищену дозу важких металів. Коли деградує ґрунтова фауна, знижуються врожаї, погіршується якість сільськогосподарської продукції, а це, як ми знаємо, спричиняє погіршення здоров'я населення. Під дією кислот з гірських порід і мінералів вивільняється алюміній, а також ртуть і свинець, що потім потрапляють у поверхневі і ґрунтові води. Алюміній здатний викликати хворобу Альцгеймера, різновид передчасного старіння. Важкі метали, що знаходяться в природних водах, негативно впливають на нирки, печінку, центральну нервову систему, викликаючи різні онкологічні захворювання. Генетичні наслідки отруєння важкими металами можуть проявитися через 20 років і більш не тільки в тих, хто вживає брудну воду, але й у їхніх нащадків. Забруднення повітря кислото утворюючими викидами робить різноманітний шкідливий вплив і на організм людини. Вдихання вологого повітря, що містить діоксид сірки, особливо небезпечно для людей похилого віку, що страждають серцево-судинними і легеневими захворюваннями, у важких випадках може виникнути набряк легень. Шкідливо це і для здорових людей, оскільки SO2 і сульфатні частки мають канцерогенну дію. Установлено тісний взаємозв'язок між підвищенням смертності від бронхітів і ростом концентрації діоксиду сірки в повітрі.
Необхідно знизити викиди оксидів сірки й азоту (SO2 , NO2 і NO) в атмосферу, але в першу чергу сірчаного газу, адже саме сірчана кислота та її солі на 70–80% обумовлюють кислотність дощів, які йдуть на великих відстанях від місця викиду; Зменшення кількості ТЕС за рахунок будівництва більш потужних, забезпечених новітніми системами очищення й утилізації (корисного використання) газу та пилу. Як відомо, одна потужна ТЕС забруднює повітря менше, ніж сотня котелень тієї самої сумарної потужності. Очищення вугілля до його надходження в топки ТЕС від піриту (сірчаного колчедану). Заміна вугілля та мазуту для ТЕС на екологічно чисте паливо – газ. ТЕС, які працюють на природному газі, крім СО (останній теж можна вилучити з диму), не викидають у повітря шкідливих газів. Регулювання двигунів внутрішнього згорання в автомобілі, встановлення на них спеціальних каталізаторів, що нейтралізують чадний газ до СО. Озеленення місті сіл. правильне планування житлових і промислових районів у межах міста
Схожі презентації
Категорії