Презентація на тему:
Загальні відомості про мінеральні добрива. Раціональне використання добрив та проблеми охорони рироди від забруднення продуктами та відходами хімічних виробництв. Роль хімії у розв'язанні продовольчої проблеми
Завантажити презентацію
Загальні відомості про мінеральні добрива. Раціональне використання добрив та проблеми охорони рироди від забруднення продуктами та відходами хімічних виробництв. Роль хімії у розв'язанні продовольчої проблеми
Завантажити презентаціюПрезентація по слайдам:
Загальні відомості про мінеральні добрива. Раціональне використання добрив та проблеми охорони рироди від забруднення продуктами та відходами хімічних виробництв. Роль хімії у розв'язанні продовольчої проблеми
Структура уроку І. Організаційний етап………………………1-2хв ІІ. Перевірка домашнього завдання………3-4хв ІІІ. Актуалізація опорних знань…………….5-6хв ІV. Вивчення нового матеріалу………....18-20хв 1. Загальна характеристика мінеральних добрив. 2. Нітратні добрива. 3. Фосфатні добрива. 4. Калійні добрива. 5. Вплив добрив на рослину. 6. Раціональне використання добрив та проблеми охорони природи від забруднення продуктами та відходами хімічних виробництв. V. Закріплення й узагальнення знань…….7-8хв 1.Практичне заняття «Починаючому фермеру». VІ. Домашнє завдання…………………….1-2хв VІІ. Оцінювання……………………………..1-2хв VІІІ. Підбиття підсумків уроку……………..1-2хв
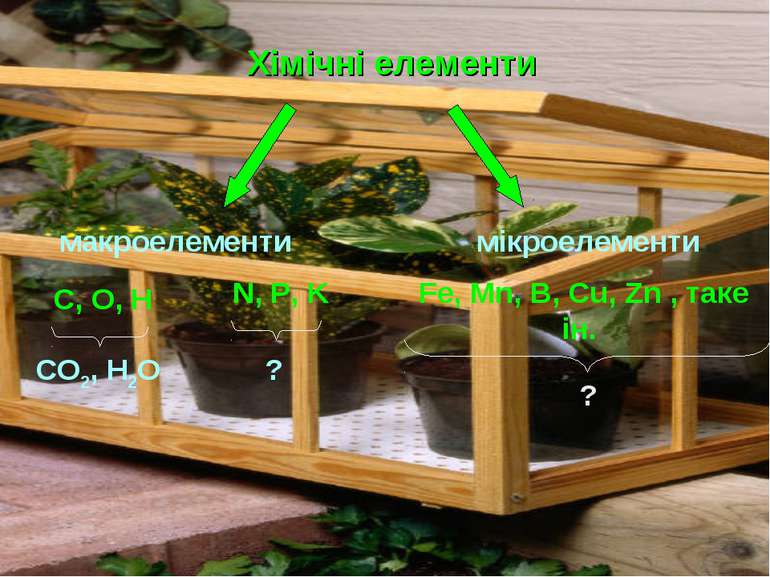
Хімічні елементи макроелементи мікроелементи С, О, Н N, P, K Fe, Mn, B, Cu, Zn , таке ін. СО2, Н2О ? ?
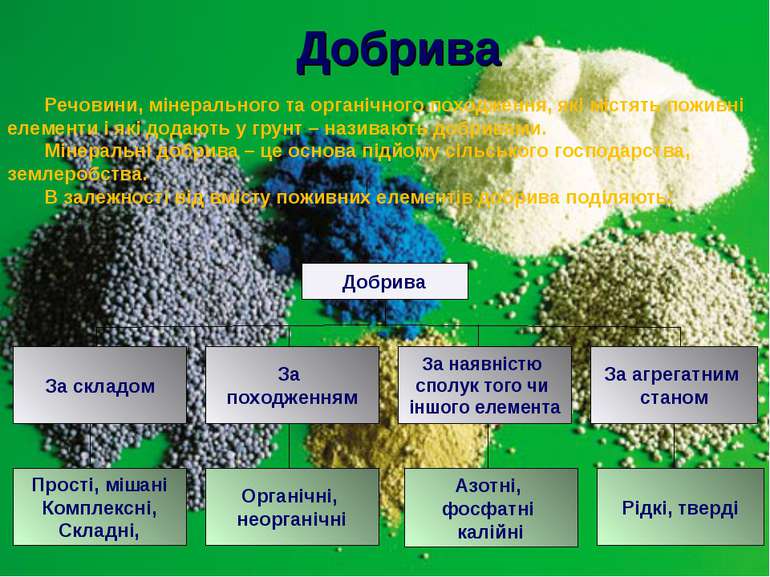
Добрива Добрива За складом За походженням За агрегатним станом За наявністю сполук того чи іншого елемента Азотні, фосфатні калійні Органічні, неорганічні Прості, мішані Комплексні, Складні, Рідкі, тверді Речовини, мінерального та органічного походження, які містять поживні елементи і які додають у грунт – називають добривами. Мінеральні добрива – це основа підйому сільського господарства, землеробства. В залежності від вмісту поживних елементів добрива поділяють:
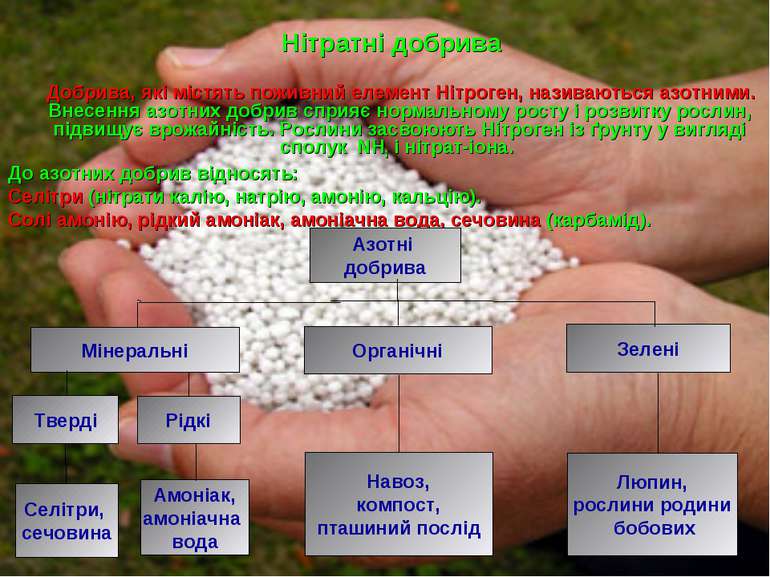
Нітратні добрива Добрива, які містять поживний елемент Нітроген, називаються азотними. Внесення азотних добрив сприяє нормальному росту і розвитку рослин, підвищує врожайність. Рослини засвоюють Нітроген із ґрунту у вигляді сполук NН3 і нітрат-іона. До азотних добрив відносять: Селітри (нітрати калію, натрію, амонію, кальцію). Солі амонію, рідкий амоніак, амоніачна вода, сечовина (карбамід). Азотні добрива Мінеральні Органічні Зелені Тверді Рідкі Селітри, сечовина Амоніак, амоніачна вода Навоз, компост, пташиний послід Люпин, рослини родини бобових
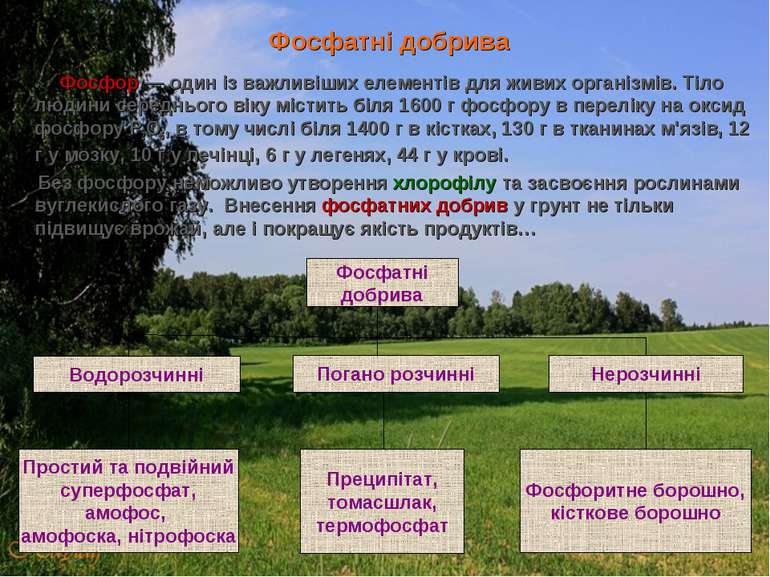
Фосфатні добрива Фосфор — один із важливіших елементів для живих організмів. Тіло людини середнього віку містить біля 1600 г фосфору в переліку на оксид фосфору Р2О5, в тому числі біля 1400 г в кістках, 130 г в тканинах м'язів, 12 г у мозку, 10 г у печінці, 6 г у легенях, 44 г у крові. Без фосфору неможливо утворення хлорофілу та засвоєння рослинами вуглекислого газу. Внесення фосфатних добрив у грунт не тільки підвищує врожай, але і покращує якість продуктів… Фосфатні добрива Водорозчинні Погано розчинні Нерозчинні Фосфоритне борошно, кісткове борошно Преципітат, томасшлак, термофосфат Простий та подвійний суперфосфат, амофос, амофоска, нітрофоска
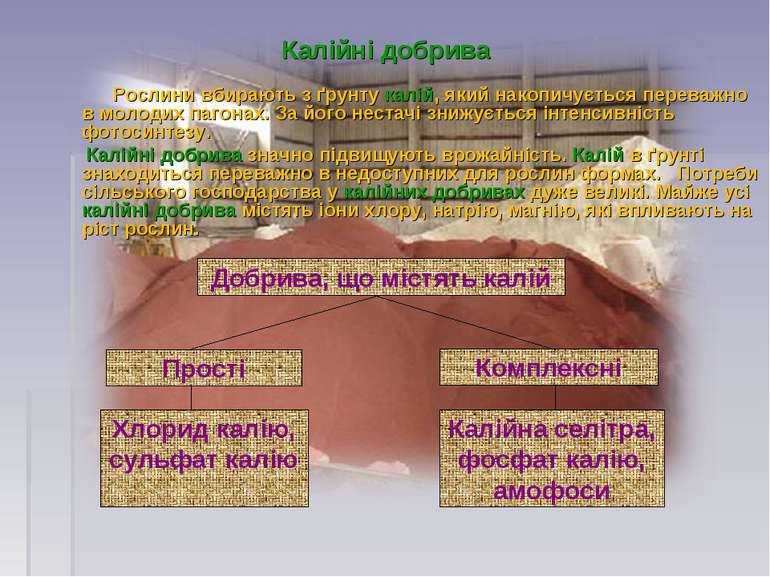
Калійні добрива Рослини вбирають з ґрунту калій, який накопичується переважно в молодих пагонах. За його нестачі знижується інтенсивність фотосинтезу. Калійні добрива значно підвищують врожайність. Калій в ґрунті знаходиться переважно в недоступних для рослин формах. Потреби сільського господарства у калійних добривах дуже великі. Майже усі калійні добрива містять іони хлору, натрію, магнію, які впливають на ріст рослин. Добрива, що містять калій Прості Комплексні Хлорид калію, сульфат калію Калійна селітра, фосфат калію, амофоси
Вплив добрив на рослину Група добрив Вплив поживного елемента на рослину Приклади добрив (формула, назва) Нітратні добрива Стимулюють ріст та збільшення зеленої маси рослин (стебла, листя). Важливі у весняний період. СО(NH2)- сечовина; NH4NO3 – амоніачна селітра; (NH4)2SO4 – сульфат амонію Фосфатні добрива Необхідні для росту репродуктивних органів (квіток, плодів). Са(Н2РО4)2 – подвійний суперфосфат; СаНРО4* 2Н2О – преципітат; Са(Н2РО4)2 + Са SO4 – простий суперфосфат Калійні добрива Прискорюють фотосинтез, сприяють накопиченню вуглеводів, укріплюють стебла злакових рослин Зола (К2СО3); КCl*NaCl – сильвініт; К2SO4 – сульфат калію. Мікродобрива Сприяють синтезу цукру, білків, крохмалю, вітамінів, нуклеїнових кислот, ферментів. Сu – сприяє росту рослин на бідних ґрунтах, підвищує стійкість до посухи, холоду. Fe – бере участь у синтезі хлорофілу. У складі мінеральних комплексів.
Недостача поживних елементів: Пожовкле нижнє листя — ознака нестачі азоту Ознаки нестачі фосфору у листках. Пожовтіння та одмирання на кінчиках листів — ознака нестачі калію.
Надлишок мінеральних речовин у ґрунті: Гостре отруєння (алергічний набряк легень, задишка, біль в області серця, кашель, блювота и др.).
Пізньою осінню, розорав землю, фермер вирішив що називається вбити двох зайців одразу: вапнувати ділянки з кислим ґрунтом та провести підкормку її суперфосфатом (все ж таки повірив, що без хімії не обійтися). Але весною з'ясувалося, що бажаного результату не досягнуто. Чому? Задача-невдача №1
Допомога фермеру Са(Н2РО4)2 + 2Са(ОН)2 Са3(РО4)2 ↓ + 4Н2О осад До якого типу відноситься реакція? До яких класів сполук відносяться дані речовини? Назвіть ці речовини.
Задача-невдача №2 Досвідчений сусід, пожалів молодого фермера, запропонував виправити помилку, вносячи в грунт добре розчинне добриво, яке містить фосфор. Сусід забув назву добрива, але приніс акуратний запис результатів його аналізу (%): Нітрогену – 12,2, Гідрогену – 5,5, Фосфору – 27,0, Оксигену – 55,6. Що це за речовина?
Допомога фермеру Дано: Розв'язок: W(N) = 12,2% Відношення елементів у речовині W(Н) = 5,5% N : Н : Р : О = W(Р) = 27,0% 12,2/14 : 5,5/1 : 27,0/31 : 55,6/16 = W(О) = 55,6% 0,87 : 5,5 : 0,87 : 3,47 = ______________ 1 : 6 : 1 : 4 Формула ? NН6РО4 або NН4 Н2РО4 Відповідь: NН4 Н2РО4 – дігідрофосфат амонію
Задача-невдача №3 Для обприскування саду фермеру знадобилось приготувати бордоську рідину. В інструкції було вказано, що потрібен 7% розчин купрум (ІІ) сульфату. Але у мішку були тільки яскраво – сині кристали мідного купоросу – п'ятиводного кристалогідрату. Як приготувати розчин потрібної концентрації?
Дано: Розв'язок: W(СuSO4)= 7% СuSO4 * 5Н2О = СuSO4 + 5Н2О m (р-ну)=10 кг. W = m (роз. реч.) / m (р-ну) Приготувати розчин: 1) m (СuSO4) = 10000*0,07=700г. m (роз. реч.) - ? 2)160 г. - 250 г. m (Н2О) - ? 700г. - х , х=1093,7г. М (СuSO4*5Н2О)=250 г/моль М(СuSO4)=160г/моль 3) 10000-1093,7=8906,3г. води Відповідь: на 10 кг. р-ну потрібно взяти: 1 кг. 93 г. СuSO4 * 5Н2О 8906,3г. води. Допомога фермеру
Задача-невдача №4 Фермер узяв оцинковане відро, відміряв потрібну кількість соли та води. Потім пішов до сараю за вапном. Що він побачив повернувшись?
Опрацювати матеріал параграфа, відповісти на запитання до нього, виконати вправи. Творче завдання: Створити рекламу або «антирекламу» мінеральних добрив
Схожі презентації
Категорії